(1)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。完成下列填空:
①As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体. 若As2S3和SnCl2恰好完全反应,As2S3和SnCl2的物质的量之比为_______ .该反应的氧化剂是_____ ,反应产生的气体可用_______ 吸收.
②As2S3和HNO3有如下反应:__ As2S3+__ NO3-+__ ___ =__ H3AsO4+__ S+__ NO2↑+__ _____
A.将方程式补充完整并配平
B.若生成1 mol H3AsO4,则反应中转移电子的物质的量为________ .
(2)某温度下将Cl2通入KOH溶液中,反应后得到KCl,KClO和KClO3的混合溶液,经测定ClO-和 的物质的量浓度之比为7:1,则Cl2与KOH反应时,氧化剂和还原剂物质的量之比为
的物质的量浓度之比为7:1,则Cl2与KOH反应时,氧化剂和还原剂物质的量之比为___ .若5mol Cl2参加反应,转移电子数为______________ (用NA表示阿伏加 德罗常数)
(3)某一反应体系中有反应物和生成物共五种物质:S,H2S,HNO3,NO,H2O. 该反应的化学方程式为______________________ ;若反应过程中转移了0.3mol电子,则氧化产物的质量是______ g;
①As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体. 若As2S3和SnCl2恰好完全反应,As2S3和SnCl2的物质的量之比为
②As2S3和HNO3有如下反应:
A.将方程式补充完整并配平
B.若生成1 mol H3AsO4,则反应中转移电子的物质的量为
(2)某温度下将Cl2通入KOH溶液中,反应后得到KCl,KClO和KClO3的混合溶液,经测定ClO-和
 的物质的量浓度之比为7:1,则Cl2与KOH反应时,氧化剂和还原剂物质的量之比为
的物质的量浓度之比为7:1,则Cl2与KOH反应时,氧化剂和还原剂物质的量之比为(3)某一反应体系中有反应物和生成物共五种物质:S,H2S,HNO3,NO,H2O. 该反应的化学方程式为
更新时间:2019-12-08 16:42:15
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】26.铁、铝、铜及其化合物在生产、生活中有广泛的用途,试回答下列问题:
(1)制造电路板的工艺中,FeCl3溶液可以蚀刻铜箔,请写出该反应的离子方程式_______________ ;
(2)已知铜与稀硫酸不反应,但将铜片在稀硫酸中长时间加热时溶液会呈蓝色,请用化学方程式表示原因_____________________ 。
(3)氯化铝广泛用于有机合成和石油工业的催化剂。将铝土矿粉(主要成分为Al2O3)与焦炭混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式____________________ 。
(4)已知Cu2S可以和硝酸反应,请配平下列化学反应方程式:
_____ Cu2S+_____ HNO3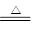
_____ CuSO4 + _____ Cu(NO3)2+_____ NO↑+ _____
(5)某校兴趣小组欲测定一种铁铝硅合金(FexAlySiz)粉末的组成,提出如下方案:准确称取1.46g该合金粉末,加入过量盐酸溶液充分反应后过滤,测定剩余固体质量0.07g。向滤液中滴加足量浓NaOH溶液,充分搅拌、过滤、洗涤得固体。再将所得固体充分加热、灼烧得红棕色粉末1.60g,通过计算确定此合金的组成为_______ (填化学式)。
(1)制造电路板的工艺中,FeCl3溶液可以蚀刻铜箔,请写出该反应的离子方程式
(2)已知铜与稀硫酸不反应,但将铜片在稀硫酸中长时间加热时溶液会呈蓝色,请用化学方程式表示原因
(3)氯化铝广泛用于有机合成和石油工业的催化剂。将铝土矿粉(主要成分为Al2O3)与焦炭混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式
(4)已知Cu2S可以和硝酸反应,请配平下列化学反应方程式:
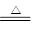
(5)某校兴趣小组欲测定一种铁铝硅合金(FexAlySiz)粉末的组成,提出如下方案:准确称取1.46g该合金粉末,加入过量盐酸溶液充分反应后过滤,测定剩余固体质量0.07g。向滤液中滴加足量浓NaOH溶液,充分搅拌、过滤、洗涤得固体。再将所得固体充分加热、灼烧得红棕色粉末1.60g,通过计算确定此合金的组成为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选。正极材料的选择决定了锂离子电池的性能。磷酸亚铁锂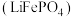 以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
(1)高温固相法是生产磷酸亚铁锂的主要方法。通常以亚铁盐、磷酸盐和锂盐为原料,按化学计量比充分混匀后,在惰性气氛中先经过较低温预分解,再经高温焙烧,最后研磨粉碎制成。请回答下列问题:
①补充完整该反应的化学方程式: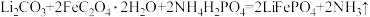
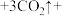
_____ 
______ 。
②理论上,反应中每转移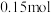 电子,会生成
电子,会生成
_____ g。
③反应需在惰性气氛中进行,其原因是____________ 。
(2)磷酸亚铁锂电池装置如图所示,其中正极材料橄榄石型 通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
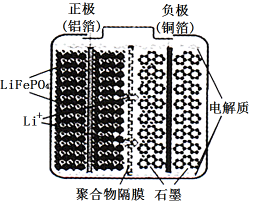
电池工作时的总反应为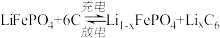 ,则放电时,正极的电极反应式为
,则放电时,正极的电极反应式为________ ,充电时, 迁移方向为
迁移方向为_____ (填“由左向右”或“由右向左”),图中聚合物隔膜应为_____ (填“阳”或“阴”)离子交换膜。
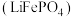 以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。(1)高温固相法是生产磷酸亚铁锂的主要方法。通常以亚铁盐、磷酸盐和锂盐为原料,按化学计量比充分混匀后,在惰性气氛中先经过较低温预分解,再经高温焙烧,最后研磨粉碎制成。请回答下列问题:
①补充完整该反应的化学方程式:
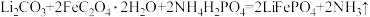
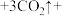

②理论上,反应中每转移
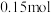 电子,会生成
电子,会生成
③反应需在惰性气氛中进行,其原因是
(2)磷酸亚铁锂电池装置如图所示,其中正极材料橄榄石型
 通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
电池工作时的总反应为
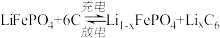 ,则放电时,正极的电极反应式为
,则放电时,正极的电极反应式为 迁移方向为
迁移方向为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】已知Ca(OH)2与Cl2反应的氧化物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应),生成物中含有Cl-、ClO-、 三种含氧元素的离子,其中ClO-、
三种含氧元素的离子,其中ClO-、 两种离子的物质的量(n)与反应时间(t)的曲线
两种离子的物质的量(n)与反应时间(t)的曲线
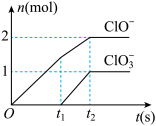
(1)t1前,氧化产物是_____________ (填化学式)。
(2)t2时,石灰乳与Cl2发生反应的总的离子方程式为:_______________ 。
(3)该反应中所消耗氯气的物质的量是______ mol。
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是__________(填字母)。
(5)配平下列离子方程式:Fe(OH)3+ClO-+OH-= +Cl-+H2O
+Cl-+H2O___________ 。
 三种含氧元素的离子,其中ClO-、
三种含氧元素的离子,其中ClO-、 两种离子的物质的量(n)与反应时间(t)的曲线
两种离子的物质的量(n)与反应时间(t)的曲线
(1)t1前,氧化产物是
(2)t2时,石灰乳与Cl2发生反应的总的离子方程式为:
(3)该反应中所消耗氯气的物质的量是
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是__________(填字母)。
| A.NaCl、Cl2 | B.NaCl、NaClO | C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
 +Cl-+H2O
+Cl-+H2O
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。
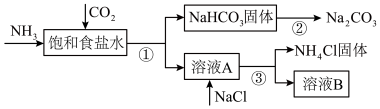
(1)饱和食盐水中通二氧化碳和氨气的化学方程式是_______
(2)下列说法中合理的是_______(填标号)。
(3)一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,在疫情期间外出需戴好口罩,返家后立即杀菌消毒。双氧水和84消毒液是日常生活常用的消毒剂,二氧化氯 气体是一种常用高效的自来水消毒剂。
气体是一种常用高效的自来水消毒剂。
①某同学设计如下实验研究 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是_______ (填序号)
②某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
_______  (填“>”或“<”);当有
(填“>”或“<”);当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为_______ mol。
③ 和浓盐酸在一定温度下反应会生成
和浓盐酸在一定温度下反应会生成 和
和 ,该反应的离子方程式
,该反应的离子方程式_______ ,将 通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式_______ 。

(1)饱和食盐水中通二氧化碳和氨气的化学方程式是
(2)下列说法中合理的是_______(填标号)。
A.副产物 可用作氮肥 可用作氮肥 |
B.溶液B中的主要离子是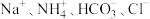 |
C.制碱流程中可回收并循环利用的物质只有碳酸氢钠分解产生的 |
| D.饱和食盐水中应该先通二氧化碳至饱和,再通入氨气至饱和 |
 气体是一种常用高效的自来水消毒剂。
气体是一种常用高效的自来水消毒剂。①某同学设计如下实验研究
 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是| 序号 | 实验 | 实验现象 |
| 1 | 向 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色裉去;b.有大量气泡产生 |
| 2 | 向 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
 (填“>”或“<”);当有
(填“>”或“<”);当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为③
 和浓盐酸在一定温度下反应会生成
和浓盐酸在一定温度下反应会生成 和
和 ,该反应的离子方程式
,该反应的离子方程式 通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:
H++ MnO4-+ H2C2O4— CO2↑+ Mn2++
(1)配平以上离子方程式,并在 中填上所需的微粒。
中填上所需的微粒。_____________
(2)该反应中的还原剂是___________________ 。
(3)测定血钙的含量的方法:取2 mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液与其反应。
①稀硫酸溶解CaC2O4沉淀的化学方程式是________________________ 。
②溶解沉淀时____ (“能”或“不能”)用稀盐酸,原因是________________ 。
③若消耗了1.0×10-4mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙____ mg。
H++ MnO4-+ H2C2O4— CO2↑+ Mn2++

(1)配平以上离子方程式,并在
 中填上所需的微粒。
中填上所需的微粒。(2)该反应中的还原剂是
(3)测定血钙的含量的方法:取2 mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液与其反应。
①稀硫酸溶解CaC2O4沉淀的化学方程式是
②溶解沉淀时
③若消耗了1.0×10-4mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】Ⅰ.煤炭中以FeS2形式存在的硫,在有水和空气及在脱硫微生物存在下发生生物氧化还原反应,有关反应的离子方程式依次为:
①2FeS2+7O2+2H2O 4H++2Fe2++4SO
4H++2Fe2++4SO ;
;
②Fe2++O2+H+ Fe3++________;
Fe3++________;
③FeS2+2Fe3+ 3Fe2++2S;
3Fe2++2S;
④2S+3O2+2H2O 4H++2SO
4H++2SO 。
。
已知:FeS2中的硫元素为-1价。
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②离子方程式配平并补充完整_______ 。
(2)反应③的还原剂是__________________ 。
(3)观察上述反应,硫元素最终转化为____________ 从煤炭中分离出来。
Ⅱ.在淀粉KI溶液中,滴入少量NaClO溶液,溶液立即变蓝,有关反应的离子方程式是____________________________ 。在上述蓝色溶液中,继续滴加足量的NaClO溶液,蓝色逐渐消失,有关反应的离子方程式是_______________________ 。(提示:碘元素被氧化成IO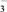 )从以上实验可知,ClO-、I2、IO
)从以上实验可知,ClO-、I2、IO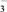 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是________________ 。
Ⅲ.工业上用黄铜矿( CuFeS2)冶炼铜,副产品中有SO2,冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是________ (填元素符号)。当生成0.8 mol 铜时,此反应转移的电子数目是________ 。
①2FeS2+7O2+2H2O
 4H++2Fe2++4SO
4H++2Fe2++4SO ;
;②Fe2++O2+H+
 Fe3++________;
Fe3++________;③FeS2+2Fe3+
 3Fe2++2S;
3Fe2++2S;④2S+3O2+2H2O
 4H++2SO
4H++2SO 。
。已知:FeS2中的硫元素为-1价。
回答下列问题:
(1)根据质量守恒定律和电荷守恒定律,将上述②离子方程式配平并补充完整
(2)反应③的还原剂是
(3)观察上述反应,硫元素最终转化为
Ⅱ.在淀粉KI溶液中,滴入少量NaClO溶液,溶液立即变蓝,有关反应的离子方程式是
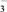 )从以上实验可知,ClO-、I2、IO
)从以上实验可知,ClO-、I2、IO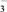 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是Ⅲ.工业上用黄铜矿( CuFeS2)冶炼铜,副产品中有SO2,冶炼铜的反应为8CuFeS2+21O2
 8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是
8Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中 Fe 的化合价为+2 ,反应中被还原的元素是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。
(1)工业上进行海水淡化有多种方法。
①蒸馏法是历史最久,技术和工艺比较成熟的海水淡化方法。下图是海水蒸馏装置示意图,仪器B的名称是_________ 。

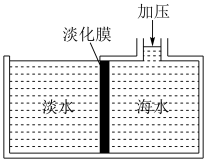
②下图是膜分离技术进行海水淡化的原理示意图。水分子可以透过淡化膜,而海水中其他各种离子不能通过淡化膜。加压后,右侧海水中减少的是_______ (填序号)。
a. 溶质质量 b. 溶液质量 c. 溶剂质量 d. 溶质的物质的量浓度
(2)碘在海水中主要以I-的形式存在,而在地壳中主要以IO3-的形式存在(几种粒子之间的转化关系如下图)。

①海水为原料按方法i制取I2的离子方程式是___________________ 。已知I2可以与Cl2继续反应生成IO3-,由该法制取I2时应注意控制的反应条件是_______ 。
②以方法ii在溶液中制取I2,反应的离子方程式是(已知:反应后所得溶液显酸性)________ 。
③上图iii中反应后溶液中IO3-和Cl-的个数比为1:6,则该反应中氧化剂和还原剂的物质的量之比是__________ 。
(1)工业上进行海水淡化有多种方法。
①蒸馏法是历史最久,技术和工艺比较成熟的海水淡化方法。下图是海水蒸馏装置示意图,仪器B的名称是

②下图是膜分离技术进行海水淡化的原理示意图。水分子可以透过淡化膜,而海水中其他各种离子不能通过淡化膜。加压后,右侧海水中减少的是

a. 溶质质量 b. 溶液质量 c. 溶剂质量 d. 溶质的物质的量浓度
(2)碘在海水中主要以I-的形式存在,而在地壳中主要以IO3-的形式存在(几种粒子之间的转化关系如下图)。

①海水为原料按方法i制取I2的离子方程式是
②以方法ii在溶液中制取I2,反应的离子方程式是(已知:反应后所得溶液显酸性)
③上图iii中反应后溶液中IO3-和Cl-的个数比为1:6,则该反应中氧化剂和还原剂的物质的量之比是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】(1)请配平以下化学方程式:Al+NaNO3+NaOH→NaAlO2+N2↑+H2O___________ 。若反应过程中转移5mole-,则生成标准状况下的N2体积为________ L。
(2)配平CuS2+HNO3→Cu(NO3)2+NO↑+H2SO4+H2O__________ 。
(3)①配平P4+CuSO4+H2O→Cu3P+H3PO4+H2SO4___________ ;
②配平Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O__________ 。
(2)配平CuS2+HNO3→Cu(NO3)2+NO↑+H2SO4+H2O
(3)①配平P4+CuSO4+H2O→Cu3P+H3PO4+H2SO4
②配平Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】(1)水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+4OH-=Fe3O4↓+S4O
+O2+4OH-=Fe3O4↓+S4O +2H2O。
+2H2O。
①参加反应的氧化剂与还原剂的物质的量之比为______ 。
②若有2molFe2+被氧化,则被Fe2+还原的O2的物质的量为______ mol。
③每生成1molFe3O4,反应转移的电子为______ mol。
(2)往含Fe3+、H+、NO 的混合液中加入少量SO
的混合液中加入少量SO ,反应的离子方程式为
,反应的离子方程式为______ 。
(3)向CuSO4溶液中逐滴加入KI溶液至过量,观察到有沉淀(CuI)生成,且溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。写出此过程涉及的离子方程式______ ,______ 。
 +O2+4OH-=Fe3O4↓+S4O
+O2+4OH-=Fe3O4↓+S4O +2H2O。
+2H2O。①参加反应的氧化剂与还原剂的物质的量之比为
②若有2molFe2+被氧化,则被Fe2+还原的O2的物质的量为
③每生成1molFe3O4,反应转移的电子为
(2)往含Fe3+、H+、NO
 的混合液中加入少量SO
的混合液中加入少量SO ,反应的离子方程式为
,反应的离子方程式为(3)向CuSO4溶液中逐滴加入KI溶液至过量,观察到有沉淀(CuI)生成,且溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。写出此过程涉及的离子方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】I.根据硫及化合物相关性质回答以下问题:
(1)将 和
和 的混合气体通入
的混合气体通入 、
、 的混合溶液中反应回收
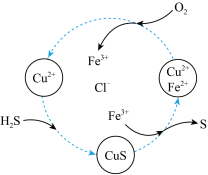
的混合溶液中反应回收 ,物质转化如图所示,下列说法不正确的是___________。
,物质转化如图所示,下列说法不正确的是___________。
(2)过量的锌与一定量㳖 反应,随着硫酸浓度变稀得到的两种气体产物为
反应,随着硫酸浓度变稀得到的两种气体产物为___________ 。使一定质量的Zn与 浓
浓 充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为
充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为___________ g。
Ⅱ.某小组用废铁屑和硝酸盐溶液模拟此过程如下。
(3)先用稀硫酸对废铁屑进行适当浸泡,其目的是___________ (用文字或者方程式表示)。
(4)将 溶液的
溶液的 调至2.5,从氧化还原的角度分析调低溶液pH的原因是
调至2.5,从氧化还原的角度分析调低溶液pH的原因是___________ 。已知:pH越小表示溶液中 越大。
越大。
(5)将上述处理过的足量铁屑投入(4)的溶液中。如图表示该反应过程中,体系内相关离子浓度、pH随时间变化的关系。
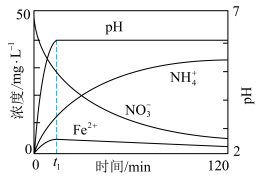
 前该反应的离子方程式是
前该反应的离子方程式是___________ 。
(1)将
 和
和 的混合气体通入
的混合气体通入 、
、 的混合溶液中反应回收
的混合溶液中反应回收 ,物质转化如图所示,下列说法不正确的是___________。
,物质转化如图所示,下列说法不正确的是___________。
A. 和 和 反应的离子方程式为: 反应的离子方程式为: |
B. 在转化过程中发生的反应为: 在转化过程中发生的反应为: |
C.整个反应过程中溶液的pH值变小(不考虑产生的 的稀释效果) 的稀释效果) |
D.提高混合气体中 的比例可防止生成的硫单质中混有 的比例可防止生成的硫单质中混有 |
 反应,随着硫酸浓度变稀得到的两种气体产物为
反应,随着硫酸浓度变稀得到的两种气体产物为 浓
浓 充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为
充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为Ⅱ.某小组用废铁屑和硝酸盐溶液模拟此过程如下。
(3)先用稀硫酸对废铁屑进行适当浸泡,其目的是
(4)将
 溶液的
溶液的 调至2.5,从氧化还原的角度分析调低溶液pH的原因是
调至2.5,从氧化还原的角度分析调低溶液pH的原因是 越大。
越大。(5)将上述处理过的足量铁屑投入(4)的溶液中。如图表示该反应过程中,体系内相关离子浓度、pH随时间变化的关系。

 前该反应的离子方程式是
前该反应的离子方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】19.(每空2分、共10分)下列两组实验中的a、b、c都是必修教材中的常见物质,它们都有如图所示的转化关系(图中的箭头“→”表示在一定条件下,物质的转化可以一步完成),试完成下列表格。

| 序号 | 已知情境 | 化学式 | 对应的离子反应方程式和现象 |
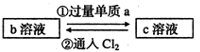 已知B溶液中滴入KSCN溶液后,溶液呈红色 | a | 反应①的离子方程式 反应②的离子方程式 | |
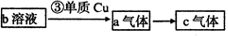 已知b为一种常见的氧化性强酸,其中某非金属元素的最高价为+5 | c | 反应③的现象为 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】氮的化合物在生产生活中有重要广泛运用。
(1)实验室用Cu、稀H2SO4、稀HNO3制备硫酸铜。先在大烧杯中放入铜,加入稀硫酸,再边搅拌边滴加稀硝酸至固体完全溶解,则最恰当的投料比n(H2SO4):n(HNO3)=___ 。
(2)12.8gCu与足量硝酸反应得到NO、NO2、N2O4混合气体4.256L(已折算为标准状况),将混合气体通入含0.2molNaOH的溶液中恰好被完全吸收,则参加反应的HNO3为___ mol。
(3)氨气具有一定还原性,在金属冶炼中因自身不产生污染,常作良好的还原剂,如用NH3热还原CuO的化学方程式为____ 。
(4)肼,又称联氨,化学式为N2H4,其电子式为___ 。联氨是一种二元弱碱,其电离方程式为:N2H4+H2O N2H
N2H +OH-,N2H
+OH-,N2H +H2O
+H2O N2H
N2H +OH-。联氨与硫酸反应生成一种碱式盐的化学式为
+OH-。联氨与硫酸反应生成一种碱式盐的化学式为____ 。
(5)肼—O2燃料电池是一种环境友好电池,介质为20%KOH溶液,其负极反应式为:___ 。
(1)实验室用Cu、稀H2SO4、稀HNO3制备硫酸铜。先在大烧杯中放入铜,加入稀硫酸,再边搅拌边滴加稀硝酸至固体完全溶解,则最恰当的投料比n(H2SO4):n(HNO3)=
(2)12.8gCu与足量硝酸反应得到NO、NO2、N2O4混合气体4.256L(已折算为标准状况),将混合气体通入含0.2molNaOH的溶液中恰好被完全吸收,则参加反应的HNO3为
(3)氨气具有一定还原性,在金属冶炼中因自身不产生污染,常作良好的还原剂,如用NH3热还原CuO的化学方程式为
(4)肼,又称联氨,化学式为N2H4,其电子式为
 N2H
N2H +OH-,N2H
+OH-,N2H +H2O
+H2O N2H
N2H +OH-。联氨与硫酸反应生成一种碱式盐的化学式为
+OH-。联氨与硫酸反应生成一种碱式盐的化学式为(5)肼—O2燃料电池是一种环境友好电池,介质为20%KOH溶液,其负极反应式为:
您最近一年使用:0次



