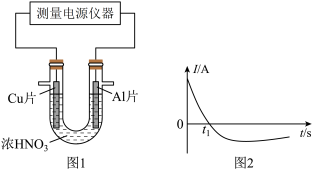
锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选。正极材料的选择决定了锂离子电池的性能。磷酸亚铁锂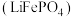 以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
(1)高温固相法是生产磷酸亚铁锂的主要方法。通常以亚铁盐、磷酸盐和锂盐为原料,按化学计量比充分混匀后,在惰性气氛中先经过较低温预分解,再经高温焙烧,最后研磨粉碎制成。请回答下列问题:
①补充完整该反应的化学方程式: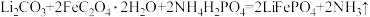
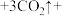
_____ 
______ 。
②理论上,反应中每转移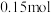 电子,会生成
电子,会生成
_____ g。
③反应需在惰性气氛中进行,其原因是____________ 。
(2)磷酸亚铁锂电池装置如图所示,其中正极材料橄榄石型 通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
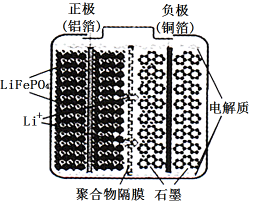
电池工作时的总反应为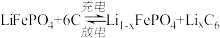 ,则放电时,正极的电极反应式为
,则放电时,正极的电极反应式为________ ,充电时, 迁移方向为
迁移方向为_____ (填“由左向右”或“由右向左”),图中聚合物隔膜应为_____ (填“阳”或“阴”)离子交换膜。
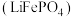 以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。(1)高温固相法是生产磷酸亚铁锂的主要方法。通常以亚铁盐、磷酸盐和锂盐为原料,按化学计量比充分混匀后,在惰性气氛中先经过较低温预分解,再经高温焙烧,最后研磨粉碎制成。请回答下列问题:
①补充完整该反应的化学方程式:
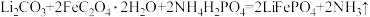
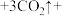

②理论上,反应中每转移
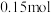 电子,会生成
电子,会生成
③反应需在惰性气氛中进行,其原因是
(2)磷酸亚铁锂电池装置如图所示,其中正极材料橄榄石型
 通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
电池工作时的总反应为
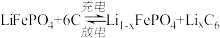 ,则放电时,正极的电极反应式为
,则放电时,正极的电极反应式为 迁移方向为
迁移方向为
18-19高二·全国·课时练习 查看更多[3]
鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第2节 化学能转化为电能——电池山东省青岛通济实验学校学校2021届高三上学期10月月考化学试题(已下线)练习8 原电池 化学电源-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)
更新时间:2020-09-19 17:30:19
|
相似题推荐
填空题
|
较难
(0.4)
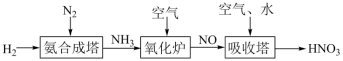
【推荐1】氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题: 的说法中,不正确的是___________(填字母)。
的说法中,不正确的是___________(填字母)。
(2)氨气在氧化炉中发生反应的化学方程式为___________ 。
(3)氮的氧化物(NOx)是常见的大气污染物之一,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。当物质NO与NO2的物质的量之比为1:1时,与足量氨气能在催化剂作用下发生反应,生成两种无污染的物质,该反应的化学方程式为___________ 。
(4)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的污染,可用以下两种方法处理:
①可用ClO2将氮氧化物转化成 。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为
。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为___________ 。
②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为___________ 。
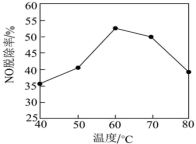
③还有人研究:在不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃ 时,NO 脱除率下降的原因是___________ 。
 的说法中,不正确的是___________(填字母)。
的说法中,不正确的是___________(填字母)。A.工业合成 需要在高温、高压、催化剂下进行 需要在高温、高压、催化剂下进行 |
B. 可用来生产碳铵和尿素等化肥 可用来生产碳铵和尿素等化肥 |
C. 可用浓硫酸或无水氯化钙干燥 可用浓硫酸或无水氯化钙干燥 |
D. 受热易分解,须置于冷暗处保存 受热易分解,须置于冷暗处保存 |
(3)氮的氧化物(NOx)是常见的大气污染物之一,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。当物质NO与NO2的物质的量之比为1:1时,与足量氨气能在催化剂作用下发生反应,生成两种无污染的物质,该反应的化学方程式为
(4)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的污染,可用以下两种方法处理:
①可用ClO2将氮氧化物转化成
 。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为
。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
③还有人研究:在不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃ 时,NO 脱除率下降的原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】根据给定信息书写氧化还原方程式:
(1)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为_____ 。
(2)硫化氢具有还原性,可以和许多氧化剂反应。在酸性条件下,H2S和KMnO4反应生成S、MnSO4、K2SO4和H2O,写出该反应的化学方程式________ 。
(3)在盛有10mL1.0mol·L-1的碘水的试管中,通入足量Cl2完全反应后,共转移了0.1mol电子。写出该反应的化学方程式:________________________ 。
(1)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
(2)硫化氢具有还原性,可以和许多氧化剂反应。在酸性条件下,H2S和KMnO4反应生成S、MnSO4、K2SO4和H2O,写出该反应的化学方程式
(3)在盛有10mL1.0mol·L-1的碘水的试管中,通入足量Cl2完全反应后,共转移了0.1mol电子。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】亚氯酸钠(NaClO2)和ClO2都是重要的漂白剂。
(1)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原NaClO3,可较安全地生成ClO2,反应的离子方程式为_______ 。
(2)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法做如下检测(已知ClO2存在于pH为4~6的溶液中,ClO 存在于中性溶液中):
存在于中性溶液中):
①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:_______ 。
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00 mL。该水样中ClO2的浓度是_______ mg·L-1。
(3)某学习小组设计如下装置制取亚氯酸钠(NaClO2)。
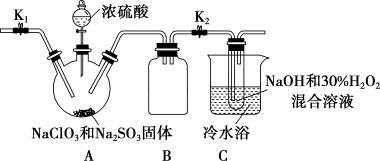
①装置A中产生的ClO2气体,在装置C中反应生成NaClO2,写出生成NaClO2的化学方程式:_______ 。
②将NaClO2溶液在一定条件下处理即可得到NaClO2晶体。装置B的作用是_______ 。
(1)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原NaClO3,可较安全地生成ClO2,反应的离子方程式为
(2)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法做如下检测(已知ClO2存在于pH为4~6的溶液中,ClO
 存在于中性溶液中):
存在于中性溶液中):①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00 mL。该水样中ClO2的浓度是
(3)某学习小组设计如下装置制取亚氯酸钠(NaClO2)。

①装置A中产生的ClO2气体,在装置C中反应生成NaClO2,写出生成NaClO2的化学方程式:
②将NaClO2溶液在一定条件下处理即可得到NaClO2晶体。装置B的作用是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】在T℃时,发生反应C(s)+H2O(g)  CO(g)+H2(g)。
CO(g)+H2(g)。
(1)T℃时,在一个2L的密闭容器中加入4molC和1molH2O(g),5min后反应达到平衡,C的转化率为20%。
①0~5min内,用H2O(g)表示的平均反应速率为____________ 。
②该反应达到平衡的标志是______ 。
A.气体的平均相对分子质量不变
B.气体的密度不变
C.H2O(g)、CO(g)、H2(g)的物质的量之比为1:1: 1
D.气体的总物质的量不变
(2)T℃时,在下列密闭容器中加入相应的物质进行实验,中间的隔板可以自由滑动。
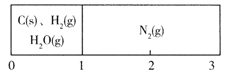
①若左室中气体的平均相对分子质量一直保持不变,则反应开始前H2O(g)、H2(g)的物质的量之比是__________ 。
②反应在达到平衡时,中间的隔板所处的位置是________ 。
A.1~1.5之间 B.1.5处 C.1.5~2之间
(3)已知:I.破坏1mol共价键所需要的能量如下表:
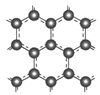
Ⅱ.石墨层由六角形蜂巢结构的碳原子构成,如图所示:
某同学构想:通过下列装置实现C(s)+H2O(g) CO(g)+H2(g)的反应。
CO(g)+H2(g)的反应。
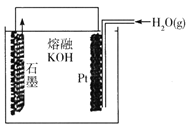
①按该考生的构想,石墨电极发生的反应式为_______________ 。
②这个构想成立吗? 说明理由:_______________ 。
 CO(g)+H2(g)。
CO(g)+H2(g)。(1)T℃时,在一个2L的密闭容器中加入4molC和1molH2O(g),5min后反应达到平衡,C的转化率为20%。
①0~5min内,用H2O(g)表示的平均反应速率为
②该反应达到平衡的标志是
A.气体的平均相对分子质量不变
B.气体的密度不变
C.H2O(g)、CO(g)、H2(g)的物质的量之比为1:1: 1
D.气体的总物质的量不变
(2)T℃时,在下列密闭容器中加入相应的物质进行实验,中间的隔板可以自由滑动。

①若左室中气体的平均相对分子质量一直保持不变,则反应开始前H2O(g)、H2(g)的物质的量之比是
②反应在达到平衡时,中间的隔板所处的位置是
A.1~1.5之间 B.1.5处 C.1.5~2之间
(3)已知:I.破坏1mol共价键所需要的能量如下表:
| 共价键 | 石墨中的碳碳键 | H-H | C≡O | H-O |
| 能量/kJ | 475.7 | 436 | 1072 | 463 |
Ⅱ.石墨层由六角形蜂巢结构的碳原子构成,如图所示:

某同学构想:通过下列装置实现C(s)+H2O(g)
 CO(g)+H2(g)的反应。
CO(g)+H2(g)的反应。
①按该考生的构想,石墨电极发生的反应式为
②这个构想成立吗? 说明理由:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】Li—CuO二次电池的比能量高、工作温度宽,性能优异,广泛应用于军事和空间领域。
(1)Li—CuO电池中,金属锂做_______ 极 。
(2)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣。比较Li、Na、Al分别作为电极时比能量的大小:____________ 。
(3)通过如下过程制备CuO。

①过程Ⅰ,H2O2的作用是__________________ 。
②过程Ⅱ产生Cu2(OH)2CO3的离子方程式是_____________________ 。
③过程Ⅱ,将CuSO4溶液加到Na2CO3溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如下:
已知:Cu2(OH)2CO3中铜元素的百分含量为57.7%。
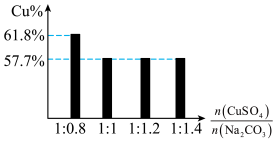
二者比值为1:0.8时,产品中可能含有的杂质是_____________ ,产生该杂质的原因是_________________________________ 。
④ 过程Ⅲ反应的化学方程式是_________________________ 。
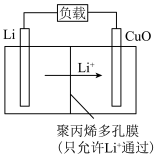
(4)Li—CuO二次电池以含Li+的有机溶液为电解质溶液,其工作原理示意如下。放电时,正极的电极反应式是______________________ 。
(1)Li—CuO电池中,金属锂做
(2)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣。比较Li、Na、Al分别作为电极时比能量的大小:
(3)通过如下过程制备CuO。

①过程Ⅰ,H2O2的作用是
②过程Ⅱ产生Cu2(OH)2CO3的离子方程式是
③过程Ⅱ,将CuSO4溶液加到Na2CO3溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如下:
已知:Cu2(OH)2CO3中铜元素的百分含量为57.7%。

二者比值为1:0.8时,产品中可能含有的杂质是
④ 过程Ⅲ反应的化学方程式是
(4)Li—CuO二次电池以含Li+的有机溶液为电解质溶液,其工作原理示意如下。放电时,正极的电极反应式是

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:
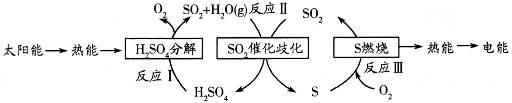
请回答下列问题:
(1)反应I的化学方程式为_____________________________________ 。1mol H2SO4(液)分解成气态物质需要吸收的能量是275.5kJ,硫的燃烧热为297 kJ·mol-1,则反应Ⅱ的热化学方程式为________________________________ 。
(2)单质硫也可以生成多硫化物实现能量间的转化。
①钠硫电池是一种新型高能电池,总反应为2Na+xS Na2Sx,该电池工作时的正极反应式为
Na2Sx,该电池工作时的正极反应式为____________________ ,给该电池充电时,钠电极应与外电源的____________ (填“正”或“负”)极相连接。
②多硫化合物H2S2O8中S的化合价为+6,分子中过氧键的数目为______________________ 。
③在碱性溶液中,多硫离子Sx2-被BrO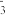 氧化成SO
氧化成SO ,
, 被还原成Br-。该反应的离子方程式是
被还原成Br-。该反应的离子方程式是________________________ 。

请回答下列问题:
(1)反应I的化学方程式为
(2)单质硫也可以生成多硫化物实现能量间的转化。
①钠硫电池是一种新型高能电池,总反应为2Na+xS
 Na2Sx,该电池工作时的正极反应式为
Na2Sx,该电池工作时的正极反应式为②多硫化合物H2S2O8中S的化合价为+6,分子中过氧键的数目为
③在碱性溶液中,多硫离子Sx2-被BrO
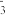 氧化成SO
氧化成SO ,
, 被还原成Br-。该反应的离子方程式是
被还原成Br-。该反应的离子方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)下图是某锌锰干电池的基本构造图。
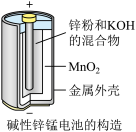
①该干电池的总反应式为2MnO2+Zn+2H2O=2 MnO(OH)+ Zn (OH)2,该电池的负极是___________ , 工作时正极的电极反应式是_______________________ 。
②关于该电池的使用和性能,下列说法正确的是( )
A. 该电池属于蓄电池
B. 电池工作时OH-向负极移动
C. 该电池的电解质溶液是H2SO4溶液
D. 该电池用完后可随意丢弃,不需要回收处理
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为: Cd +2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是 ( )
A .以上反应是可逆反应 B.电池充电时是将化学能转化为电能
C. 电池放电时Cd 做负极 D. 电池放电时正极附近碱性增强
(3)另一种常用的电池锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式表示不能用水溶液的原因________________________________ 。
(4)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一氢氧燃料电池,以电极a为正极,电极b为负极,采用氢氧化钠溶液为电解液,则氧气应通入________ 极(填序号),电解质溶液的pH将_______ (填“变大”,“变小”或“不变”)
(1)下图是某锌锰干电池的基本构造图。

①该干电池的总反应式为2MnO2+Zn+2H2O=2 MnO(OH)+ Zn (OH)2,该电池的负极是
②关于该电池的使用和性能,下列说法正确的是
A. 该电池属于蓄电池
B. 电池工作时OH-向负极移动
C. 该电池的电解质溶液是H2SO4溶液
D. 该电池用完后可随意丢弃,不需要回收处理
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为: Cd +2NiO(OH)+2H2O
 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是 A .以上反应是可逆反应 B.电池充电时是将化学能转化为电能
C. 电池放电时Cd 做负极 D. 电池放电时正极附近碱性增强
(3)另一种常用的电池锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式表示不能用水溶液的原因
(4)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一氢氧燃料电池,以电极a为正极,电极b为负极,采用氢氧化钠溶液为电解液,则氧气应通入
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】(1)海水中有丰富的食盐资源,工业上以粗食盐水(含少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3流程如图,请回答:
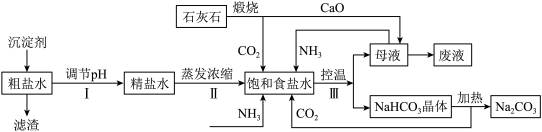
①粗盐精制过程中加入的沉淀剂是石灰乳和纯碱,应先加__ 。
②上述流程中循环使用的物质有__ 。
③图中制得的饱和食盐水还可用于氯碱工业,NaCl溶液的电解产物可用于生产盐酸、漂白粉、氢氧化钠等产品。工业上电解饱和食盐水的离子方程式为__ 。
④氨气可用电解法合成,其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如下图1和图2所示。图1中,a电极上通入的X为__ ,图2中,d电极上的电极反应式为___ 。
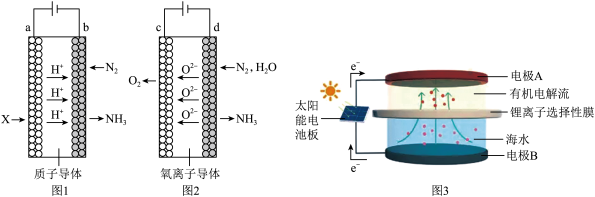
(2)我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图3所示:
①金属锂在电极__ (填“A”或“B”)上生成。
②阳极能产生两种气体单质,电极反应式是2Cl--2e-=Cl2↑和__ 。
③某种锂离子二次电池的总反应为:FePO4(s)+Li(s) LiFePO4(s),装置如图所示(a极材料为金属锂和石墨的复合材料)。
LiFePO4(s),装置如图所示(a极材料为金属锂和石墨的复合材料)。
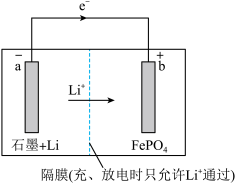
下列说法错误的有___ 。
A.图中e-及Li+移动方向说明该电池处于放电状态
B.该电池可选择含Li+的水溶液做离子导体
C.充电时a极连接外接电源的正极
D.充电时,b极电极反应式为:LiFePO4-e-=Li++FePO4

①粗盐精制过程中加入的沉淀剂是石灰乳和纯碱,应先加
②上述流程中循环使用的物质有
③图中制得的饱和食盐水还可用于氯碱工业,NaCl溶液的电解产物可用于生产盐酸、漂白粉、氢氧化钠等产品。工业上电解饱和食盐水的离子方程式为
④氨气可用电解法合成,其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如下图1和图2所示。图1中,a电极上通入的X为

(2)我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图3所示:
①金属锂在电极
②阳极能产生两种气体单质,电极反应式是2Cl--2e-=Cl2↑和
③某种锂离子二次电池的总反应为:FePO4(s)+Li(s)
 LiFePO4(s),装置如图所示(a极材料为金属锂和石墨的复合材料)。
LiFePO4(s),装置如图所示(a极材料为金属锂和石墨的复合材料)。
下列说法错误的有
A.图中e-及Li+移动方向说明该电池处于放电状态
B.该电池可选择含Li+的水溶液做离子导体
C.充电时a极连接外接电源的正极
D.充电时,b极电极反应式为:LiFePO4-e-=Li++FePO4
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:_____ 。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于对器皿实现化学镀银。
①H3PO2中,P元素的化合价为____ 。
②利用H3PO2进行化学镀银反应中,氧化产物为H3PO4,则氧化剂与还原剂的物质的量之比为____ 。
③NaH2PO2为____ (填“正盐”或“酸式盐”)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应即可制得H3PO2。写出白磷与Ba(OH)2溶液反应的化学方程式:____ 。反应中生成0.1mol Ba(H3PO2)2,转移电子数___ (以NA代表阿伏加 德罗常数的数值)。
(1)H3PO2是一元中强酸,写出其电离方程式:
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于对器皿实现化学镀银。
①H3PO2中,P元素的化合价为
②利用H3PO2进行化学镀银反应中,氧化产物为H3PO4,则氧化剂与还原剂的物质的量之比为
③NaH2PO2为
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应即可制得H3PO2。写出白磷与Ba(OH)2溶液反应的化学方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+4OH-=Fe3O4↓+S4O
+O2+4OH-=Fe3O4↓+S4O +2H2O。
+2H2O。
①参加反应的氧化剂与还原剂的物质的量之比为______ 。
②若有2molFe2+被氧化,则被Fe2+还原的O2的物质的量为______ mol。
③每生成1molFe3O4,反应转移的电子为______ mol。
(2)往含Fe3+、H+、NO 的混合液中加入少量SO
的混合液中加入少量SO ,反应的离子方程式为
,反应的离子方程式为______ 。
(3)向CuSO4溶液中逐滴加入KI溶液至过量,观察到有沉淀(CuI)生成,且溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。写出此过程涉及的离子方程式______ ,______ 。
 +O2+4OH-=Fe3O4↓+S4O
+O2+4OH-=Fe3O4↓+S4O +2H2O。
+2H2O。①参加反应的氧化剂与还原剂的物质的量之比为
②若有2molFe2+被氧化,则被Fe2+还原的O2的物质的量为
③每生成1molFe3O4,反应转移的电子为
(2)往含Fe3+、H+、NO
 的混合液中加入少量SO
的混合液中加入少量SO ,反应的离子方程式为
,反应的离子方程式为(3)向CuSO4溶液中逐滴加入KI溶液至过量,观察到有沉淀(CuI)生成,且溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。写出此过程涉及的离子方程式
您最近一年使用:0次
【推荐3】在一定条件下,Pb(N3)2(名称叠氮化铅,其中Pb为+2价,N平均为- 价)与Cr(MnO4)2能发生以下反应:4Cr(MnO4)2+6Pb(N3)2=2Pb3O4+17N2+2NO+8MnO2+2Cr2O3
价)与Cr(MnO4)2能发生以下反应:4Cr(MnO4)2+6Pb(N3)2=2Pb3O4+17N2+2NO+8MnO2+2Cr2O3
根据你学过的有关化学知识,回答下列问题:
(1)过渡元素多有可变化合价,如Cr常见化合价为+2、+3、+6,Mn的常见化合价为+2、+4、+6、+7,则在化合物Cr(MnO4)2中Cr的化合价为___________ ,Mn的化合价为___________ 。依据某种分类标准,在产物中N2与其它四种物质种类不同,该分类标准是___________ 。
(2)Pb(N3)2在该反应中做___________ 剂,该反应的还原产物是___________ (写物质化学式),当1 mol Cr(MnO4)2参加反应,反应中转移电子数是___________ (用NA表示阿伏加德罗常数)。
 价)与Cr(MnO4)2能发生以下反应:4Cr(MnO4)2+6Pb(N3)2=2Pb3O4+17N2+2NO+8MnO2+2Cr2O3
价)与Cr(MnO4)2能发生以下反应:4Cr(MnO4)2+6Pb(N3)2=2Pb3O4+17N2+2NO+8MnO2+2Cr2O3根据你学过的有关化学知识,回答下列问题:
(1)过渡元素多有可变化合价,如Cr常见化合价为+2、+3、+6,Mn的常见化合价为+2、+4、+6、+7,则在化合物Cr(MnO4)2中Cr的化合价为
(2)Pb(N3)2在该反应中做
您最近一年使用:0次