(1)请配平以下化学方程式:Al+NaNO3+NaOH→NaAlO2+N2↑+H2O___________ 。若反应过程中转移5mole-,则生成标准状况下的N2体积为________ L。
(2)配平CuS2+HNO3→Cu(NO3)2+NO↑+H2SO4+H2O__________ 。
(3)①配平P4+CuSO4+H2O→Cu3P+H3PO4+H2SO4___________ ;
②配平Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O__________ 。
(2)配平CuS2+HNO3→Cu(NO3)2+NO↑+H2SO4+H2O
(3)①配平P4+CuSO4+H2O→Cu3P+H3PO4+H2SO4
②配平Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O
更新时间:2020-12-15 11:29:26
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】铁及其化合物在日常生活、生产中应用广泛。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。按要求回答下列问题:
高铁酸钠主要通过如下反应制取:2Fe(OH)3 + 3NaClO + 4NaOH =2Na2FeO4 + 3X + 5H2O, 则X的化学式_______ ,反应中_______ 被氧化。
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如图:

①酸溶过程中Fe2O3与稀硫酸反应的化学方程式为_______ ;
“滤渣A”主要成分的化学式为_______ 。
②还原过程中加入FeS2的目的是将溶液中的Fe3 +还原为Fe2 +,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2 + 14Fe3 + +_______H2O =15Fe2 + + _______SO +_______。
+_______。
_______
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为_______ 。
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8,如果pH过大,可能引起的后果是_______ (几种离子沉淀的pH见表);滤液B可以回收的物质有(写化学式)_______ 。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。按要求回答下列问题:
高铁酸钠主要通过如下反应制取:2Fe(OH)3 + 3NaClO + 4NaOH =2Na2FeO4 + 3X + 5H2O, 则X的化学式
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如图:

①酸溶过程中Fe2O3与稀硫酸反应的化学方程式为
“滤渣A”主要成分的化学式为
②还原过程中加入FeS2的目的是将溶液中的Fe3 +还原为Fe2 +,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2 + 14Fe3 + +_______H2O =15Fe2 + + _______SO
 +_______。
+_______。③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.2 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】根据题目填写内容
(1)下列物质:①纯H2SO4②硝酸钾溶液③铜④二氧化碳⑤Ba(OH)2固体⑥KHSO4固体⑦蔗糖⑧熔融KCl⑨氨水
能导电的是___________ (填序号,下同),属于电解质的是___________ ,属于非电解质的是_______ 。
检验②中金属阳离子的实验方法是______________________________ (填实验操作的名称)。
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是_____________ 。
Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的方法是_____________ 。
(3)酸性条件下,高锰酸钾可与草酸(H2C2O4)溶液发生反应,其反应如下,补上产物,配平化学方程式,并用单线桥法标出电子转移的方向和数目_____________ 。
____KMnO4+____H2C2O4+____H2SO4→____K2SO4+____MnSO4+____CO2+________
(4)①0.5mol C2H6O的质量是____ 克,含____ 个C2H6O分子,含____ mol氢原子,与____ g H2O分子中的氢的原子数目相同。
②在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,若其中CO和N2的物质的量之比为1:1,则混合气体中氧元素的质量分数为____ 。
③有K2SO4和Al2(SO)3的混合溶液,已知其中Al3+的物质的量浓度为0.4 mol·L-1, 的物质的量浓度为0.7 mol·L-1,,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.7 mol·L-1,,则此溶液中K+的物质的量浓度为____ 。
(1)下列物质:①纯H2SO4②硝酸钾溶液③铜④二氧化碳⑤Ba(OH)2固体⑥KHSO4固体⑦蔗糖⑧熔融KCl⑨氨水
能导电的是
检验②中金属阳离子的实验方法是
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是
Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的方法是
(3)酸性条件下,高锰酸钾可与草酸(H2C2O4)溶液发生反应,其反应如下,补上产物,配平化学方程式,并用单线桥法标出电子转移的方向和数目
____KMnO4+____H2C2O4+____H2SO4→____K2SO4+____MnSO4+____CO2+________
(4)①0.5mol C2H6O的质量是
②在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,若其中CO和N2的物质的量之比为1:1,则混合气体中氧元素的质量分数为
③有K2SO4和Al2(SO)3的混合溶液,已知其中Al3+的物质的量浓度为0.4 mol·L-1,
 的物质的量浓度为0.7 mol·L-1,,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.7 mol·L-1,,则此溶液中K+的物质的量浓度为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】亚硝酰氯(NOCl)是有机药物制备的重要试剂,可按以下流程合成和利用。
请回答:
(1)NOCl的电子式为_______ ,化合物X的结构简式为_______ 。
(2)下列说法正确的是_______。
(3)已知浓盐酸和浓硝酸混合配制王水时也会产生亚硝酰氯,写出该反应的化学方程式_______ 。
(4)设计实验验证化合物X中含有Cl元素_______ ;写出实验过程中涉及的反应方程式_______ 。
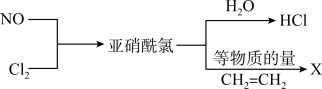
请回答:
(1)NOCl的电子式为
(2)下列说法正确的是_______。
| A.NOCl中的氮元素呈正价 |
| B.NOCl分子的空间结构为V形 |
C.化合物X的沸点低于氯乙酰胺( ) ) |
| D.工业上可以用蒸馏水吸收多余的NOCl,防止污染环境 |
(3)已知浓盐酸和浓硝酸混合配制王水时也会产生亚硝酰氯,写出该反应的化学方程式
(4)设计实验验证化合物X中含有Cl元素
您最近一年使用:0次
【推荐1】二氧化氯( )是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:
)是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:
(1)将二氧化氯通入品红溶液中,溶液褪色的原因是_______ 。
(2)配平下列反应的化学方程式:_______ 。
_______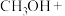 _______
_______ _______= CO2↑_______
_______= CO2↑_______ _______
_______ _______
_______
(3)上述反应中,被氧化的元素是_______ 。还原产物与氧化产物的物质的量之比是_______ 。
(4)根据上述反应可推知_______ (填字母)。
a.氧化性: b.氧化性:
b.氧化性: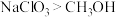
c.还原性: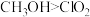 d.还原性:
d.还原性:
(5)若转移的电子数目为 (
( 为阿伏加德罗常数的值)则反应产生气体的体积约为
为阿伏加德罗常数的值)则反应产生气体的体积约为_______ L(标准状况)。
 )是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:
)是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:(1)将二氧化氯通入品红溶液中,溶液褪色的原因是
(2)配平下列反应的化学方程式:
_______
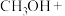 _______
_______ _______= CO2↑_______
_______= CO2↑_______ _______
_______ _______
_______(3)上述反应中,被氧化的元素是
(4)根据上述反应可推知
a.氧化性:
 b.氧化性:
b.氧化性: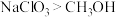
c.还原性:
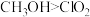 d.还原性:
d.还原性:
(5)若转移的电子数目为
 (
( 为阿伏加德罗常数的值)则反应产生气体的体积约为
为阿伏加德罗常数的值)则反应产生气体的体积约为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将化学方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O(未配平,不考虑2NO2 N2O4)
N2O4)
完成下列填空:
(1)硝酸在该反应中的作用是_________ ,该反应的还原产物是_______ 。
(2)0.3molCu被硝酸完全溶解后,Cu失去的电子数是____ 个,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______ ,若用排水法收集这些气体,可得标准状况下的气体______ L。
(3)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出该反应的离子方程式________ 。
(4)如果没有对该反应中的某些物质的比例作限定,则化学方程式可能的配平系数有许多组。原因是_______________________ 。
 N2O4)
N2O4)完成下列填空:
(1)硝酸在该反应中的作用是
(2)0.3molCu被硝酸完全溶解后,Cu失去的电子数是
(3)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出该反应的离子方程式
(4)如果没有对该反应中的某些物质的比例作限定,则化学方程式可能的配平系数有许多组。原因是
您最近一年使用:0次

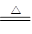 2KCl+2MnCl2+5Cl2↑+8H2O。
2KCl+2MnCl2+5Cl2↑+8H2O。

