(1)下列原子或离子的电子排布的表示方法中,正确的是___ ,违反了能量最低原理的是___ ,违反洪特规则的是__ 。
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C: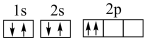
绿柱石被国际珠宝界公认为四大名贵宝石之一。主要成分为Be3Al2[Si6O18],因含适量的Cr2O3(0.15~0.6%),而形成祖母绿。试回答下列问题:
(2)基态Al原子中,电子填充的最高能级是___ ,基态Cr原子的价电子排布式是___ 。
(3)用“>”或“<”填空:
(4)卟啉与Fe2+合即可形成血红素,Fe2+的电子排布式为___ ,铁在周期表中的位置为__ 。
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:

④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C:

绿柱石被国际珠宝界公认为四大名贵宝石之一。主要成分为Be3Al2[Si6O18],因含适量的Cr2O3(0.15~0.6%),而形成祖母绿。试回答下列问题:
(2)基态Al原子中,电子填充的最高能级是
(3)用“>”或“<”填空:
| 第一电离能 | 沸点 | 离子半径 |
| Be | H2S | Al3+ |
(4)卟啉与Fe2+合即可形成血红素,Fe2+的电子排布式为
更新时间:2019-12-24 13:02:05
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】用“>”“<”表示下列各组能级的能量高低。
(1)2s__ 4s;(2)2p__ 4p;(3)4s__ 3d
(1)2s
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】金属钛密度小、强度高、抗腐蚀性能好,是应用广泛的金属。含钛的矿石主要有金红石和钛铁矿。
(1)基态Ti原子的价层电子排布式为___________ ,含有未成对电子___________ 个,Ti元素在周期表中的位置是___________ 。
(2)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知 Ti3+的配位数为 6,TiCl3·4H2O 的化学式用配合物的形式表示为___________ 。
(1)基态Ti原子的价层电子排布式为
(2)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知 Ti3+的配位数为 6,TiCl3·4H2O 的化学式用配合物的形式表示为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】有几种元素的粒子核外电子排布式均为1s22s22p63s23p6,其中:
(1)某电中性微粒一般不和其他元素的原子反应,这种微粒的符号是___________ ;
(2)某微粒的盐溶液,能使溴水褪色,并出现浑浊,这种微粒的符号是___________ ;
(3)某微粒氧化性很弱,但得到电子后还原性很强,且这种原子有一个单电子,这种微粒的符号是___________ ;
(4)某微粒还原性虽弱,但失去电子后氧化性强,且这种元素的原子得到一个电子即达稳定结构,这种微粒的符号是___________ 。
(1)某电中性微粒一般不和其他元素的原子反应,这种微粒的符号是
(2)某微粒的盐溶液,能使溴水褪色,并出现浑浊,这种微粒的符号是
(3)某微粒氧化性很弱,但得到电子后还原性很强,且这种原子有一个单电子,这种微粒的符号是
(4)某微粒还原性虽弱,但失去电子后氧化性强,且这种元素的原子得到一个电子即达稳定结构,这种微粒的符号是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式__ 。
(2)根据元素周期律,原子半径Ga__ As,第一电离能Ga__ As。(填“大于”或“小于”)。
(1)写出基态As原子的核外电子排布式
(2)根据元素周期律,原子半径Ga
您最近一年使用:0次
【推荐1】我国科学家成功合成了世界上首个全氮阴离子盐,使氮原子簇化合物的研究有了新的突破。
(1)基态N原子中有___________ 个未成对电子,电子占据的最高能级的符号是___________ 。
(2)第二周期元素原子的第一电离能介于B、N之间的是___________ (填元素符号)。
(3)以氮化镓(GaN)等为代表的第三代半导体材料具有优异性能,基态 价层电子的轨道表示式
价层电子的轨道表示式___________ 。
(1)基态N原子中有
(2)第二周期元素原子的第一电离能介于B、N之间的是
(3)以氮化镓(GaN)等为代表的第三代半导体材料具有优异性能,基态
 价层电子的轨道表示式
价层电子的轨道表示式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】不同元素的气态原子失去最外层一个电子所需要的最低能量,设其为E,如图所示。试根据元素在周期表中的位置,分析图中曲线的变化特点,并完成下列问题。

(1)写出14号元素基态原子的电子排布式___________ 。
(2)用所学理论解释13号元素的E值比12号元素低的原因___________ 。
(3)同一周期内,随着原子序数的增大,E值增大,但个别元素的E值出现反常现象。试预测下列关系式中正确的是___________ (填序号)。
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)
(4)估计1mol气态钙原子失去最外层一个电子所需最低能量E值的范围___________ 。
(5)从原子结构的角度解释19号元素的E值比11号元素E值低的原因___________ 。

(1)写出14号元素基态原子的电子排布式
(2)用所学理论解释13号元素的E值比12号元素低的原因
(3)同一周期内,随着原子序数的增大,E值增大,但个别元素的E值出现反常现象。试预测下列关系式中正确的是
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)
(4)估计1mol气态钙原子失去最外层一个电子所需最低能量E值的范围
(5)从原子结构的角度解释19号元素的E值比11号元素E值低的原因
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)________ I1(Cu)(填“大于”或“小于”)。原因是_______________________ 。
(2)氮原子价层电子的轨道表达式(电子排布图)为_________ 。
(3)基态Ge原子的核外电子排布式为[Ar]__________ ,有________ 个未成对电子。
(4)镍元素基态原子的电子排布式为_________________ ,3d能级上的未成对电子数为________ 。
(2)氮原子价层电子的轨道表达式(电子排布图)为
(3)基态Ge原子的核外电子排布式为[Ar]
(4)镍元素基态原子的电子排布式为
您最近一年使用:0次



