常温下,几种物质的溶度积常数见下表:
(1)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净CuCl2溶液,宜先加入_______ (填试剂分子式),然后调至溶液pH=4,使Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=________________ 。
(2)在有CuCl与CuI固体共存的悬浊液中,C(Cl-)______ C(I-)(填 > < =)
某溶液中C(Cl-)为0.0001 mol·L-1, C(I-)为0.1 mol·L-1,往溶液中滴加硝酸亚铜,先产生的沉淀是__________ (填沉淀化学式)
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 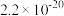 | 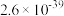 | 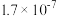 | 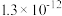 |
(1)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净CuCl2溶液,宜先加入
(2)在有CuCl与CuI固体共存的悬浊液中,C(Cl-)
某溶液中C(Cl-)为0.0001 mol·L-1, C(I-)为0.1 mol·L-1,往溶液中滴加硝酸亚铜,先产生的沉淀是
19-20高二上·广西北海·期中 查看更多[2]
更新时间:2019-12-28 17:57:48
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在“观察·思考”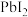 固体的沉淀溶解平衡实验中,哪些现象能证明
固体的沉淀溶解平衡实验中,哪些现象能证明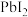 溶液中存在沉淀溶解平衡
溶液中存在沉淀溶解平衡______ ?
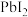 固体的沉淀溶解平衡实验中,哪些现象能证明
固体的沉淀溶解平衡实验中,哪些现象能证明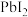 溶液中存在沉淀溶解平衡
溶液中存在沉淀溶解平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol•L-1)如图所示。
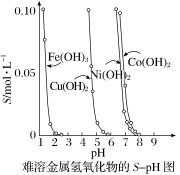
(1)pH=3时溶液中铜元素的主要存在形式是________ 。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为_______ (填字母)。
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含有少量的Co2+杂质,________ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是_________ 。

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含有少量的Co2+杂质,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铵盐是实验室常用试剂。回答下列问题:
(1)NH4Cl溶液中 水解的离子方程式为
水解的离子方程式为_____ ;加入镁粉可产生大量气体,该气体的成分是______ (写化学式)。
(2)物质的量浓度相同的下列四种铵盐的溶液中,c( )从大到小的顺序为
)从大到小的顺序为______ (用标号表示)。
A.(NH4)2CO3 B.CH3COONH4 C.NH4HSO4 D.NH4Cl
(3)少量Mg(OH)2能溶于CH3COONH4浓溶液(呈中性)的原因是______ (用文字和方程式说明)。
(4)甲醛法测定铵盐中氮的质量分数的实验步骤如下:步骤I.称取a g (NH4)2SO4样品,用水溶解后定容于250 mL容量瓶中;步骤II.取出25.00 mL溶液于锥形瓶中,加入足量中性甲醛溶液[4 +6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。
+6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。
①滴定到终点时,溶液颜色的变化是__________ 。
②该(NH4)2SO4样品中氮的质量分数为______ (用含a、c、V的代数式表示)。
③推测下列铵盐中不能用该法测定其中氮的质量分数的是______ (填标号)。
A.NH4Cl B.NH4HCO3 C.NH4NO3 D.CH3COONH4
(1)NH4Cl溶液中
 水解的离子方程式为
水解的离子方程式为(2)物质的量浓度相同的下列四种铵盐的溶液中,c(
 )从大到小的顺序为
)从大到小的顺序为A.(NH4)2CO3 B.CH3COONH4 C.NH4HSO4 D.NH4Cl
(3)少量Mg(OH)2能溶于CH3COONH4浓溶液(呈中性)的原因是
(4)甲醛法测定铵盐中氮的质量分数的实验步骤如下:步骤I.称取a g (NH4)2SO4样品,用水溶解后定容于250 mL容量瓶中;步骤II.取出25.00 mL溶液于锥形瓶中,加入足量中性甲醛溶液[4
 +6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。
+6HCHO=3H++6H2O+(CH2)6N4H+],再加入酚酞指示剂,用c mol·L-1 NaOH标准溶液滴定[3H++(CH2)6N4H++4OH-=(CH2)6N4+4H2O],滴定到终点时消耗标准溶液V mL。①滴定到终点时,溶液颜色的变化是
②该(NH4)2SO4样品中氮的质量分数为
③推测下列铵盐中不能用该法测定其中氮的质量分数的是
A.NH4Cl B.NH4HCO3 C.NH4NO3 D.CH3COONH4
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、
②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1 硝酸银溶液中,
其中Ag+浓度最小的是____________ 。(填序号)
(2)电解氯化钠可以得到多种化工原料。用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO 等杂质。某次除杂操作时,往粗盐水中先加入过量的BaCl2溶液,至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO
等杂质。某次除杂操作时,往粗盐水中先加入过量的BaCl2溶液,至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO ,其原因是
,其原因是______________________________ [已知:Ksp(BaSO4)=1.1×10-10、Ksp(BaCO3)=2.6×10-9]。
②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1 硝酸银溶液中,
其中Ag+浓度最小的是
(2)电解氯化钠可以得到多种化工原料。用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO
 等杂质。某次除杂操作时,往粗盐水中先加入过量的BaCl2溶液,至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO
等杂质。某次除杂操作时,往粗盐水中先加入过量的BaCl2溶液,至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO ,其原因是
,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知:Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10-39,pH=7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10-6 mol·L-1),需调节溶液pH范围为___________ 。
您最近一年使用:0次

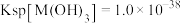 ,要使溶液中的
,要使溶液中的 降至
降至 ,则应调节溶液
,则应调节溶液


