如图是金属镁和卤素单质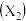 反应的能量变化示意图。下列说法不正确的是
反应的能量变化示意图。下列说法不正确的是
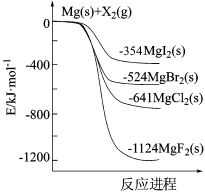
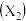 反应的能量变化示意图。下列说法不正确的是
反应的能量变化示意图。下列说法不正确的是

A.由 制取Mg是吸热过程 制取Mg是吸热过程 |
B.热稳定性: |
C.常温下还原性: |
D.由图知此温度下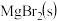 与 与 反应的热化学方程式为: 反应的热化学方程式为: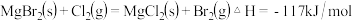 |
2019高三·全国·专题练习 查看更多[3]
(已下线)第1章 化学反应的热效应(能力提升卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)(已下线)小题必刷23 焓变与热化学方程式——2021年高考化学一轮复习小题必刷(通用版)2019年秋高三化学复习强化练习—— 盖斯定律及应用
更新时间:2019-12-28 19:19:18
|
相似题推荐
单选题
|
较难
(0.4)
真题
解题方法
【推荐1】相同温度和压强下,关于反应的 ,下列判断正确的是
,下列判断正确的是

 ,下列判断正确的是
,下列判断正确的是
A. | B. |
C.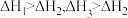 | D.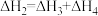 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】以CO和 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将 转化为甲醇。
转化为甲醇。
已知:①
 kJ·mol
kJ·mol
②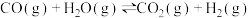
 kJ·mol
kJ·mol
③
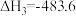 kJ·mol
kJ·mol
下列说法不正确 的是
 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将 转化为甲醇。
转化为甲醇。已知:①

 kJ·mol
kJ·mol
②
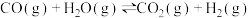
 kJ·mol
kJ·mol
③

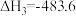 kJ·mol
kJ·mol
下列说法
A.若温度不变,反应①中生成1 mol  时,放出的热量大于90.5 kJ 时,放出的热量大于90.5 kJ |
B. 与 与 合成甲醇的热化学方程式为: 合成甲醇的热化学方程式为:  kJ·mol kJ·mol |
C.通过电解制 和选用高效催化剂,可降低 和选用高效催化剂,可降低 与 与 合成甲醇反应的焓变 合成甲醇反应的焓变 |
D.以 和 和 为原料合成甲醇,同时生成 为原料合成甲醇,同时生成 ,该反应需要吸收能量 ,该反应需要吸收能量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列关于化学反应速率和化学平衡的说法正确的是
| A.化学平衡常数K变化,平衡不一定发生移动 |
B.已知反应: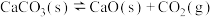 ,在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时 ,在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时 (g)的浓度将升高 (g)的浓度将升高 |
C.两个体积相同的容器中充入等量的 发生反应: 发生反应: △H<0,绝热容器中气体的颜色比铁制容器中颜色深 △H<0,绝热容器中气体的颜色比铁制容器中颜色深 |
| D.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】丙烯与HBr发生加成反应的机理及反应体系中的能量变化如图所示。下列说法不正确的是
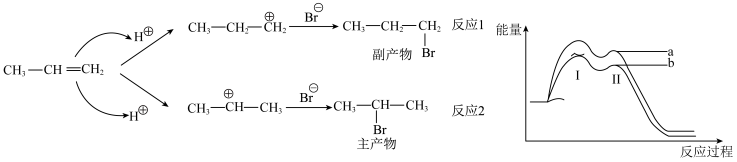

| A.曲线a表示反应2的能量变化 | B.反应1和反应2都是放热反应 |
| C.反应1和反应2的决速步骤都是第1步 | D.相同条件下反应2的速率比反应1大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在25 ℃、1.01×105 Pa下,将22 g CO2通入750 mL 1mol/LNaOH溶液中充分反应,测得反应放出x kJ热量。在该条件下,1 mol CO2通入1mol/L NaOH溶液2 L中充分反应放出y kJ热量。则CO2与NaOH溶液反应生成NaHCO3的热化学方程式是
| A.CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-(2y-x) kJ·mol−1 |
| B.CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-(2x-y) kJ·mol−1 |
| C.CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-(4x-y) kJ·mol−1 |
| D.2CO2(g)+NaOH(l)=NaHCO3(l) ΔH=-(8x-2y) kJ·mol−1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在298 K、1.01×105 Pa,将22 g CO2通入0.75 L 1.0 mol·L-1NaOH溶液中充分反应,测得反应放出的热量为a kJ。已知该条件下1 mol CO2通入1 L 2.0 mol·L-1NaOH溶液中充分反应放出的热量为b kJ。则CO2与NaOH反应生成NaHCO3的热化学方程式为( )。
A.CO2(g)+NaOH(aq) NaHCO3(aq) ΔH=-(2b-a) kJ·mol-1 NaHCO3(aq) ΔH=-(2b-a) kJ·mol-1 |
B.CO2(g)+NaOH(aq) NaHCO3(aq) ΔH=+(4a-b) kJ·mol-1 NaHCO3(aq) ΔH=+(4a-b) kJ·mol-1 |
C.CO2(g)+NaOH(aq) NaHCO3(aq) ΔH=-(4a-b) kJ·mol-1 NaHCO3(aq) ΔH=-(4a-b) kJ·mol-1 |
D.CO2(g)+NaOH(aq) NaHCO3(aq) ΔH=+(2b-a) kJ·mol-1 NaHCO3(aq) ΔH=+(2b-a) kJ·mol-1 |
您最近一年使用:0次









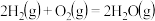 ;
; 则
则 表示CO和
表示CO和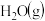 生成
生成 和
和 的能量变化
的能量变化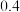
 HB溶液和
HB溶液和
 溶液等体积混合后溶液的
溶液等体积混合后溶液的 ,则混合溶液中离子浓度的大小顺序为:
,则混合溶液中离子浓度的大小顺序为:
 和
和 从
从 到
到 的转化率逐减小,且HX的还原性逐渐减弱
的转化率逐减小,且HX的还原性逐渐减弱 中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中, 的变化情况
的变化情况


