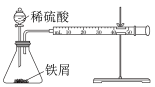
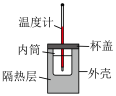
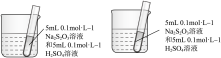
下列实验操作正确的是
A.测定中和热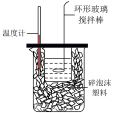 |
B.验证温度对化学平衡的影响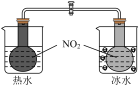 |
C.配制酸碱中和滴定的标准液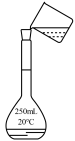 |
D.组装铜锌原电池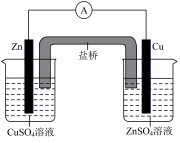 |
更新时间:2019-12-24 08:51:06
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作或实验设计正确的是
| A | B | C | D |
 |  |  手不会画,也找不到相似的 手不会画,也找不到相似的 |  |
| 探究铁钉的电化学腐蚀类型 | 中和反应热的测定 | 提纯乙酸乙酯 | 干燥HI气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作会导致实验结果偏高的是
| A.用NaOH标准液测定未知浓度的盐酸时,滴定后滴定管尖嘴出现气泡 |
| B.测定中和热实验中,两只烧杯口不相平 |
| C.测定硫酸铜晶体结晶水含量的实验中,加热分解后的样品置于空气中自然冷却 |
| D.配制0.1 mol·L-1 NaCl溶液时,定容时俯视刻度线 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】对于反应2SiHCl3(g) SiH2Cl2(g) + SiCl4(g) ,采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g) + SiCl4(g) ,采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。

下列说法正确的是
 SiH2Cl2(g) + SiCl4(g) ,采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g) + SiCl4(g) ,采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。
下列说法正确的是
| A.343K时SiHCl3的平衡常数约为0.02 |
| B.323K时反应的平衡转化率α=22% |
| C.在343K时,要提高SiHCl3转化率,可采取的措施是及时移去产物或者提高反应物浓度 |
| D.比较a、b 处反应速率大小:va小于vb |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验操作能达到实验目的的是
| 选项 | 操作 | 目的 |
| A | 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取NaClO溶液滴于试纸的中部,与标准比色卡对比 | 测定NaClO溶液的pH |
| B | 向含有酚酞的Na2CO3溶液中滴入BaCl2溶液至过量,观察溶液颜色的变化 | 证明Na2CO3溶液中存在碳酸根的水解平衡 |
| C | 取两支试管,各加入5 mL淀粉溶液、2滴碘水和1 mL 2 mol·L-1的稀硫酸,迅速将一支置于85℃的水浴中,另一支在室温下反应,观察蓝色褪色的时间 | 研究温度对反应速率的影响 |
| D | 在醋酸铅稀溶液中通入硫化氢气体,观察现象 | 判断H2S与CH3COOH酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法正确的是
| A.食醋总酸含量测定时若没有控制好滴定终点,溶液显深红色,则必须重做实验 |
| B.配制一定物质的量浓度的稀硫酸时,用移液管量取浓硫酸可以提高实验精度 |
| C.探究温度对硫代硫酸钠与酸反应速率的影响时,应先将两种溶液混合后,再用水浴加热至设定温度 |
| D.在两支试管中分别加1mL无水乙醇和1.5g苯酚固体,再加等量等体积的钠,比较乙醇、苯酚羟基上氢原子的活泼性 |
您最近一年使用:0次
单选题
|
适中
(0.64)
【推荐1】某学生配制了100mL 2mol/L的NaCI溶液,然后对溶液浓度做精确测定,且测定过程中一切操作都正确。结果测得溶液的物质的量浓度低于2mol/L。那么在配制过程中,下列操作可能导致溶液浓度偏低的是
①托盘天平称量过程中NaCI固体和砝码放反了
②将NaCl在烧杯中稀释,转移到容积为lOOmL的容量瓶中后,没有洗涤烧杯
③在定容时观察液面俯视
④最后定容时,加水超过了刻度,马上用胶头滴管吸去多余的水,使溶液凹液面刚好与刻度线相切
①托盘天平称量过程中NaCI固体和砝码放反了
②将NaCl在烧杯中稀释,转移到容积为lOOmL的容量瓶中后,没有洗涤烧杯
③在定容时观察液面俯视
④最后定容时,加水超过了刻度,马上用胶头滴管吸去多余的水,使溶液凹液面刚好与刻度线相切
| A.②③④ | B.③④ | C.①②④ | D.①②③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关实验操作的叙述正确的是
| A.用量筒量取5.00mL1.00mol/盐酸于50mL容量瓶中,加水稀释至刻度,可配制0.100mol/L盐酸 |
| B.向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
| C.用铂丝做焰色反应实验,每次做完后都要用硫酸洗涤 |
| D.过滤操作中,为了加快过滤速度可用玻璃棒在漏斗中轻轻搅拌 |
您最近一年使用:0次