10 ℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
(1)甲同学认为,该溶液pH升高的原因是HCO3-的水解程度增大,碱性增强,该反应的离子方程式为____________________ 。
(2)乙同学认为:该溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度________ (填“大于”或“小于”)NaHCO3的水解程度。
(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液的pH,若pH______ 8.3(填“>”“<”或“=”,下同),说明甲同学正确;若_______ 8.3,说明乙同学正确。
| 温度(℃) | 10 | 20 | 30 | 50 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
(1)甲同学认为,该溶液pH升高的原因是HCO3-的水解程度增大,碱性增强,该反应的离子方程式为
(2)乙同学认为:该溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液的pH,若pH
19-20高二上·湖南株洲·阶段练习 查看更多[2]
湖南省株洲市茶陵县第三中学2019-2020学年高二上学期第三次月考化学(选考)试题(已下线)3.3.2 影响盐类水解的因素(重点练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)
更新时间:2019-12-26 01:06:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求填空
(1)常温时的Fe2(SO4)3的水溶液pH_______ 7(填“>”“<”或“=”),原因是(用离子方程式表示):_______ 。
(2)将AlCl3溶液蒸干、灼烧,最后所得的固体的主要成分是_______ 。
(3)纯碱溶液显碱性,原因是(用离子方程式表示):_______ 。
(4)物质的量浓度相同的三种盐NaX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是_______ 。
(5)常温时,向明矾溶液中逐滴加入Ba(OH)2溶液至SO 刚好沉淀完全时,溶液的pH
刚好沉淀完全时,溶液的pH_______ 7(填“>”“<”或“=”),离子反应总方程式为:_______ 。
(1)常温时的Fe2(SO4)3的水溶液pH
(2)将AlCl3溶液蒸干、灼烧,最后所得的固体的主要成分是
(3)纯碱溶液显碱性,原因是(用离子方程式表示):
(4)物质的量浓度相同的三种盐NaX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
(5)常温时,向明矾溶液中逐滴加入Ba(OH)2溶液至SO
 刚好沉淀完全时,溶液的pH
刚好沉淀完全时,溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】CH3COOH、H2CO3、H2SO3的电离常数如表所示。
请回答下列问题:
(1)①NaHSO3溶液中电荷守恒表达式_____ 。
②NaHSO3溶液中各离子浓度大小顺序:_____ 。
(2)①用离子方程式表示Na2CO3溶液碱性的原因_____ 。
②写出Na2CO3溶液中物料守恒表达式______ 。
③写出NaHCO3溶液中质子守恒表达式______ 。
(3)常温下,物质的量浓度相同的下列溶液:
①NH4Cl ② NH4HCO3 ③(NH4)2SO4 ④NH4HSO4 ⑤(NH4)2Fe(SO4)2
溶液中c(NH4+)从大到小排列顺序为____ (填序号)。
(4)常温下,物质的量浓度均为0.1mol/L的六种溶液①NaOH、②NaCl、③Na2CO3、④H2SO3、⑤CH3COONa、⑥H2SO4,pH从大到小排列顺序为____ (填序号)。
(5)常温时,AlCl3的水溶液呈酸性,原因是(用离子方程式表示):____ ,将AlCl3溶液蒸干,灼烧,最后得到的固体产物主要是____ (填化学式)。
(6)证明CH3COOH是弱电解质的简单且可行的方法是:_____ 。
(7)下列混合溶液中,各离子浓度的大小顺序或等量关系正确的是____ 。
A.10 mL0.1mol/L氨水与10mL0.1mol/L盐酸混合:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.10 mL0.1mol/LNH4Cl溶液与5mL0.2mol/LNaOH溶液混合:c(Na+)=c(Cl-)>c(OH-)>c(H+)
C.10mL0.1mol/LCH3COOH溶液与5mL0.2 mol/LNaOH溶液混合:c(Na+)=c(CH3COO-)>c(OH-)>c(H+)
D.10mL0.5mol/L CH3COONa溶液与6mL1mol/L盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+)
E.在NaHSO4溶液中,c(H+)=c(OH-)+c(SO42-)
| 酸 | 电离常数 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7,K2=5.6×10-11 |
| H2SO3 | K1=1.54×10-2 ,K2=1.02×10-7 |
请回答下列问题:
(1)①NaHSO3溶液中电荷守恒表达式
②NaHSO3溶液中各离子浓度大小顺序:
(2)①用离子方程式表示Na2CO3溶液碱性的原因
②写出Na2CO3溶液中物料守恒表达式
③写出NaHCO3溶液中质子守恒表达式
(3)常温下,物质的量浓度相同的下列溶液:
①NH4Cl ② NH4HCO3 ③(NH4)2SO4 ④NH4HSO4 ⑤(NH4)2Fe(SO4)2
溶液中c(NH4+)从大到小排列顺序为
(4)常温下,物质的量浓度均为0.1mol/L的六种溶液①NaOH、②NaCl、③Na2CO3、④H2SO3、⑤CH3COONa、⑥H2SO4,pH从大到小排列顺序为
(5)常温时,AlCl3的水溶液呈酸性,原因是(用离子方程式表示):
(6)证明CH3COOH是弱电解质的简单且可行的方法是:
(7)下列混合溶液中,各离子浓度的大小顺序或等量关系正确的是
A.10 mL0.1mol/L氨水与10mL0.1mol/L盐酸混合:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.10 mL0.1mol/LNH4Cl溶液与5mL0.2mol/LNaOH溶液混合:c(Na+)=c(Cl-)>c(OH-)>c(H+)
C.10mL0.1mol/LCH3COOH溶液与5mL0.2 mol/LNaOH溶液混合:c(Na+)=c(CH3COO-)>c(OH-)>c(H+)
D.10mL0.5mol/L CH3COONa溶液与6mL1mol/L盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+)
E.在NaHSO4溶液中,c(H+)=c(OH-)+c(SO42-)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列电解质溶液:
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
(1) 溶液呈
溶液呈___________ (填“酸性”“碱性”或“中性”),其原因是___________ (用离子方程式表示)。
(2)上述六种电解质溶液中,既能与盐酸反应又能与烧碱溶液反应的是___________ (填序号)。
(3)写出⑤与足量 溶液混合加热的离子方程式:
溶液混合加热的离子方程式:___________ 。
(4)常温下,物质的量浓度均为 的④、⑥、⑦三种溶液,溶液中
的④、⑥、⑦三种溶液,溶液中 由大到小的顺序为:
由大到小的顺序为:___________ >___________ >___________ (填序号)。
(5)已知: ,
,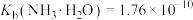 。常温下,
。常温下, 溶液中的pH
溶液中的pH___________ 7(填“>”“=”或“<”),理由是___________ 。
(6)已知 能定量完成反应:
能定量完成反应: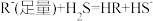 ,
,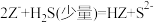 。相同温度下,相同物质的量浓度的①
。相同温度下,相同物质的量浓度的① ②
② ③
③ ④
④ 四种溶液的
四种溶液的 由大到小的顺序为:
由大到小的顺序为:___________ (填序号)。
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
(1)
 溶液呈
溶液呈(2)上述六种电解质溶液中,既能与盐酸反应又能与烧碱溶液反应的是
(3)写出⑤与足量
 溶液混合加热的离子方程式:
溶液混合加热的离子方程式:(4)常温下,物质的量浓度均为
 的④、⑥、⑦三种溶液,溶液中
的④、⑥、⑦三种溶液,溶液中 由大到小的顺序为:
由大到小的顺序为:(5)已知:
 ,
,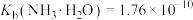 。常温下,
。常温下, 溶液中的pH
溶液中的pH(6)已知
 能定量完成反应:
能定量完成反应: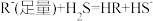 ,
,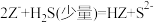 。相同温度下,相同物质的量浓度的①
。相同温度下,相同物质的量浓度的① ②
② ③
③ ④
④ 四种溶液的
四种溶液的 由大到小的顺序为:
由大到小的顺序为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
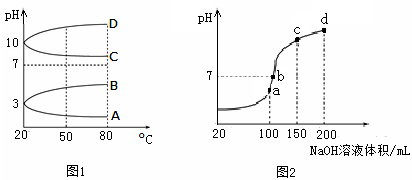
(1)如图1是几种0.1 mol·L-1电解质溶液的pH随温度变化的图象。
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是_________ (填写字母);
②20℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=______ 。
(2)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是___ 点;在b点,溶液中各离子浓度由大到小的排列顺序是____________ 。

(1)如图1是几种0.1 mol·L-1电解质溶液的pH随温度变化的图象。
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是
②20℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=
(2)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 在工业中有着广泛用途,实验室可利用
在工业中有着广泛用途,实验室可利用 的水解反应制取
的水解反应制取 。请回答下列问题:
。请回答下列问题:
(1) 是无色晶体,在空气中微发烟,分子中所有原子都达到了8电子稳定结构,请写出
是无色晶体,在空气中微发烟,分子中所有原子都达到了8电子稳定结构,请写出 的电子式:
的电子式:________________ 。
(2)利用 的水解反应制取
的水解反应制取 (
( 的水解分三步进行,中间产物有
的水解分三步进行,中间产物有 等)时,其总反应可表示为
等)时,其总反应可表示为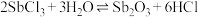 ,为了促进水解反应趋于完全,可采取的措施:
,为了促进水解反应趋于完全,可采取的措施:_____________________ (写两点即可)。
 在工业中有着广泛用途,实验室可利用
在工业中有着广泛用途,实验室可利用 的水解反应制取
的水解反应制取 。请回答下列问题:
。请回答下列问题:(1)
 是无色晶体,在空气中微发烟,分子中所有原子都达到了8电子稳定结构,请写出
是无色晶体,在空气中微发烟,分子中所有原子都达到了8电子稳定结构,请写出 的电子式:
的电子式:(2)利用
 的水解反应制取
的水解反应制取 (
( 的水解分三步进行,中间产物有
的水解分三步进行,中间产物有 等)时,其总反应可表示为
等)时,其总反应可表示为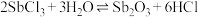 ,为了促进水解反应趋于完全,可采取的措施:
,为了促进水解反应趋于完全,可采取的措施:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】脱除工业废气中的氮氧化物(主要指NO和NO2)可以净化空气、改善环境,是环境保护的重要课题。
(1)以漂粉精溶液为吸收剂可以有效脱除烟气中的NO。
①漂粉精溶液的主要成分是Ca(ClO)2,若吸收过程中,消耗的Ca(ClO)2与吸收的NO的物质的量之比为3∶4,则脱除后NO转化为_______ (填离子符号)。
②某化学兴趣小组研究不同温度下相同浓度漂粉精溶液对NO脱除率的影响,结果如图1所示。图1中,40~60 ℃区间 NO脱除率上升的原因为_______ ;60~80 ℃ 区间NO脱除率下降的原因可能为_______ (写一点即可)。

(2)以过硫酸钠(Na2S2O8)为氧化剂是一种新型除NO方法。
第一步:NO在碱性环境中被Na2S2O8氧化为NaNO2;
第二步:NaNO2继续被氧化为NaNO3,反应为NO +S2O
+S2O +2OH-⇌NO
+2OH-⇌NO +2SO
+2SO +H2O。
+H2O。
不同温度下,平衡时NO 的脱除率与过硫酸钠溶液初始浓度(指第二步反应的初始浓度)的关系如图2 所示。
的脱除率与过硫酸钠溶液初始浓度(指第二步反应的初始浓度)的关系如图2 所示。
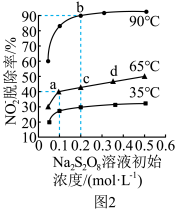
①若要平衡时NO 的脱除率至少达到90%,应选择的适宜条件是
的脱除率至少达到90%,应选择的适宜条件是_______ 。
②a、b、c三点对应平衡常数Ka、Kb、Kc的大小关系为_______ 。
③65 ℃时,NO 的初始浓度为c mol·L-1,平衡时c(OH-)=0.1 mol·L-1,该温度下第二步反应的平衡常数K=
的初始浓度为c mol·L-1,平衡时c(OH-)=0.1 mol·L-1,该温度下第二步反应的平衡常数K=_______ (用含c的代数式表示)。
(1)以漂粉精溶液为吸收剂可以有效脱除烟气中的NO。
①漂粉精溶液的主要成分是Ca(ClO)2,若吸收过程中,消耗的Ca(ClO)2与吸收的NO的物质的量之比为3∶4,则脱除后NO转化为
②某化学兴趣小组研究不同温度下相同浓度漂粉精溶液对NO脱除率的影响,结果如图1所示。图1中,40~60 ℃区间 NO脱除率上升的原因为

(2)以过硫酸钠(Na2S2O8)为氧化剂是一种新型除NO方法。
第一步:NO在碱性环境中被Na2S2O8氧化为NaNO2;
第二步:NaNO2继续被氧化为NaNO3,反应为NO
 +S2O
+S2O +2OH-⇌NO
+2OH-⇌NO +2SO
+2SO +H2O。
+H2O。不同温度下,平衡时NO
 的脱除率与过硫酸钠溶液初始浓度(指第二步反应的初始浓度)的关系如图2 所示。
的脱除率与过硫酸钠溶液初始浓度(指第二步反应的初始浓度)的关系如图2 所示。
①若要平衡时NO
 的脱除率至少达到90%,应选择的适宜条件是
的脱除率至少达到90%,应选择的适宜条件是②a、b、c三点对应平衡常数Ka、Kb、Kc的大小关系为
③65 ℃时,NO
 的初始浓度为c mol·L-1,平衡时c(OH-)=0.1 mol·L-1,该温度下第二步反应的平衡常数K=
的初始浓度为c mol·L-1,平衡时c(OH-)=0.1 mol·L-1,该温度下第二步反应的平衡常数K=
您最近一年使用:0次



