氮是我们熟悉的典型非金属元素,研究氮及其化合物的性质对于生产、生活、科研具有重要意义,请回答以下问题:


I. (1)图1为制取氨气的装置和选用的试剂,其中合理的是______________ (填字母)。
A,①② B. ②③ C. ②④ D. ①③
(2)实验室制备氨气的化学方程式是____________________________________ 。
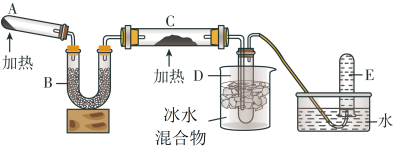
II. 图2位铵盐的受热分解装置
(1)被加热的铂丝处发生反应的化学方程式为____________________________________ 。
(2)B中出现的现象为_______________________________________________________ 。
(3)如图3:将上述烧杯C中反应得到酸的足量的浓溶液与Cu反应,实验完毕后,试管中收集到气体的主要成分为____________________ (写化学式)。



I. (1)图1为制取氨气的装置和选用的试剂,其中合理的是
A,①② B. ②③ C. ②④ D. ①③
(2)实验室制备氨气的化学方程式是
II. 图2位铵盐的受热分解装置
(1)被加热的铂丝处发生反应的化学方程式为
(2)B中出现的现象为
(3)如图3:将上述烧杯C中反应得到酸的足量的浓溶液与Cu反应,实验完毕后,试管中收集到气体的主要成分为
更新时间:2020-01-01 11:34:34
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
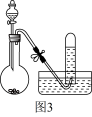
【推荐1】某化学兴趣小组欲探究NH3还原CuO的实验(部分夹持装置略),已知该反应生成对环境友好的物质。实验室装置图如下
回答下列问题:
(1)连接装置后,接下来的实验操作为_______ 。
(2)实验过程中点燃C处酒精灯之前应该先_______ 。
(3)A中制氨气的化学方程式是_______ 。
(4)装置B的作用是_______ 。装置D的作用是_______ 。
(5)该套装置不足之处_______ 。
(6)证明氨气能还原氧化铜的现象为_______ 。氨气还原氧化铜的方程式_______ 。
(7)一同学对反应产物存有疑虑,于是将尾气收集后与空气接触发现有少量红棕色气体生成,说明还存在的反应有_______ (用方程式表示)。

回答下列问题:
(1)连接装置后,接下来的实验操作为
(2)实验过程中点燃C处酒精灯之前应该先
(3)A中制氨气的化学方程式是
(4)装置B的作用是
(5)该套装置不足之处
(6)证明氨气能还原氧化铜的现象为
(7)一同学对反应产物存有疑虑,于是将尾气收集后与空气接触发现有少量红棕色气体生成,说明还存在的反应有
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】I.某实验小组利用以下装置制取氨气并探究氨气的性质:

(1)装置A中发生反应的化学方程式为______ 。
(2)装置B中的干燥剂是______ (填名称)。
(3)装置C中的现象是______ 。
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是____ ,发生反应的化学方程式为______ 。
(5)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是_____ (填“E”或“F”)。
II.现有足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体2.24L(标准状况),这些气体与一定体积O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4 mol∙L−1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL。
(6)参加反应的硝酸是_____ mol;标准状况下混合气体中含NO2体积为_____ L。

(1)装置A中发生反应的化学方程式为
(2)装置B中的干燥剂是
(3)装置C中的现象是
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是
II.现有足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体2.24L(标准状况),这些气体与一定体积O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4 mol∙L−1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL。
(6)参加反应的硝酸是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】框图所示的转化关系中,甲为生活中常见的金属单质,乙、丙、丁为气体单质,D为家庭中常用物质(部分反应物和生成物及溶剂水已略去)。
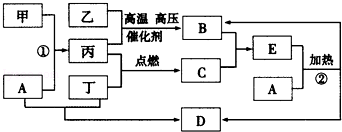
请回答:
(1)E的化学式为_______ ;甲的原子结构示意图为_______ ;
(2)反应①的离子方程式为_______ ;反应②的化学方程式为_______ ;
(3)实验室制取并收集B的操作中,用_______ 法收集B,验证B已收集满的方法是_______ (限答一种)。
(4)实验室制备丁的方程式为_______ ,工业上输送丁的管道出现气体泄漏,如何查漏(用方程式表示)_______ .

请回答:
(1)E的化学式为
(2)反应①的离子方程式为
(3)实验室制取并收集B的操作中,用
(4)实验室制备丁的方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
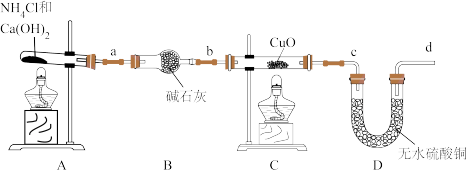
【推荐2】人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图一装置制备氨气并探究相关性质。
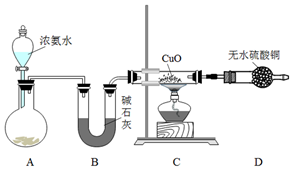
(1)装置B中,碱石灰作用___________ ;
(2)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体。则该反应相关化学方程式为:___________ 。 工业上,通过氨的催化氧化等一系列反 应最终可以制得硝酸,请写出氨的催化氧化的化学反应方程式______ ;
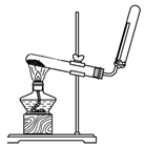
(3)实验室还可用下图所示装置制备氨气。化学反应方程式为___________ 。
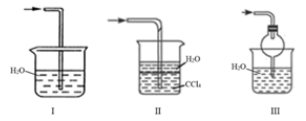
(4)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是___________ (填装置序号)。

(1)装置B中,碱石灰作用
(2)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体。则该反应相关化学方程式为:
(3)实验室还可用下图所示装置制备氨气。化学反应方程式为

(4)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
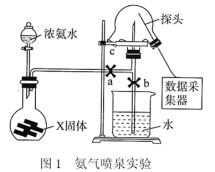
【推荐3】利用压强传感器测定氨气的喷泉实验中的压强变化。___________ 。
(2)可以用___________ 试纸置于三颈瓶口c处验满。
(3)关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧瓶口c,挤压胶头滴管,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,___________ 点时喷泉最剧烈(选填A、B、C、D、E)。 且混合均匀,实验开始前烧瓶中气体的平均分子量为
且混合均匀,实验开始前烧瓶中气体的平均分子量为___________ ,实验结束后烧瓶中溶液的物质的量浓度为___________ mol/L。
(2)可以用
(3)关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧瓶口c,挤压胶头滴管,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,
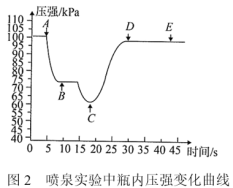
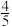 且混合均匀,实验开始前烧瓶中气体的平均分子量为
且混合均匀,实验开始前烧瓶中气体的平均分子量为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】固体化合物X由3种元素组成。某学习小组进行了如下实验:
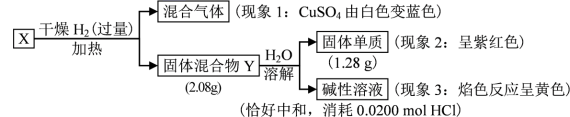
请回答:
(1)由现象1得出化合物X含有____________ 元素(填元素符号)。
(2)固体混合物Y的成分____________ (填化学式)。
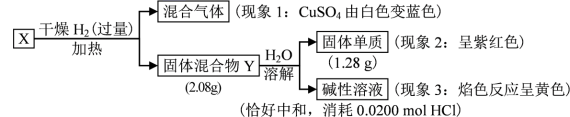
请回答:
(1)由现象1得出化合物X含有
(2)固体混合物Y的成分
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】实验室以含有Ca2+、Mg2+、Brˉ、Clˉ等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
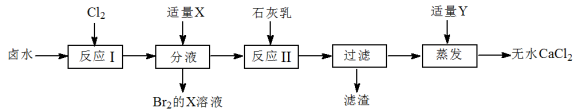
(1)试剂X可以选择___________(填字母序号)。
(2)试剂Y可以选择 ___________(填字母序号)
(3)反应Ⅰ的离子反应方程式是___________ 。
(4)分液所用主要仪器的名称是___________ 。
(5)已知:反应Ⅱ加石灰乳,调节溶液的pH范围是___________ 。其目的是___________ 。

(1)试剂X可以选择___________(填字母序号)。
| A.酒精 | B.四氯化碳 | C.水 | D.苯 |
| A.稀盐酸 | B.稀硫酸 | C.氢氧化钠 | D.氯化钠 |
(4)分液所用主要仪器的名称是
| 开始沉淀的pH | 完全沉淀的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OHˉ)=1.8mol/L |
(5)已知:反应Ⅱ加石灰乳,调节溶液的pH范围是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】84消毒液与NaCl、硫酸溶液在加热条件下反应可以生成氯气,反应原理为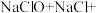
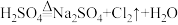 。为探究氯气的性质,某同学利用此原理制氯气并设计了如图所示的实验装置。
。为探究氯气的性质,某同学利用此原理制氯气并设计了如图所示的实验装置。
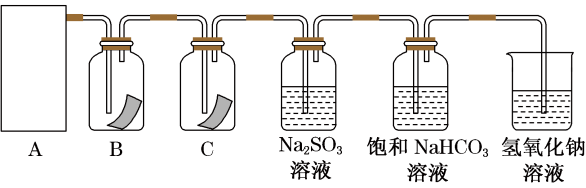
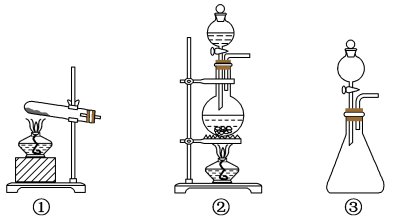
(1)从装置①、②、③中选择合适的制氯气装置(A处)__________ (填序号)。
(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中干燥的红色布条褪色,其原因可能是________________ ;说明该装置存在明显的缺陷,请提出合理的改进方法:_________________ 。
(3)为了验证氯气的氧化性,将氯气通入 溶液中,然后检验反应后的溶液中是否含有
溶液中,然后检验反应后的溶液中是否含有 。方法是取少量反应后的溶液于试管中,先加入足量的
。方法是取少量反应后的溶液于试管中,先加入足量的________ ,无明显现象,然后再加入少量______ (填化学式)溶液,有白色沉淀生成,说明含有 。
。
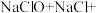
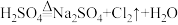 。为探究氯气的性质,某同学利用此原理制氯气并设计了如图所示的实验装置。
。为探究氯气的性质,某同学利用此原理制氯气并设计了如图所示的实验装置。
(1)从装置①、②、③中选择合适的制氯气装置(A处)

(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中干燥的红色布条褪色,其原因可能是
(3)为了验证氯气的氧化性,将氯气通入
 溶液中,然后检验反应后的溶液中是否含有
溶液中,然后检验反应后的溶液中是否含有 。方法是取少量反应后的溶液于试管中,先加入足量的
。方法是取少量反应后的溶液于试管中,先加入足量的 。
。
您最近一年使用:0次