向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
(1)写出H2O分子的电子式:________ 。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是________ 。
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
Ⅱ.胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、花卉上。
(3)写出铜原子价电子层的电子排布式:_____ ,与铜同一周期副族元素的基态原子中最外层电子数与铜原子相同的元素有________ (填元素符号)。
(4)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有________ 。
(5)实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是_________________________ 。
Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
(1)写出H2O分子的电子式:
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
Ⅱ.胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、花卉上。
(3)写出铜原子价电子层的电子排布式:
(4)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有
(5)实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是
更新时间:2020-01-14 17:05:34
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求回答下列问题:
(1)在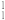 H、
H、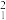 H、
H、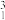 H、
H、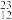 Mg、
Mg、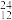 Mg和
Mg和 Cu中共有
Cu中共有______ 种元素,______ 种原子
(2)下列各组微粒:①16O2和18O2 ②H2和D2 ③1735Cl和1737Cl ④1H218O和2H216O属于同位素的是___________________
(3)下列物质中:H2O2、KCl、Na2SO4、Na2O2、HCl、O2; 其中只含离子键的是________ ,只含极性键的是______ ,既含离子键又含极性键的是_____ ,既含离子键又含非极性键的是_______
(4)写出下列物质的电子式:Na2O2 :______________ H2O2 :________________
(5)用电子式表示下列化合物的形成过程
H2S:__________________________________
KCl:_________________
(1)在
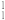 H、
H、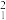 H、
H、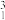 H、
H、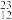 Mg、
Mg、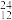 Mg和
Mg和 Cu中共有
Cu中共有(2)下列各组微粒:①16O2和18O2 ②H2和D2 ③1735Cl和1737Cl ④1H218O和2H216O属于同位素的是
(3)下列物质中:H2O2、KCl、Na2SO4、Na2O2、HCl、O2; 其中只含离子键的是
(4)写出下列物质的电子式:Na2O2 :
(5)用电子式表示下列化合物的形成过程
H2S:
KCl:
您最近一年使用:0次
【推荐2】碳与硅是十分重要的两种元素,金刚石、SiC具有耐磨、耐腐蚀特性,应用广泛。
(1)碳元素在周期表中的位置是_______________ ,其原子核外通常未成对电子数为___________ 个。
(2)已知2Ca3(PO4)2(s)+10C(s)→P4(g)+6CaO(s)+10CO(g)反应中,被破坏的化学键有________ 。
a.离子键 b.极性共价键 c. 非极性共价键
(3)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,除去粗产品中少量钠的试剂为_______________ 。
(4)下列叙述正确的有____________ 填序号),
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③NaSiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④Si在一定条件下可与FeO发生置换反应
(1)碳元素在周期表中的位置是
(2)已知2Ca3(PO4)2(s)+10C(s)→P4(g)+6CaO(s)+10CO(g)反应中,被破坏的化学键有
a.离子键 b.极性共价键 c. 非极性共价键
(3)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,除去粗产品中少量钠的试剂为
(4)下列叙述正确的有
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③NaSiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④Si在一定条件下可与FeO发生置换反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】表为元素周期表中短周期元素的一部分,表中所列的字母分别代表一种元素。
(1)a、b、c、d、e、f六种元素的原子半径最大的是_______ (填元素符号)。
(2)d、e两种元素的最高价氧化物对应水化物的碱性较强的物质俗称为_______ , 、
、 的沸点较高的是
的沸点较高的是_______ (填化学式)。
(3)过量的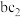 与
与 溶液能发生反应,写出反应的离子方程式:
溶液能发生反应,写出反应的离子方程式:_______ 。
(4)化学式为 的化合物属于
的化合物属于_______ (填“离子化合物”或“共价化合物”),其中含有的化学键的类型为_______ 。
| a | |||||||
| b | c | ||||||
| d | e | f |
(2)d、e两种元素的最高价氧化物对应水化物的碱性较强的物质俗称为
 、
、 的沸点较高的是
的沸点较高的是(3)过量的
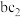 与
与 溶液能发生反应,写出反应的离子方程式:
溶液能发生反应,写出反应的离子方程式:(4)化学式为
 的化合物属于
的化合物属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某元素原子序数为24,试问:
它有__________ 个能层,__________ 个能级,占有__________ 个原子轨道
它有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求填空:
(1)写出下列化合物的电子式:KCN_______ ,NaClO_______
(2)写出下列基态原子或离子核外电子排布式:P_______ ,Fe2+ _______
(3)写出下列微粒中心原子的杂化方式:CCl4_______ ,NO
_______
(4)铬原子的最高能层符号是_______ ,其价层电子的轨道表达式为_______ 。
(5)比较第二电离能Cu_______ Zn(填“>”、“=”、“<”),理由是:_______ 。
(1)写出下列化合物的电子式:KCN
(2)写出下列基态原子或离子核外电子排布式:P
(3)写出下列微粒中心原子的杂化方式:CCl4

(4)铬原子的最高能层符号是
(5)比较第二电离能Cu
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制等方面发挥着越来越大的作用。
(1)三氯化钛( )用于催化聚丙烯的生产等。在浓的
)用于催化聚丙烯的生产等。在浓的 溶液中加入乙醚,并通入
溶液中加入乙醚,并通入 至饱和,可得到配位数为6、组成为
至饱和,可得到配位数为6、组成为 的绿色晶体,该晶体中两配位体的物质的量之比为1∶5,则该配离子的化学式为
的绿色晶体,该晶体中两配位体的物质的量之比为1∶5,则该配离子的化学式为___________ 。
(2)研究表明,对于中心离子为 等阳离子的配合物,配位体给出电子的能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定。预测
等阳离子的配合物,配位体给出电子的能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定。预测 与
与 的稳定性强弱:
的稳定性强弱: 与
与 更
更___________ (填“稳定”或“不稳定”)。
(1)三氯化钛(
 )用于催化聚丙烯的生产等。在浓的
)用于催化聚丙烯的生产等。在浓的 溶液中加入乙醚,并通入
溶液中加入乙醚,并通入 至饱和,可得到配位数为6、组成为
至饱和,可得到配位数为6、组成为 的绿色晶体,该晶体中两配位体的物质的量之比为1∶5,则该配离子的化学式为
的绿色晶体,该晶体中两配位体的物质的量之比为1∶5,则该配离子的化学式为(2)研究表明,对于中心离子为
 等阳离子的配合物,配位体给出电子的能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定。预测
等阳离子的配合物,配位体给出电子的能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定。预测 与
与 的稳定性强弱:
的稳定性强弱: 与
与 更
更
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含有____ mol配位键。
您最近一年使用:0次

 基态核外电子排布式为
基态核外电子排布式为 基态核外电子排布式为
基态核外电子排布式为 ⑧BF3⑨H2O ⑩N2(填序号)
⑧BF3⑨H2O ⑩N2(填序号)

