无水氯化铁加热易升华,遇潮湿空气易变质。在实验室中,可以采用如下装置和药品制取较纯的无水氯化铁固体。
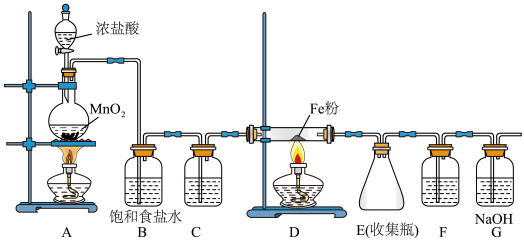
(1)制取氯化铁时,应先点燃_____ (填“A”或“D”)处的酒精灯,制取氯化铁的化学方程式为_____ 。
(2)C、F装置中所装试剂相同,试剂均为________ 。
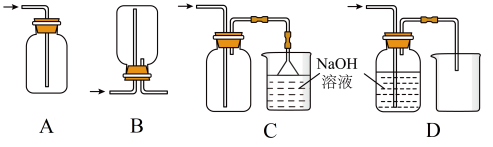
(3)下列收集Cl2的正确装置是______ 。
(4)G装置中反应的离子方程式为________________________________ 。
(5)反应后装置D中残余的固体混合物溶于稀盐酸,滴加几滴KSCN溶液。若溶液变血红色,推断固体物质的成分为______ (选填序号,下同);写出溶液变血红色的离子方程式:_____________ ,若溶液未变血红色,推断固体物质的成分为______ 。
A. 只有 FeCl3 B.只有Fe C.一定有 FeCl3 D.一定有Fe

(1)制取氯化铁时,应先点燃
(2)C、F装置中所装试剂相同,试剂均为
(3)下列收集Cl2的正确装置是

(4)G装置中反应的离子方程式为
(5)反应后装置D中残余的固体混合物溶于稀盐酸,滴加几滴KSCN溶液。若溶液变血红色,推断固体物质的成分为
A. 只有 FeCl3 B.只有Fe C.一定有 FeCl3 D.一定有Fe
更新时间:2020-01-17 16:04:41
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】如图1所示,A是氯气的发生装置,B、C是净化气体的装置,D中装铁丝网;反应后E的底部有棕黄色固体聚集;F中盛放NaOH溶液,是吸收多余气体的吸收装置
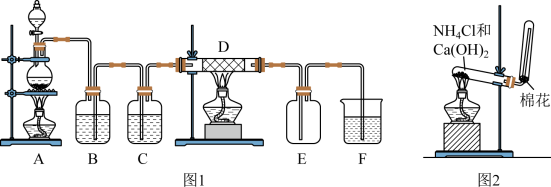
(1)上述装置中有一处明显错误,请指出是_________ 处(用字母表示)
(2)实验室用二氧化锰和浓盐酸加热制氯气,写出A中反应的化学方程式___________________
(3)B中盛放饱和食盐水,其作用是_________________________
(4)写出D中发生反应的化学方程式_________________________
图2是实验室制氨气的装置图,请回答:
(5)写出实验室制氨气的化学方程式:_______________________
(6)干燥氨气的干燥剂通常用_____________
(7)如何检验氨气是否收集满:_____________________________

(1)上述装置中有一处明显错误,请指出是
(2)实验室用二氧化锰和浓盐酸加热制氯气,写出A中反应的化学方程式
(3)B中盛放饱和食盐水,其作用是
(4)写出D中发生反应的化学方程式
图2是实验室制氨气的装置图,请回答:
(5)写出实验室制氨气的化学方程式:
(6)干燥氨气的干燥剂通常用
(7)如何检验氨气是否收集满:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室用浓盐酸、二氧化锰共热制氯气,但是氯气是有毒的污染性气体,在制取的过程中必须在通风橱内进行。下图是某研究性学习小组设计的在没有通风橱的情况下,收集纯净的氯气,图中A、B是可控制的弹簧夹。

(1)写出制取氯气的化学方程式_______
(2)烧杯中盛放的液体是____ ,其作用是____ ,写出其作用的反应离子方程式:____ 。
(3)水槽中应盛放的液体是_______ 。
(4)简述操作过程:
①开始收集氯气:应打开_______ ,关闭_______ ;
②氯气收集完毕:应打开_______ ,关闭_______ 。

(1)写出制取氯气的化学方程式
(2)烧杯中盛放的液体是
(3)水槽中应盛放的液体是
(4)简述操作过程:
①开始收集氯气:应打开
②氯气收集完毕:应打开
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】碘酸钙[Ca(IO3)2]是广泛使用的既能补钙又能补碘的新型食品添加剂,不溶于乙醇,在水中的溶解度随温度降低而减小。实验室制取Ca(IO3)2的流程如图所示:
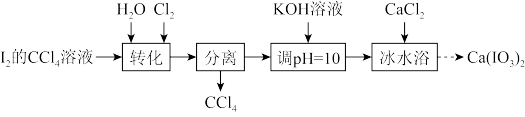
已知:碘酸(HIO3)是易溶于水的强酸,不溶于有机溶剂。
(1)实验流程中“转化”步骤是为了制得碘酸,该过程在下图所示的装置中进行(部分仪器省略)。
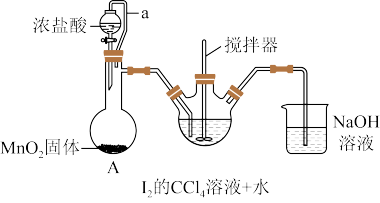
①盛装浓盐酸的仪器的名称为___________ 。
②橡皮管a的作用是___________ 。
③装置A中反应需要加热,其反应的离子方程式___________ 。
(2)三颈烧瓶中发生“转化”的化学方程式___________ 。
(3)流程中采用冰水浴的目的是__ 。
(4)有关该实验说法正确的是__ 。
A.分离出CCl4的操作为分液。
B.“调pH=10”后的溶液中只含有KIO3
C.制得的碘酸钙可选用酒精溶液洗涤
(5)准确称取产品0.25g,加酸溶解后,再加入足量KI发生反应 +5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液,用0.2000 mol·L-1Na2S2O3溶液滴定(I2+2
+5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液,用0.2000 mol·L-1Na2S2O3溶液滴定(I2+2 =2I-+
=2I-+ )至终点,消耗Na2S2O3溶液30.00mL。达滴定终点时的现象是
)至终点,消耗Na2S2O3溶液30.00mL。达滴定终点时的现象是___________ , 产品中Ca(IO3)2的质量分数___________ [已知Ca(IO3)2的摩尔质量: 390g·mol-1]

已知:碘酸(HIO3)是易溶于水的强酸,不溶于有机溶剂。
(1)实验流程中“转化”步骤是为了制得碘酸,该过程在下图所示的装置中进行(部分仪器省略)。

①盛装浓盐酸的仪器的名称为
②橡皮管a的作用是
③装置A中反应需要加热,其反应的离子方程式
(2)三颈烧瓶中发生“转化”的化学方程式
(3)流程中采用冰水浴的目的是
(4)有关该实验说法正确的是
A.分离出CCl4的操作为分液。
B.“调pH=10”后的溶液中只含有KIO3
C.制得的碘酸钙可选用酒精溶液洗涤
(5)准确称取产品0.25g,加酸溶解后,再加入足量KI发生反应
 +5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液,用0.2000 mol·L-1Na2S2O3溶液滴定(I2+2
+5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液,用0.2000 mol·L-1Na2S2O3溶液滴定(I2+2 =2I-+
=2I-+ )至终点,消耗Na2S2O3溶液30.00mL。达滴定终点时的现象是
)至终点,消耗Na2S2O3溶液30.00mL。达滴定终点时的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】三氯化铬是化学合成中的常见物质,三氯化铬易升华,在高温下能被氧气氧化。制备三氯化铬的流程如下图所示:

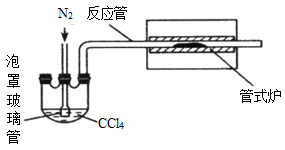
(1)重铬酸铵分解产生的三氧化二铬(Cr2O3 难溶于水)需用蒸馏水洗涤,不用化学方法如何用简单方法判断其已洗涤干净?_____ 。
(2)用上图装置制备 CrCl3时,反应管中发生的主要反应为:Cr2O3+3CCl4=2CrCl3+3COCl2,则向三颈烧瓶中通入 N2的作用:①_____ ;②鼓气使反应物进入管式炉中进行反应。
(3)样品中三氯化铬质量分数的测定:称取样品 0.3000g,加水溶解并定容于 250mL 容量瓶中。移取 25.00mL 于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入 1g Na2O2,充分加热煮沸,适当稀释,然后加入过量 2mol·L–1H2SO4至溶液呈强酸性,此时铬以 存在,再加入 1.1g KI,加塞摇匀,充分反应后铬以 Cr3+存在,于暗处静置 5min 后,加入 0.5mL 指示剂,用 0.0250mol·L–1标准 Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准 Na2S2O3溶液 18.00mL。(已知:2Na2S2O3+I2 =Na2S4O6+2NaI,CrCl3相对分子质量为 158.5)
存在,再加入 1.1g KI,加塞摇匀,充分反应后铬以 Cr3+存在,于暗处静置 5min 后,加入 0.5mL 指示剂,用 0.0250mol·L–1标准 Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准 Na2S2O3溶液 18.00mL。(已知:2Na2S2O3+I2 =Na2S4O6+2NaI,CrCl3相对分子质量为 158.5)
①滴定实验选用的指示剂为淀粉溶液,判定滴定终点的现象是_____ 。若加入 Na2O2后不加热煮沸,结果_____ 。 (填“偏高”“偏低”或“无影响”)
②加入 KI 时发生反应的离子方程式为_____ 。
③样品中无水三氯化铬的质量分数为_____ 。


(1)重铬酸铵分解产生的三氧化二铬(Cr2O3 难溶于水)需用蒸馏水洗涤,不用化学方法如何用简单方法判断其已洗涤干净?
(2)用上图装置制备 CrCl3时,反应管中发生的主要反应为:Cr2O3+3CCl4=2CrCl3+3COCl2,则向三颈烧瓶中通入 N2的作用:①
(3)样品中三氯化铬质量分数的测定:称取样品 0.3000g,加水溶解并定容于 250mL 容量瓶中。移取 25.00mL 于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入 1g Na2O2,充分加热煮沸,适当稀释,然后加入过量 2mol·L–1H2SO4至溶液呈强酸性,此时铬以
 存在,再加入 1.1g KI,加塞摇匀,充分反应后铬以 Cr3+存在,于暗处静置 5min 后,加入 0.5mL 指示剂,用 0.0250mol·L–1标准 Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准 Na2S2O3溶液 18.00mL。(已知:2Na2S2O3+I2 =Na2S4O6+2NaI,CrCl3相对分子质量为 158.5)
存在,再加入 1.1g KI,加塞摇匀,充分反应后铬以 Cr3+存在,于暗处静置 5min 后,加入 0.5mL 指示剂,用 0.0250mol·L–1标准 Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准 Na2S2O3溶液 18.00mL。(已知:2Na2S2O3+I2 =Na2S4O6+2NaI,CrCl3相对分子质量为 158.5)①滴定实验选用的指示剂为淀粉溶液,判定滴定终点的现象是
②加入 KI 时发生反应的离子方程式为
③样品中无水三氯化铬的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究小组同学在实验室用卤块制备少量Mg(ClO3)2·6H2O,其流程如图所示:
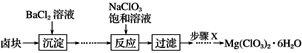
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
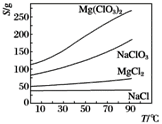
②四种化合物的溶解度(S)随温度(T)的变化曲线如图所示。
③形成氢氧化物沉淀时,不同离子对应溶液的pH如下:Fe2+开始沉淀的pH为5.8,完全沉淀的pH为8.8;Fe3+开始沉淀的pH为1.1,完全沉淀的pH为3.2;Mg2+开始沉淀的pH为8.2,完全沉淀的pH为11。
④可选用的试剂:H2O2、稀硫酸、KMnO4溶液、MgCl2溶液、MgO。
(1)步骤X包含的操作为___________ 、 ___________ 、____________ 、过滤洗涤并干燥。
(2)加入BaCl2溶液沉淀后需经过两步实验步骤才进行下步反应,请写出这两步实验步骤:
①________________________________________________________________________ ;
②_______________________________________________________________________ ;
(3)加入NaClO3饱和溶液发生反应的化学方程式为_______________________________ 。
(4)将Mg(ClO3)2加入到含有KSCN的FeSO4溶液中立即出现红色,写出相关反应的离子方程式______________ 。

已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度(T)的变化曲线如图所示。

③形成氢氧化物沉淀时,不同离子对应溶液的pH如下:Fe2+开始沉淀的pH为5.8,完全沉淀的pH为8.8;Fe3+开始沉淀的pH为1.1,完全沉淀的pH为3.2;Mg2+开始沉淀的pH为8.2,完全沉淀的pH为11。
④可选用的试剂:H2O2、稀硫酸、KMnO4溶液、MgCl2溶液、MgO。
(1)步骤X包含的操作为
(2)加入BaCl2溶液沉淀后需经过两步实验步骤才进行下步反应,请写出这两步实验步骤:
①
②
(3)加入NaClO3饱和溶液发生反应的化学方程式为
(4)将Mg(ClO3)2加入到含有KSCN的FeSO4溶液中立即出现红色,写出相关反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,溶于水成绿色,难溶于乙醇,见光分解,是一些有机反应的催化剂。制备三草酸合铁酸钾主要有两步,制备FeC2O4黄色沉淀,并在K2C2O4、H2C2O4并存时氧化FeC2O4制得产品:
(NH4)2Fe(SO4)2·6H2O+H2C2O4 FeC2O4·2H2O↓+(NH4)2SO4+H2SO4+4H2O
FeC2O4·2H2O↓+(NH4)2SO4+H2SO4+4H2O
2 FeC2O4·2H2O+H2O2+3K2C2O4+H2C2O4 2K3Fe(C2O4)3·3H2O
2K3Fe(C2O4)3·3H2O
(1) K3[Fe(C2O4)3]·3H2O (三草酸合铁酸钾)铁元素化合价为______ 。
(2)实验时需要滴加1mol·L-1H2SO4溶液,配制该溶液需要的玻璃仪器有玻璃棒、胶头滴管、容量瓶、______ 和______ 。
(3)用如图装置制备FeC2O4·2H2O时,药品添加的顺序是:______ (填序号),加热溶解后再滴入草酸。
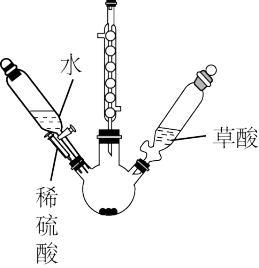
A.先加入硫酸,再滴入水 B.先滴入水,再加入硫酸
(4)制备三草酸合铁酸钾,保持温度为40℃左右,原因是______ 。观察到______ 现象时,反应结束,此时加热至沸,主要的目的是______ (用化学方程式表示)。然后冷却至室温,加入______ (填化学式)和硝酸钾固体,搅拌,洗出亮绿色晶体。
(NH4)2Fe(SO4)2·6H2O+H2C2O4
 FeC2O4·2H2O↓+(NH4)2SO4+H2SO4+4H2O
FeC2O4·2H2O↓+(NH4)2SO4+H2SO4+4H2O2 FeC2O4·2H2O+H2O2+3K2C2O4+H2C2O4
 2K3Fe(C2O4)3·3H2O
2K3Fe(C2O4)3·3H2O(1) K3[Fe(C2O4)3]·3H2O (三草酸合铁酸钾)铁元素化合价为
(2)实验时需要滴加1mol·L-1H2SO4溶液,配制该溶液需要的玻璃仪器有玻璃棒、胶头滴管、容量瓶、
(3)用如图装置制备FeC2O4·2H2O时,药品添加的顺序是:

A.先加入硫酸,再滴入水 B.先滴入水,再加入硫酸
(4)制备三草酸合铁酸钾,保持温度为40℃左右,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】马鞍山有丰富的黄铁矿,可用于工业制硫酸,该市硫酸厂可用下列仪器组装一套装置来测定黄铁矿 (主要成分FeS2)中硫的质量分数(忽略SO2、H2SO3与氧气的反应)。实验的正确操作步骤如下:

A.连接好装置,并检查装置的气密性
B.称取研细的黄铁矿样品
C.将2.0g样品小心地放入硬质玻璃管中
D.以1L∙min-1的速率鼓入空气
E.将硬质玻璃管中的黄铁矿样品加热到800°C~850°C
F.用300mL的足量饱和碘水吸收SO2,发生的反应是:I2+SO2+2H2O=2HI+H2SO4
G.吸收液用CCl4萃取、分离
H.取20.00mL G中所得溶液,用0.2000mol/L的NaOH标准溶液滴定。
试回答:
(1)步骤G中所用主要仪器是__________ ,应取__________ (填“上”或“下”)层溶液进行后续实验。
(2)装置正确的连接顺序是____ →____ 一___ →④→____ (填编号)。
(3)装置⑤中KMnO4的作用是_______ 。 若缺少装置⑤,则测定结果会__________ (填“偏大”“偏小”或“不变”)。
(4)步骤H中滴定时一般选用_____ 作指示剂,可以根据________ 现象来判断滴定已经达到终点。
(S)假定黄铁矿中的硫在操作E中已全部转化为SO2,并且被饱和碘水完全吸收,滴定得到的数据如下表所示:
则黄铁矿样品中硫元素的质量分数为____________ (保留小数点后1位)。
(6)也有人提出用“沉淀质量法”测定黄铁矿中含硫质量分数,若用这种方法测定,最好是在装置①所得吸收液中加入下列哪种试剂_________________ 。
A.硝酸银溶液 B.氯化钡溶液 C.澄清石灰水 D.酸性高锰酸钾溶液

A.连接好装置,并检查装置的气密性
B.称取研细的黄铁矿样品
C.将2.0g样品小心地放入硬质玻璃管中
D.以1L∙min-1的速率鼓入空气
E.将硬质玻璃管中的黄铁矿样品加热到800°C~850°C
F.用300mL的足量饱和碘水吸收SO2,发生的反应是:I2+SO2+2H2O=2HI+H2SO4
G.吸收液用CCl4萃取、分离
H.取20.00mL G中所得溶液,用0.2000mol/L的NaOH标准溶液滴定。
试回答:
(1)步骤G中所用主要仪器是
(2)装置正确的连接顺序是
(3)装置⑤中KMnO4的作用是
(4)步骤H中滴定时一般选用
(S)假定黄铁矿中的硫在操作E中已全部转化为SO2,并且被饱和碘水完全吸收,滴定得到的数据如下表所示:
| 滴定次数 | 待测液的体积/mL | NaOH标准溶液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 第一次 | 20.00 | 0.00 | 20.48 |
| 第二次 | 20.00 | 0.22 | 20.20 |
| 第三次 | 20.00 | 0.36 | 20.38 |
(6)也有人提出用“沉淀质量法”测定黄铁矿中含硫质量分数,若用这种方法测定,最好是在装置①所得吸收液中加入下列哪种试剂
A.硝酸银溶液 B.氯化钡溶液 C.澄清石灰水 D.酸性高锰酸钾溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某科学探究小组设计以下装置依次完成氯气的制备、氯酸钠的制备、次氯酸钠的制备并探究氯水的性质。

①为氯气发生装置,烧瓶中盛放MnO2固体;
②的试管里盛有15 mL 30%NaOH溶液。并置于热水浴中;
③的试管里盛有15 ml 8% NaOH溶液,并置于冰水浴中;
④的试管里加有紫色石磊试液:
⑤为尾气吸收装置。
(1)如何检验装置①的气密性_________________ 。
(2)如果实验室没有MnO2,下列物质可以用来代替MnO2制Cl2的是___________。
(3)制备氯酸钠的化学方程式为_____________________ 。
(4)比较制取氯酸钠和次氯酸钠的条件,二者的差异是:__________ 。
(5)④的试管里紫色石蕊试液现象:________________ 。
(6)次氯酸钠溶液可以杀灭析冠病毒,若将其与稀硫酸混合使用可增强消毒能力。现用18 mol/L浓硫酸来配制450 mL 0.2mol/L的稀硫酸。
①需用量筒量取浓硫酸的体积为_____ mL。
②定容时的操作:当液面离容量瓶颈部的刻度线1-2 cm时,_______ ,反复上下顺倒,摇匀。
③若所配制的稀硫酸浓度偏高,则下列可能的原因分析中正多的是________ 。
A.配制前,容量瓶用蒸馏水洗涤后再用硫酸润洗
B.量取浓硫酸时,读数时俯视液体的凹液面
C.浓硫酸稀释后立即转移至容量瓶定容
D.颠倒摇匀后,液面低于刻度线,继续滴加蒸馏水

①为氯气发生装置,烧瓶中盛放MnO2固体;
②的试管里盛有15 mL 30%NaOH溶液。并置于热水浴中;
③的试管里盛有15 ml 8% NaOH溶液,并置于冰水浴中;
④的试管里加有紫色石磊试液:
⑤为尾气吸收装置。
(1)如何检验装置①的气密性
(2)如果实验室没有MnO2,下列物质可以用来代替MnO2制Cl2的是___________。
| A.KMnO4 | B.Fe2O3 | C.浓硫酸 | D.KClO3 |
(4)比较制取氯酸钠和次氯酸钠的条件,二者的差异是:
(5)④的试管里紫色石蕊试液现象:
(6)次氯酸钠溶液可以杀灭析冠病毒,若将其与稀硫酸混合使用可增强消毒能力。现用18 mol/L浓硫酸来配制450 mL 0.2mol/L的稀硫酸。
①需用量筒量取浓硫酸的体积为
②定容时的操作:当液面离容量瓶颈部的刻度线1-2 cm时,
③若所配制的稀硫酸浓度偏高,则下列可能的原因分析中正多的是
A.配制前,容量瓶用蒸馏水洗涤后再用硫酸润洗
B.量取浓硫酸时,读数时俯视液体的凹液面
C.浓硫酸稀释后立即转移至容量瓶定容
D.颠倒摇匀后,液面低于刻度线,继续滴加蒸馏水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】叠氮化钠(NaN3)常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并与氨气充分反应后,停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。

已知:I.NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
II.NaNH2熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)装置B中盛放的药品为___ ;装置C的主要作用是___ 。
(2)步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为___ 。步骤③中最适宜的加热方式为____ (填“水浴加热”,“油浴加热”)。
(3)N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则可选择的气体发生装置是(填序号)___ 。

(4)生成NaN3的化学方程式为____ 。
(5)图中仪器a用的是铁质而不用玻璃,其主要原因是____ 。
(6)步骤④中用乙醚洗涤的主要目的是____ 。
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并与氨气充分反应后,停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。

已知:I.NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
II.NaNH2熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)装置B中盛放的药品为
(2)步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为
(3)N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则可选择的气体发生装置是(填序号)

(4)生成NaN3的化学方程式为
(5)图中仪器a用的是铁质而不用玻璃,其主要原因是
(6)步骤④中用乙醚洗涤的主要目的是
您最近一年使用:0次



