已知2SO2(g)+ O2(g)⇌2SO3(g);∆H=-196.64kJ⋅mol-1,下列说法正确的是( )
| A.该反应是吸热反应 |
| B.SO2燃烧热为196.64kJ⋅mol-1 |
| C.在容器中充入1molSO2和0.5molO2充分反应,热变化为98.32kJ |
| D.当有NA个电子发生转移时,热变化为49.16kJ |
更新时间:2020-02-14 20:43:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】设NA为阿伏伽德罗常数的值,下列说法错误的是
| A.室温下,20gKH固体中所含H-的数目为0.5NA |
| B.1L0.01mol·L-1的Ca(HCO3)2溶液中含碳粒子总数为0.02NA |
| C.50g质量分数为46%的乙醇水溶液中含有的氧原子总数为0.5NA |
| D.2NH3(g)⇌3H2(g)+N2(g) ΔH=+akJ·mol-1,若参加反应的NH3数目为2NA,反应会吸收akJ热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】相同温度时,下列两个反应的反应热分别用ΔH1和ΔH2表示,则
①H2(g)+ O2(g)=H2O(g) ΔH1=-Q1 kJ/mol;
O2(g)=H2O(g) ΔH1=-Q1 kJ/mol;
②2H2O(l)=2H2(g)+O2(g) ΔH2=+Q2 kJ/mol
①H2(g)+
 O2(g)=H2O(g) ΔH1=-Q1 kJ/mol;
O2(g)=H2O(g) ΔH1=-Q1 kJ/mol;②2H2O(l)=2H2(g)+O2(g) ΔH2=+Q2 kJ/mol
| A.Q1>Q2 | B.Q1=Q2 | C.2Q1<Q2 | D. Q2=Q1 Q2=Q1 |
您最近一年使用:0次
【推荐3】氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)燃烧的热化学方程式分别为:
H2 (g) + O2(g) = H2O (l) △H = -285.8 kJ /mol
O2(g) = H2O (l) △H = -285.8 kJ /mol
CO(g) + O2(g) = CO2(g) △H = -283 kJ /mol
O2(g) = CO2(g) △H = -283 kJ /mol
C8H18 (l) + O2(g) = 8CO2(g) + 9H2O (l) △H = -5518 kJ /mol
O2(g) = 8CO2(g) + 9H2O (l) △H = -5518 kJ /mol
CH4 (g) + 2O2(g) = CO2(g) + 2H2O (l) △H = -890.3 kJ /mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是
H2 (g) +
 O2(g) = H2O (l) △H = -285.8 kJ /mol
O2(g) = H2O (l) △H = -285.8 kJ /molCO(g) +
 O2(g) = CO2(g) △H = -283 kJ /mol
O2(g) = CO2(g) △H = -283 kJ /molC8H18 (l) +
 O2(g) = 8CO2(g) + 9H2O (l) △H = -5518 kJ /mol
O2(g) = 8CO2(g) + 9H2O (l) △H = -5518 kJ /molCH4 (g) + 2O2(g) = CO2(g) + 2H2O (l) △H = -890.3 kJ /mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是
| A.H2 (g) | B.CO(g) | C.C8H18 (l) | D.CH4 (g) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关热化学方程式的书写和叙述正确的是
A. 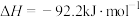 ,则在一定条件下向密闭容器中充入 ,则在一定条件下向密闭容器中充入 和 和 充分反应后放出46.1kJ的热量 充分反应后放出46.1kJ的热量 |
B.甲烷的燃烧热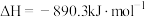 ,则甲烷燃烧的热化学方程式可表示为 ,则甲烷燃烧的热化学方程式可表示为 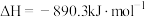 |
C.已知: 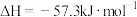 ,则 ,则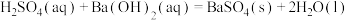  |
D.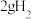 在氧气中完全燃烧生成液态水放出热量为285.8kJ,其热化学方程式可表示为 在氧气中完全燃烧生成液态水放出热量为285.8kJ,其热化学方程式可表示为  |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.在101kPa时,1molC与适量O2反应生成1molCO时,放出110.5kJ热量,则C的燃烧热为110.5kJ/mol |
| B.在101kPa时,1molH2完全燃烧生成液态水,放出285.8kJ热量,H2燃烧热为-285.8kJ·mol-1 |
| C.测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度、NaOH起始温度和反应后最高温度 |
| D.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量等于57.3kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列有关反应热的说法中正确的是
| A.已知:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,则1.00L 1.00mol·L-1H2SO4溶液与足量稀NaOH溶液完全反应放出57.3kJ的热量 |
| B.在101kPa时,1molCH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热 |
| C.同温同压下,H2(g)+Cl2(g)=2HCl (g)在光照和点燃条件下ΔH不同 |
| D.已知S(g)+O2(g)=SO2(g) ΔH1; S(S)+O2(g)=SO2(g) ΔH2,则ΔH1<ΔH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在一定条件下,已知下列物质燃烧的热化学方程式为:
C(s)+O2(g)=CO2(g) ΔH= -393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH= -572kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH= -890kJ。mol-1。
在此条件下,下列叙述正确的是
C(s)+O2(g)=CO2(g) ΔH= -393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH= -572kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH= -890kJ。mol-1。
在此条件下,下列叙述正确的是
| A.C(s)+2H2(g)=CH4(g) ΔH= +75.5kJ·mol-1 |
| B.相同质量的H2和C充分燃烧时,H2放出的热量约等于C放出的热量的4.36倍 |
| C.1molH2(g)和1molCH4(g)燃烧共放热1462kJ |
| D.CH4(g)+O2(g)=C(s)+2H2O(g) ΔH= -1283.5kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=﹣Q1kJ•mol﹣1
2H2(g)+O2(g)=2H2O(g) ΔH2=﹣Q2kJ•mol﹣1
2H2(g)+O2(g)=2H2O(l) ΔH3=﹣Q3kJ•mol﹣1
现取体积比1∶4的甲烷和氢气的混合气体11.2 L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为( )
2H2(g)+O2(g)=2H2O(g) ΔH2=﹣Q2kJ•mol﹣1
2H2(g)+O2(g)=2H2O(l) ΔH3=﹣Q3kJ•mol﹣1
现取体积比1∶4的甲烷和氢气的混合气体11.2 L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为( )
| A.0.1Q1+0.2Q2 | B.0.1Q1+0.2Q3 | C.0.1Q1+0.4Q3 | D.0.1Q1+0.4Q2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,下列有关说法错误 的是
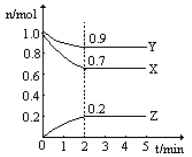

A.该反应的化学方程式为3X+Y  2Z 2Z |
| B.2 min时,反应达最大限度,但化学反应仍在进行 |
| C.反应开始至2 min,Z的反应速率为0.05 mol•L﹣1•min﹣1 |
| D.反应达到平衡时,压强是开始时的0.8倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知反应:A2(g)+2B2(g)  2AB2(g),下列说法正确的是
2AB2(g),下列说法正确的是
 2AB2(g),下列说法正确的是
2AB2(g),下列说法正确的是| A.升高温度正反应速率加快,逆反应速率减慢 |
| B.催化剂能同等程度改变正、逆反应速率 |
| C.达平衡后,正、逆反应速率均为零 |
| D.0.1molA2和0.2molB2反应达到平衡时生成0.2molAB2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】用NA表示阿伏加 德罗常数的值。下列叙述中不正确的是
| A.常温常压下62gP4中所含P-P键数目为3NA。 |
| B.0.1molH2和0.1molI2于密闭容器中充分反应后,其分子总数为0.2NA。 |
| C.1molFeI2与足量氯气反应时,转移的电子数为2NA。 |
| D.48g正丁烷和10g异丁烷的混合物中氢原子数目为10NA。 |
您最近一年使用:0次



