由废铁屑制Fe2O3的一种流程如图:下列说法错误的是( )
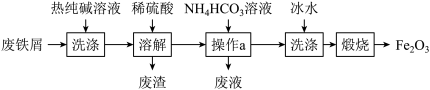

| A.废液中一定含有NH4+ |
| B.操作a是过滤 |
| C.冰水只有洗去杂质的作用 |
| D.Fe2O3俗名铁红,可用作红色颜料 |
19-20高三上·天津·期末 查看更多[2]
更新时间:2020-02-26 22:07:29
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某工业废水中含有大量的 、较多的
、较多的 和少量的
和少量的 。为减少污染并变废为宝,某实验小组设计了如下流程图制备
。为减少污染并变废为宝,某实验小组设计了如下流程图制备 并回收金属铜。下列说法不正确的是
并回收金属铜。下列说法不正确的是
 、较多的
、较多的 和少量的
和少量的 。为减少污染并变废为宝,某实验小组设计了如下流程图制备
。为减少污染并变废为宝,某实验小组设计了如下流程图制备 并回收金属铜。下列说法不正确的是
并回收金属铜。下列说法不正确的是 
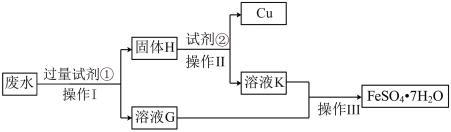
| A.试剂①为铁粉,试剂②为稀硫酸 |
| B.“溶液G”和“溶液K”的溶质组成均相同 |
| C.加入“试剂②”时,固体H部分溶解同时有气体生成 |
| D.进行“操作Ⅰ”和“操作Ⅱ”时,需要用到的玻璃仪器有烧杯、漏斗、玻璃棒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以废旧铅酸电池中的含铅废料(含Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料制备高纯PbO的工艺流程如图所示:
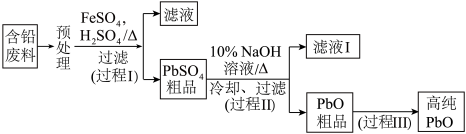
| A.预处理时可以将含铅废料进行粉碎,有利于加快反应速率 |
| B.滤液1的主要成分为Na2SO4 |
C.过程II的主反应离子方程式为 |
D.上述过程中可用 代替 代替 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】利用废铝箔(主要成分为Al,含少量Mg、Fe等)制明矾 的一种工艺流程如下:
的一种工艺流程如下:
 的一种工艺流程如下:
的一种工艺流程如下:
| A.①体现了铝能与碱溶液反应的性质 |
B.乙溶液中含有的离子主要为 |
| C.步骤②中,为了将铝元素完全沉淀,可改成加入过量的稀硫酸 |
D.由④可推测,室温下明矾的溶解度小于 和 和 的溶解度 的溶解度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列气体去除杂质的方法中,不能实现目的的是
| 气体(杂质) | 方法 | |
| A | 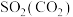 | 通过足量氢氧化钠溶液 |
| B | 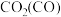 | 通过足量灼热的氧化铜 |
| C | 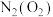 | 通过足量灼热的铜丝网 |
| D | 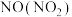 | 通过足量水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】CuI是有机合成的一种催化剂,受热易氧化。实验室可通过向CuSO4与NaI的混合溶液中通入SO2制备CuI(2CuSO4+2NaI+SO2+2H2O 2CuI↓+2H2SO4+Na2SO4)。下列实验原理和装置不能达到实验目的的是( )
2CuI↓+2H2SO4+Na2SO4)。下列实验原理和装置不能达到实验目的的是( )
 2CuI↓+2H2SO4+Na2SO4)。下列实验原理和装置不能达到实验目的的是( )
2CuI↓+2H2SO4+Na2SO4)。下列实验原理和装置不能达到实验目的的是( )A. 制备SO2 制备SO2 |
B.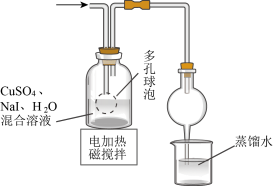 制备CuI并制备少量含SO2的溶液 制备CuI并制备少量含SO2的溶液 |
C.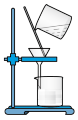 将CuI与母液分离并用装置制得的含SO2的溶液洗涤沉淀 将CuI与母液分离并用装置制得的含SO2的溶液洗涤沉淀 |
D. 加热干燥湿的CuI固体 加热干燥湿的CuI固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】氯化亚铜(CuCl)广泛应用于化工等行业,其难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺流程如图所示:
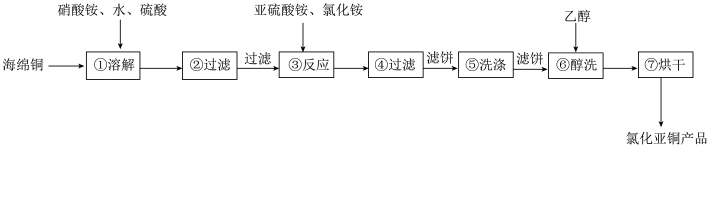
下列说法正确的是

下列说法正确的是
| A.步骤①,为加快海绵铜的溶解速度,可将其进行适当粉碎并用大火持续加热 |
| B.步骤③主要离子方程式:H2O+2Cu2++SO32-+2Cl-=CuCl↓+SO42-+2H+ |
| C.步骤⑤包括用pH=2的酸洗、水洗两步操作,为了防止CuCl被氧化,故不采用硝酸,而应采用硫酸或盐酸 |
| D.步骤⑥中醇洗主要目的是去除CuCl表面水分,但在步骤⑦中仍需要烘干,故节约成本可删除醇洗操作 |
您最近一年使用:0次

 ,并含少量的
,并含少量的 、
、 、
、 等)为原料制备氧化锌的工艺流程如图:
等)为原料制备氧化锌的工艺流程如图: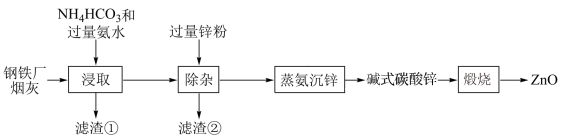
 、
、 。下列说法错误的是
。下列说法错误的是 代替氨水
代替氨水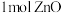 ,转移
,转移 电子
电子
 是由于其为单原子分子,是非极性分子
是由于其为单原子分子,是非极性分子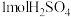 消耗
消耗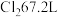 (标准状况)
(标准状况)


