某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
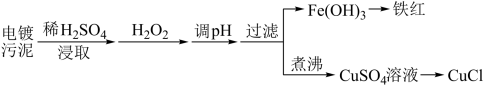
(1)酸浸后加入H2O2的目的是__ ,调pH的最适宜范围为__ 。
(2)调pH过程中加入的试剂最好是__ 。
A.NaOH B.CuO C.NH3·H2O D.Cu2(OH)2CO3
(3)煮沸CuSO4溶液的原因是__ 。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式__ 。
(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是__ 。
(5)称取所制备的CuCl样品0.2500g置于一定量的0.5mol﹒L-1FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol﹒L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数___ 。

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是
(2)调pH过程中加入的试剂最好是
A.NaOH B.CuO C.NH3·H2O D.Cu2(OH)2CO3
(3)煮沸CuSO4溶液的原因是
(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是
(5)称取所制备的CuCl样品0.2500g置于一定量的0.5mol﹒L-1FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol﹒L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数
更新时间:2020-03-01 16:56:46
|
相似题推荐
【推荐1】市政污泥含大量金属(Cu、Zn、Ni、Fe、Ag等),不经处理直接填埋会对环境造成严重的污染。市政污泥的综合利用能够使其得到科学、妥善的处置,并可以作为资源再次被我们利用,同时可以带来一定的经济价值。某科研团队利用市政污泥回收皓矾(ZnSO4·7H2O)的工艺流程如下:
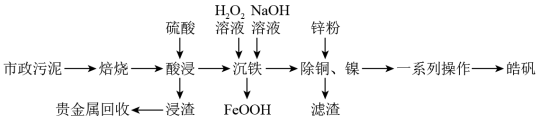
已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有___________ (任写一条)。
(2)“一系列操作”主要包括___________ 、___________ 、过滤、洗涤,干燥。
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为___________ 。
(4)“浸渣”中含有Ag2S,经一系列处理得Ag(NH3)2Cl(可溶于水,电离成[Ag(NH3)2]+和Cl-},用肼(N2H4)还原Ag(NH3)2Cl得到单质银,N2H4的氧化产物为N2,写出该反应的离子方程式:_______ ,则反应中氧化剂与还原剂的物质的量之比为_______ 。
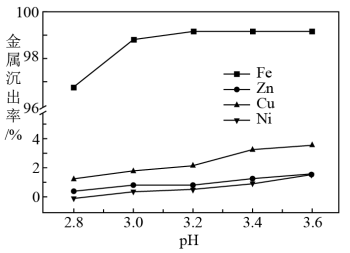
(5)浸出液中含有Fe2+,“沉铁”步骤中发生反应的离子方程式为_______ 。pH对不同金属沉出率的影响如图所示,则“沉铁’时最合理的pH约为_______ 。在pH<6时,Zn2+、Cu2+、Ni2+在溶液中以离子形式存在,但是有铁离子存在时,pH升高,Zn、Cu、Ni损失率均升高,原因可能是_______ 。

已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有
(2)“一系列操作”主要包括
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为
(4)“浸渣”中含有Ag2S,经一系列处理得Ag(NH3)2Cl(可溶于水,电离成[Ag(NH3)2]+和Cl-},用肼(N2H4)还原Ag(NH3)2Cl得到单质银,N2H4的氧化产物为N2,写出该反应的离子方程式:
(5)浸出液中含有Fe2+,“沉铁”步骤中发生反应的离子方程式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质) 制取七水合硫酸亚铁(FeSO4•7H2O)的流程如图:
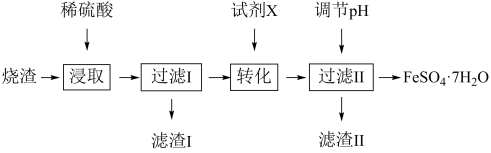
(1)FeO属于碱性氧化物,写出FeO与硫酸反应的化学方程式____________
(2)FeCl3可用于作净水剂,是因为其溶于水能形成Fe(OH)3胶体具有___ 性,FeCl3溶液中分散质粒子的直径______ (填“>”或“<”) m。
m。
(3)“转化”是为了将溶液中的Fe2(SO4)3转化为FeSO4。一种方法是向溶液中加入铁粉,铁粉与Fe2(SO4)3发生化合反应生成FeSO4,该反应的化学方程式是_______ ,该反应中化合价升高的元素是_____ ,化合价降低的元素是_____ 。另一种方法是向溶液中通入SO2,发生反应Fe2(SO4)3+SO2+2H2O=2FeSO4+2H2SO4,该反应属于_______ (填“氧化还原”或“非氧化还原”)反应。Fe2(SO4)3的电离方程式为_________ 。
(4)“过滤”所用到的玻璃仪器有__________ 。

(1)FeO属于碱性氧化物,写出FeO与硫酸反应的化学方程式
(2)FeCl3可用于作净水剂,是因为其溶于水能形成Fe(OH)3胶体具有
 m。
m。(3)“转化”是为了将溶液中的Fe2(SO4)3转化为FeSO4。一种方法是向溶液中加入铁粉,铁粉与Fe2(SO4)3发生化合反应生成FeSO4,该反应的化学方程式是
(4)“过滤”所用到的玻璃仪器有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】黄铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备高档颜料—铁红(Fe2O3)的流程如下:
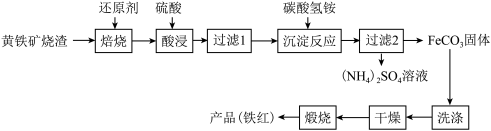
回答下列问题:
(1)“焙烧”时所添加的最佳还原剂是________ (填序号)。
a.焦炭 b.硫黄 c.镁粉 d.锌粉
(2)“过滤1”后的滤液中溶质的主要成分是________________ (填化学式)。
(3)“沉淀反应”时不宜混入过多空气,其原因为______________________ (用离子方程式表示)。
(4)为检验FeCO3是否洗涤干净,可以向最后一次洗涤液中滴加________ 溶液。
(5)在空气中煅烧FeCO3生成铁红和另一种氧化物,反应的化学方程式为________ 。
(6)现有黄铁矿烧渣500t,铁元素的质量分数为16.8%,经过一系列转化后,得到90t铁红,该产品的产率为________ 。(提示: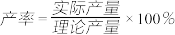 )
)

回答下列问题:
(1)“焙烧”时所添加的最佳还原剂是
a.焦炭 b.硫黄 c.镁粉 d.锌粉
(2)“过滤1”后的滤液中溶质的主要成分是
(3)“沉淀反应”时不宜混入过多空气,其原因为
(4)为检验FeCO3是否洗涤干净,可以向最后一次洗涤液中滴加
(5)在空气中煅烧FeCO3生成铁红和另一种氧化物,反应的化学方程式为
(6)现有黄铁矿烧渣500t,铁元素的质量分数为16.8%,经过一系列转化后,得到90t铁红,该产品的产率为
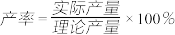 )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】海带中含有碘元素,从海带中提取碘的实验过程如下图。
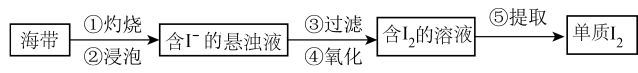
(1)步骤①一定不会用到下列仪器中的___________ 。
a.酒精灯 b.漏斗 c.坩埚
(2)步骤④选用的试剂为氯水,则该反应的离子方程式为___________ ;检验该步骤中有 生成的方法是
生成的方法是___________ 。
(3)步骤⑤包含以下四个过程。
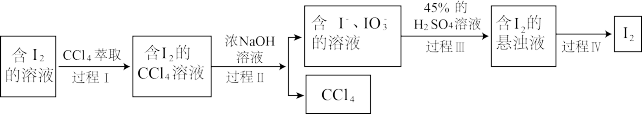
①过程Ⅰ使用的
___________ (填“能”或“不能”)用乙醇代替。
②过程Ⅱ中 与浓NaOH溶液反应的离子方程式为
与浓NaOH溶液反应的离子方程式为___________ 。
③过程Ⅲ中化合价发生变化的元素为___________ (填元素符号)。
④过程Ⅳ的操作名称为___________ 。

(1)步骤①一定不会用到下列仪器中的
a.酒精灯 b.漏斗 c.坩埚
(2)步骤④选用的试剂为氯水,则该反应的离子方程式为
 生成的方法是
生成的方法是(3)步骤⑤包含以下四个过程。

①过程Ⅰ使用的

②过程Ⅱ中
 与浓NaOH溶液反应的离子方程式为
与浓NaOH溶液反应的离子方程式为③过程Ⅲ中化合价发生变化的元素为
④过程Ⅳ的操作名称为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】回收废弃锂离子电池中的有价物质对工业可持续发展非常重要。利用 对废弃的锂离子电池正极材料
对废弃的锂离子电池正极材料 进行氯化处理并再生的一种工艺流程如图所示:
进行氯化处理并再生的一种工艺流程如图所示: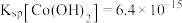
② 的溶解度曲线如图所示:
的溶解度曲线如图所示:
(1)“烧渣”是 、
、 利
利 的混合物,“氯化焙烧”时的化学方程式为
的混合物,“氯化焙烧”时的化学方程式为_______ 。
(2)常温下,“沉钻”过程中为了使 沉淀完全,溶液的
沉淀完全,溶液的 应该不低于
应该不低于_______ [已知: ,
, 时,可认为
时,可认为 沉淀完全]。
沉淀完全]。
(3)为提高 的析出量和纯度,“沉锂”后进行的操作依次为
的析出量和纯度,“沉锂”后进行的操作依次为_______ 、_______ 、洗涤、干燥。
(4)该工艺流程中可循环利用的物质有_______ (填化学式)。
(5)“煅烧”过程中生成 的化学方程式为
的化学方程式为_______ 。
(6)“焙烧”过程中固体残留率(固体残留率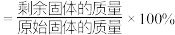 )随温度的变化如图1所示。为了获得纯净的
)随温度的变化如图1所示。为了获得纯净的 ,则该步骤应该控制的温度为_______(填字母)。
,则该步骤应该控制的温度为_______(填字母)。
(7) 晶体结构属于六方晶系,其晶体结构如图2所示,若阿伏加德罗常数的值为
晶体结构属于六方晶系,其晶体结构如图2所示,若阿伏加德罗常数的值为 ,
, 晶体的密度为
晶体的密度为_______  (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
 对废弃的锂离子电池正极材料
对废弃的锂离子电池正极材料 进行氯化处理并再生的一种工艺流程如图所示:
进行氯化处理并再生的一种工艺流程如图所示: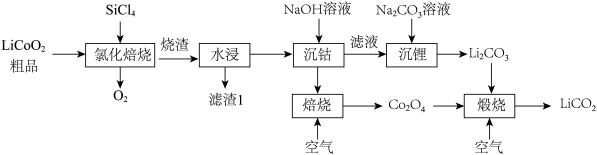
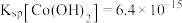
②
 的溶解度曲线如图所示:
的溶解度曲线如图所示: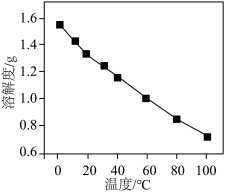
(1)“烧渣”是
 、
、 利
利 的混合物,“氯化焙烧”时的化学方程式为
的混合物,“氯化焙烧”时的化学方程式为(2)常温下,“沉钻”过程中为了使
 沉淀完全,溶液的
沉淀完全,溶液的 应该不低于
应该不低于 ,
, 时,可认为
时,可认为 沉淀完全]。
沉淀完全]。(3)为提高
 的析出量和纯度,“沉锂”后进行的操作依次为
的析出量和纯度,“沉锂”后进行的操作依次为(4)该工艺流程中可循环利用的物质有
(5)“煅烧”过程中生成
 的化学方程式为
的化学方程式为(6)“焙烧”过程中固体残留率(固体残留率
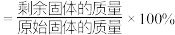 )随温度的变化如图1所示。为了获得纯净的
)随温度的变化如图1所示。为了获得纯净的 ,则该步骤应该控制的温度为_______(填字母)。
,则该步骤应该控制的温度为_______(填字母)。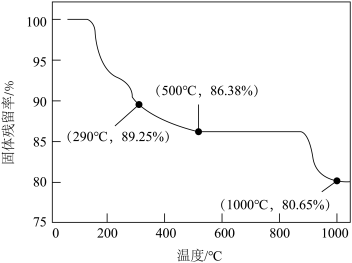
A.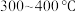 | B.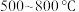 | C. | D. 以上 以上 |
(7)
 晶体结构属于六方晶系,其晶体结构如图2所示,若阿伏加德罗常数的值为
晶体结构属于六方晶系,其晶体结构如图2所示,若阿伏加德罗常数的值为 ,
, 晶体的密度为
晶体的密度为 (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。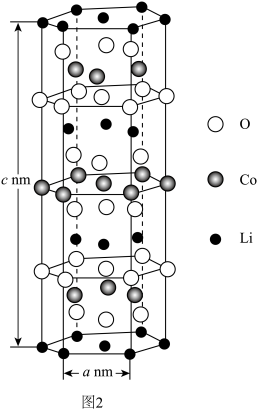
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】以橄榄石(主要成分是Mg9FeSi5O20)等为原料固定CO2并生产硅胶、碱式碳酸镁[Mg2(OH)2CO3]的部分工艺流程如图所示:
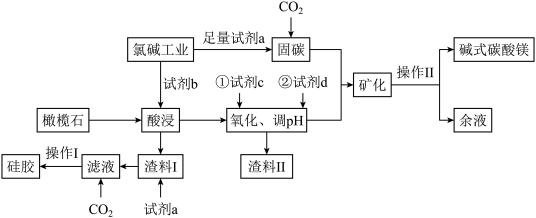
(1)Mg9FeSi5O20中铁的化合价为_ ,为提高镁的浸出率 ,可采取的两种主要措施是_ ,渣料Ⅱ的成分是___ 。
(2)若试剂c是氯碱工业中生成的某种气体 ,写出加入c后反应的离子方程式___ ,试剂d的用途是调节溶液pH ,其成分是____ ,余液中溶质的主要成分是___ 。
(3)操作Ⅰ的内容是___________ ,若固碳后溶液中的阴离子主要为CO ,写出生成碱式碳酸镁的离子方程式
,写出生成碱式碳酸镁的离子方程式____ 。

(1)Mg9FeSi5O20中铁的化合价为
(2)若试剂c是氯碱工业中生成的某种气体 ,写出加入c后反应的离子方程式
(3)操作Ⅰ的内容是
 ,写出生成碱式碳酸镁的离子方程式
,写出生成碱式碳酸镁的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度 ),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。

相关信息如下:
a.四氯化硅接触水会发生化学反应;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
请回答下列问题:
(1)写出装置A中发生反应的化学方程式___________ ,D中发生反应的化学方程式为___________ 。
(2)A中g管的作用是___________ ,装置C中的试剂是___________ ,作用是___________ 。
(3)过量的氯气可以用石灰乳来处理,请写出该反应的化学方程式___________ 。
 ),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
相关信息如下:
a.四氯化硅接触水会发生化学反应;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
| 物质 |  |  |  |  |  |
沸点 | 57.7 | 12.8 | - | 315 | - |
熔点 | 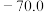 | 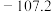 | - | - | - |
升华温度 | - | - | 180 | 300 | 162 |
(1)写出装置A中发生反应的化学方程式
(2)A中g管的作用是
(3)过量的氯气可以用石灰乳来处理,请写出该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
Ⅰ.工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO、SiO2等)制备绿矾 的流程如下:
的流程如下:
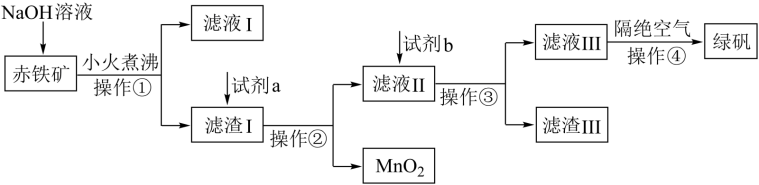
(1)滤液Ⅰ中的溶质除NaOH外还有_______ 。
(2)向滤渣Ⅰ中加入过量的试剂a为_______ ,试剂b要加入过量,试剂b为_______ 。
(3)操作④隔绝空气的目的是_______ 。
(4)操作①②③中所需的玻璃仪器是_______ 。
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比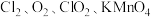 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为: ,该反应中Na2O2是
,该反应中Na2O2是_______ (填氧化剂、还原剂),Na2O2与 反应的化学反应方程式为
反应的化学反应方程式为_______ 。
(6)湿法制备高铁酸钾的反应体系中有六种微粒: 。
。
①碱性条件下,氧化剂和还原剂按物质的量之比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:_______ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为_______ mol。
Ⅰ.工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO、SiO2等)制备绿矾
 的流程如下:
的流程如下:
(1)滤液Ⅰ中的溶质除NaOH外还有
(2)向滤渣Ⅰ中加入过量的试剂a为
(3)操作④隔绝空气的目的是
(4)操作①②③中所需的玻璃仪器是
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比
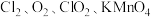 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。(5)干法制备高铁酸钠的主要反应为:
 ,该反应中Na2O2是
,该反应中Na2O2是 反应的化学反应方程式为
反应的化学反应方程式为(6)湿法制备高铁酸钾的反应体系中有六种微粒:
 。
。①碱性条件下,氧化剂和还原剂按物质的量之比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】钛(Ti)被称为继铁、铝之后的第三金属,钛白(TiO2)是目前使用最广泛的白色颜料。纳米TiO2是一种应用广泛的催化剂。制备TiO2和Ti的原料是钛铁矿,用含Fe2O3的钛铁矿(主要成分为FeTiO3)制备TiO2的流程如下:
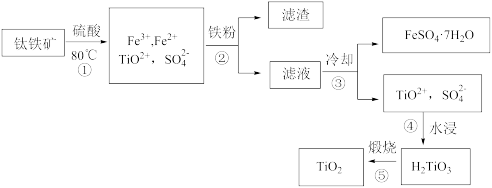
(1)S在元素周期表中的位置是_______
(2)步骤②加Fe的目的是(用离子方程式表示)________ ;步骤③冷却的目的是_____ 。
(3)步骤②③④中,均需用到的操作是________ 。煅烧操作中用到的主要仪器是__________ 。
(4)由TiO2制取单质钛(所加试剂均过量),涉及的步骤如下:
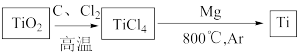
写出制备TiCl4的化学方程式_______ 。
(5)TiO2可用作甲烷燃料电池的催化剂载体,该电池以甲烷、空气、氢氧化钾溶液为原料,石墨为电极。写出负极上的电极反应式___________ 。

(1)S在元素周期表中的位置是
(2)步骤②加Fe的目的是(用离子方程式表示)
(3)步骤②③④中,均需用到的操作是
(4)由TiO2制取单质钛(所加试剂均过量),涉及的步骤如下:
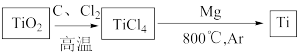
写出制备TiCl4的化学方程式
(5)TiO2可用作甲烷燃料电池的催化剂载体,该电池以甲烷、空气、氢氧化钾溶液为原料,石墨为电极。写出负极上的电极反应式
您最近一年使用:0次



