一定温度下,将3mol A和2.5mol B混合,充入2 L密闭容器中,发生反应: 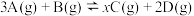 △H>0,经5秒钟反应达到平衡,生成1mol D,并测得C的浓度为0.5mol·L-1。下列有关叙述错误的是
△H>0,经5秒钟反应达到平衡,生成1mol D,并测得C的浓度为0.5mol·L-1。下列有关叙述错误的是
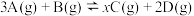 △H>0,经5秒钟反应达到平衡,生成1mol D,并测得C的浓度为0.5mol·L-1。下列有关叙述错误的是
△H>0,经5秒钟反应达到平衡,生成1mol D,并测得C的浓度为0.5mol·L-1。下列有关叙述错误的是| A.x的值为1 | B.平衡时A的浓度为0.75mol·L-1 |
| C.B的转化率为20% | D.反应速率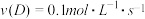 |
19-20高三下·贵州·阶段练习 查看更多[2]
更新时间:2020-03-10 08:23:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定条件下的合成氨反应: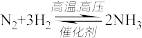 ,下列四个数据都表示合成氨的反应速率,其中表示的反应速率相同的是( )
,下列四个数据都表示合成氨的反应速率,其中表示的反应速率相同的是( )
①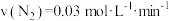 ②
②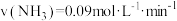
③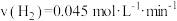 ④
④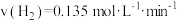
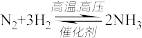 ,下列四个数据都表示合成氨的反应速率,其中表示的反应速率相同的是( )
,下列四个数据都表示合成氨的反应速率,其中表示的反应速率相同的是( )①
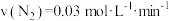 ②
②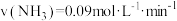
③
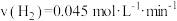 ④
④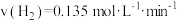
| A.①②③ | B.①③ | C.①②④ | D.②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某温度下,向1L恒容密闭容器中充入1.0molA和1.0molB,发生反应A(g)+B(g)  C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如下表:
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如下表:
下列说法正确的是
 C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如下表:
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如下表: | t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A.加入催化剂,平衡向正反应方向移动 |
| B.反应在前5s的平均速率v(B)=0.015mol/(L·s) |
| C.如果保持其他条件不变,升高温度,平衡时c(A)=0.81mol/L,则反应的△H﹤0 |
| D.相同温度下,起始时向容器中充入2.0molC,达到平衡时,A的物质的量为1.6mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】749K向2 L恒容真空密闭容器中充入CO和H2O各1 mol,发生反应
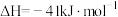 。已知:
。已知: ,
,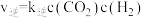 ,
, 、
、 为速率常数。测得CO的体积分数
为速率常数。测得CO的体积分数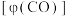 随时间(t)变化的关系如下表所示:
随时间(t)变化的关系如下表所示:
下列说法正确的是

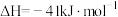 。已知:
。已知: ,
,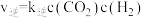 ,
, 、
、 为速率常数。测得CO的体积分数
为速率常数。测得CO的体积分数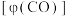 随时间(t)变化的关系如下表所示:
随时间(t)变化的关系如下表所示: | 0 | 20 | 40 | 60 | 80 |
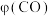 /% /% | 50 | 35 | 28 | 20 | 20 |
A.0~60 min内 |
B.749 K时,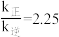 |
C.改变温度至T1时,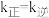 ,则 ,则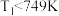 |
D.若保持绝热,60 min时,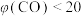 % % |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】利用工业废气中的CO2制备甲醇。该过程发生的主要反应如下:
反应I: CO2(g)+ 3H2(g)= CH3OH(g)+ H2O(g) △H1= - 49.4 kJ·mol-1
反应II: CO2(g)+ H2(g)= CO(g)+H2O(g)△H2=+41.1 kJ·mol-1
反应III: CO(g)+ 2H2(g)= CH3OH(g) △H3= -90.5 kJ·mol-1
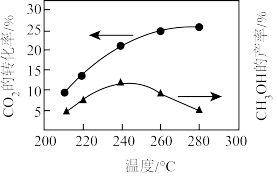
恒压条件下,将n(CO2):n(H2)为1 :3的混合气体以一定流速通过装有催化剂的反应管,在出口处测得CO2转化率、CH3OH产率[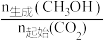 × 100%与温度的关系如图所示。
× 100%与温度的关系如图所示。
下列说法正确的是
反应I: CO2(g)+ 3H2(g)= CH3OH(g)+ H2O(g) △H1= - 49.4 kJ·mol-1
反应II: CO2(g)+ H2(g)= CO(g)+H2O(g)△H2=+41.1 kJ·mol-1
反应III: CO(g)+ 2H2(g)= CH3OH(g) △H3= -90.5 kJ·mol-1
恒压条件下,将n(CO2):n(H2)为1 :3的混合气体以一定流速通过装有催化剂的反应管,在出口处测得CO2转化率、CH3OH产率[
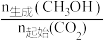 × 100%与温度的关系如图所示。
× 100%与温度的关系如图所示。
下列说法正确的是
A.反应I的平衡常数可表示为K=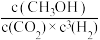 |
| B.反应3CO(g)+ 2H2O(g)= 2CO2(g)+ CH3OH(g)的△H= +172.7 kJ·mol-1 |
| C.240°C时,CH3OH产率最大,说明反应I、反应III已达到平衡状态 |
| D.提高CO2转化为CH3OH的转化率,可以研发在低温区高效的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】1molX气体跟a molY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g) bZ(g),反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
bZ(g),反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
 bZ(g),反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
bZ(g),反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是| A.a=1,b=3 | B.a=2,b=1 | C.a=2,b=2 | D.a=3,b=2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某反应体系前30min各物质的物质的量的浓度变化如图所示。下列说法正确的是
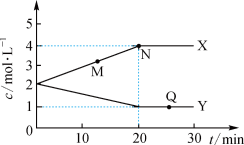

A.该反应的化学方程式为X Y Y |
| B.M点的正反应速率小于逆反应速率 |
| C.Q点正、逆反应速率相等,反应停止。 |
| D.前20min反应速率v(X)=0.1mol·L-1·min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备,正丁烷(C4H10)催化脱氢制1-丁烯(C4H8) 的化学方程式如下:C4H10(g)=C4H8(g)+ H2(g) △H,如图是该反应平衡转化率与反应温度及压强的关系图,下列说法正确的是
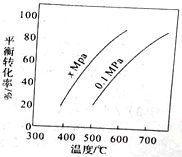

| A.x>0.1 |
| B.△H>O |
| C.500C时,压强xMPa比0.1MPa条件下的平衡常数大 |
| D.一定温度下,在一恒容密闭容器中发生该反应,C4H10的浓度越高,平衡转化率越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知: 2NO2(g)+ CH4(g) N2(g)+ CO2(g)+ 2H2O(g) ΔH,向容积为2L的恒容密闭容器中,充入NO2和CH4的混合气体0.3mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如右图所示。[投料比=
N2(g)+ CO2(g)+ 2H2O(g) ΔH,向容积为2L的恒容密闭容器中,充入NO2和CH4的混合气体0.3mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如右图所示。[投料比=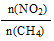 ] ;下列说法
] ;下列说法不正确 的是

 N2(g)+ CO2(g)+ 2H2O(g) ΔH,向容积为2L的恒容密闭容器中,充入NO2和CH4的混合气体0.3mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如右图所示。[投料比=
N2(g)+ CO2(g)+ 2H2O(g) ΔH,向容积为2L的恒容密闭容器中,充入NO2和CH4的混合气体0.3mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如右图所示。[投料比=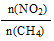 ] ;下列说法
] ;下列说法
| A.ΔH < 0 |
| B.X > 2 |
| C.400K时,反应的平衡常数为5×10-2 |
| D.投料比为2时,Q点v逆(CH4)小于P点的v逆(CH4) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2 O2+HbCO时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。下列结论不正确的是
O2+HbCO时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。下列结论不正确的是
 O2+HbCO时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。下列结论不正确的是
O2+HbCO时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。下列结论不正确的是A.CO与HbO2反应的平衡常数K=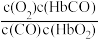 |
| B.当O2与CO浓度之比大于11000时,人的智力会受损 |
| C.人体吸入的CO越多,与血红蛋白结合的O2越少 |
| D.将CO中毒的病人放入高压氧舱中可以解毒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】氨和二氧化碳合成尿素的合成反应分两步进行:
第一步:2NH3(l)+CO2(g)⇌NH2COONH4 (l) △H1=﹣100.5 kJ·mol-1
第二步:NH2COONH4 (l)⇌CO(NH2)2(s)+H2O(l) △H2=﹢27.6 kJ·mol-1
下列说法中不正确 的是
第一步:2NH3(l)+CO2(g)⇌NH2COONH4 (l) △H1=﹣100.5 kJ·mol-1
第二步:NH2COONH4 (l)⇌CO(NH2)2(s)+H2O(l) △H2=﹢27.6 kJ·mol-1
下列说法中
| A.第一步反应随着温度的升高,平衡常数增大 |
| B.1 mol H2O和1 mol NH3中含有的质子数相等 |
| C.通入过量的CO2可提高NH3的转化率 |
| D.合成尿素的总的热化学方程式为:2NH3(l)+CO2(g)⇌CO(NH2)2(s)+H2O(l) △H=﹣72.9 kJ·mol-1 |
您最近一年使用:0次
【推荐2】 与
与 在催化剂表面生成
在催化剂表面生成 ,反应历程及能量变化示意如下。下列说法
,反应历程及能量变化示意如下。下列说法不正确 的是

 与
与 在催化剂表面生成
在催化剂表面生成 ,反应历程及能量变化示意如下。下列说法
,反应历程及能量变化示意如下。下列说法
| A.①→②吸收能量 | B.②→③形成了N-H键 |
| C.该反应为放热反应 | D.该催化剂可提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次



