由N、P、Ti等元素组成的新型材料有着广泛的用途,请回答下列问题。
(1)钛元素基态原子未成对电子数为__ 个,能量最高的电子占据的能级符号为___ 。
(2)磷的一种同素异形体—白磷(P4)的立体构型为__ ,推测其在CS2中的溶解度__ (填“大于”或“小于”)在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因:__ 。
(4)工业上制金属钛采用金属还原四氯化钛。先将TiO2(或天然的金红石)和足量炭粉混合加热至1000~1100K,进行氯化处理,生成TiCl4。写出生成TiCl4的化学反应方程式:___ 。
(5)有一种氮化钛晶体的晶胞如图所示,该晶体的化学式为__ ,已知晶体的密度为ρg·cm-3,阿伏加 德罗常数为NA,则晶胞边长为__ cm(用含ρ、NA的式子表示)。

(1)钛元素基态原子未成对电子数为
(2)磷的一种同素异形体—白磷(P4)的立体构型为
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因:
(4)工业上制金属钛采用金属还原四氯化钛。先将TiO2(或天然的金红石)和足量炭粉混合加热至1000~1100K,进行氯化处理,生成TiCl4。写出生成TiCl4的化学反应方程式:
(5)有一种氮化钛晶体的晶胞如图所示,该晶体的化学式为

更新时间:2020-03-15 11:59:00
|
相似题推荐
【推荐1】按要求回答下列问题:
(1)某元素原子的价电子排布式为3d14s2,元素符号为________ ,最高正化合价为________ 。
(2)原子序数为26的元素的原子中有________ 个能级,________ 个未成对电子,________ 种运动状态不同的电子,位于________ 族________ 区,该原子的原子结构示意图为________ 。
(3)请写出有2个能层且p轨道中只有一对成对电子的基态原子的外围电子排布图为________ ,其能量最高的电子的电子云在空间有________ 个方向,原子轨道呈________ 形。
(4)请写出次外层电子数是最外层电子数 的元素的基态原子的电子排布式:
的元素的基态原子的电子排布式:____________ 。
(5)1~36号元素原子核外电子排布中未成对电子数最多的元素名称是________ 。
(1)某元素原子的价电子排布式为3d14s2,元素符号为
(2)原子序数为26的元素的原子中有
(3)请写出有2个能层且p轨道中只有一对成对电子的基态原子的外围电子排布图为
(4)请写出次外层电子数是最外层电子数
 的元素的基态原子的电子排布式:
的元素的基态原子的电子排布式:(5)1~36号元素原子核外电子排布中未成对电子数最多的元素名称是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】(一)Na、Cu、O、Si、S、Cl是常见的六种元素.
(1)Na位于元素周期表第__ 周期第__ 族;S的基态原子核外有__ 个未成对电子;
Si的基态原子核外电子排布式为__ .
(2)用“>”或“<”填空:
(3)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取。写出该反应的离子方程式,并标出电子转移的方向和数目___
(二).某元素的原子序数为33,请回答:
(1)该元素原子核外有_______ 个电子层,______ 个能级,______ 个原子轨道。
(2)它的最外层电子排布式为____________ ,它的电子排布式为________ ,轨道表示式为_______________ 。
(1)Na位于元素周期表第
Si的基态原子核外电子排布式为
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si | O2- | NaCl | H2SO4 |
(二).某元素的原子序数为33,请回答:
(1)该元素原子核外有
(2)它的最外层电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)基态硫原子电子占据的最高能层符号为______ ,核外有______ 种能量不同的电子,硫原子核外电子有______ 种空间运动状态。
(2)与S同主族,位于第四周期的元素的符号是______ ,其价电子排布式为______
(3)已知有下列转化:
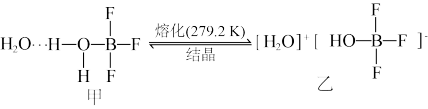
 的VSEPR模型为
的VSEPR模型为______ 。化合物乙中微粒间不存在的化学键有______ (填序号)。
A.离子键 B.共价键 C. 键 D.
键 D. 键 E.氢键
键 E.氢键
(4)相同条件下 与
与 分子在水中的溶解度较大的是
分子在水中的溶解度较大的是______ (写分子式),理由是______ 。 中的
中的 键角
键角______ (填“>”“<”或“=”) 中的
中的 键角。
键角。
(5)已知 是直线形分子,且有对称性,则
是直线形分子,且有对称性,则 分子的结构式为
分子的结构式为______ ,其中 键与
键与 键的个数比为
键的个数比为______ 。
(1)基态硫原子电子占据的最高能层符号为
(2)与S同主族,位于第四周期的元素的符号是
(3)已知有下列转化:
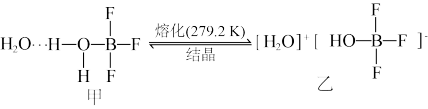
 的VSEPR模型为
的VSEPR模型为A.离子键 B.共价键 C.
 键 D.
键 D. 键 E.氢键
键 E.氢键(4)相同条件下
 与
与 分子在水中的溶解度较大的是
分子在水中的溶解度较大的是 中的
中的 键角
键角 中的
中的 键角。
键角。(5)已知
 是直线形分子,且有对称性,则
是直线形分子,且有对称性,则 分子的结构式为
分子的结构式为 键与
键与 键的个数比为
键的个数比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)钛在周期表中的位置________ ,Ti2+电子占据的最高能层的电子排布式为_________ 。
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO 的空间构型是
的空间构型是___________ ,第一电离能介于Al、P之间的第三周期元素为___________ (填元素符号)。
(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为___________ ,B原子的杂化方式是___________ ,其中的BH 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有___________ (填序号)
①σ键②π键③氢键④配位键⑤离子键
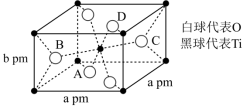
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为___________ g·cm-3(设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。
(1)钛在周期表中的位置
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO
 的空间构型是
的空间构型是(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为
 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有①σ键②π键③氢键④配位键⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】物质的光学性质在科研中有重要的用途。回答下列问题:
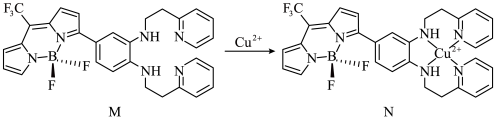
Ⅰ.一种比率光声探针M与Cu2+配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:___________ ,M中键角F-B-F___________  中键角F-B-F(填“>”、“<”或“=”);基态
中键角F-B-F(填“>”、“<”或“=”);基态 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为___________ 。
(2)均为平面结构的吡咯(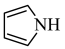 )和吡啶(
)和吡啶(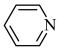 )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为___________ ,原因是___________ 。
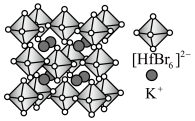
Ⅱ.铪(Hf)的卤化物八面体离子是构建卤化物钙钛矿的基本发光单元,其构建的某晶胞结构如图所示。 的配位数为
的配位数为___________ ,阴离子形成的八面体空隙有___________ 个。
(4)该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Hf-Hf最近距离为
,则Hf-Hf最近距离为___________ nm。
Ⅰ.一种比率光声探针M与Cu2+配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
 中键角F-B-F(填“>”、“<”或“=”);基态
中键角F-B-F(填“>”、“<”或“=”);基态 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为(2)均为平面结构的吡咯(
 )和吡啶(
)和吡啶( )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较大的为Ⅱ.铪(Hf)的卤化物八面体离子是构建卤化物钙钛矿的基本发光单元,其构建的某晶胞结构如图所示。
 的配位数为
的配位数为(4)该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Hf-Hf最近距离为
,则Hf-Hf最近距离为
您最近一年使用:0次
【推荐3】高温炼铜的反应之一为2CuFeS2+O2 Cu2S+2FeS+SO2。
Cu2S+2FeS+SO2。
(1) Cu+基态核外电子排布式为________________ 。
(2) Cu、Zn的第二电离能:I2(Cu)________ (填“>”“<”或“=”)I2(Zn)。
(3) SO2分子中S原子的轨道杂化类型为________ ,分子的空间构型为________ ,与SO2互为等电子体的分子有________ (写一种)。
(4) [Cu(CH3CN)4]+是非常稳定的络合离子,配体中σ键和π键个数之比为________ 。
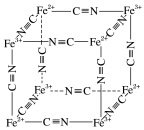
(5) Fe2+、Fe3+能与CN-络合,其结构如图所示。该离子可形成铁蓝钾盐,该钾盐的化学式为________ 。
 Cu2S+2FeS+SO2。
Cu2S+2FeS+SO2。(1) Cu+基态核外电子排布式为

(2) Cu、Zn的第二电离能:I2(Cu)
(3) SO2分子中S原子的轨道杂化类型为
(4) [Cu(CH3CN)4]+是非常稳定的络合离子,配体中σ键和π键个数之比为
(5) Fe2+、Fe3+能与CN-络合,其结构如图所示。该离子可形成铁蓝钾盐,该钾盐的化学式为
您最近一年使用:0次
【推荐1】已知A、B、C、D、E、F都是元素周期表前四周期的元素,它们的核电荷数:B<A<C<D<E<F。B、C两种元素都能引起水体富营养化。E原子得到一个电子后3p轨道全充满。A+比E原子形成的离子少1个电子层。D可以形成两种氧化物,其中一种氧化物是形成酸雨的主要气体之一。F的原子序数为26。请回答下列问题:
(1)C、D、E的第一电离能由小到大的顺序为________ (用元素符号表示)。
(2)写出B的氢化物与水反应的离子方程式:________________ ,B的氢化物极易溶于水的原因是____________________________________________________________ 。
(3)化合物BE3的分子空间构型为________________ 。
(4)F元素原子的核外电子排布式为________ 。F的一种常见化合物F(CO)5在常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,则F(CO)5的晶体类型为__________________ 。
(5)将FE3的饱和溶液滴入沸水中,请写出有关反应的离子方程式:___________________________ 。
(6)比较B、C两种元素的氢化物稳定性并说明理由:____________________ 。
(1)C、D、E的第一电离能由小到大的顺序为
(2)写出B的氢化物与水反应的离子方程式:
(3)化合物BE3的分子空间构型为
(4)F元素原子的核外电子排布式为
(5)将FE3的饱和溶液滴入沸水中,请写出有关反应的离子方程式:
(6)比较B、C两种元素的氢化物稳定性并说明理由:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】四氯化钛( )是制取航天工业材料——钛合金的重要原料。
)是制取航天工业材料——钛合金的重要原料。
实验室反应原理为 ,装置如下:
,装置如下:
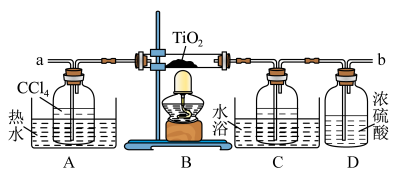
已知:有关物质的性质如下表:
请回答下列问题:
(1)A处水浴加热的目的是___________ ,C处水浴___________ (填“冷水”或“热水”)。
(2)D中浓硫酸的作用是___________ 。
(3) 与
与 互溶的原因是
互溶的原因是___________ 。
(4)从C处产物中分离出 的实验方法是
的实验方法是___________ 。
(5)本实验开始前要做两项工作是:
①___________ ;目的是___________ ,并简述如何进行___________ 。
②___________ ,目的是___________ ,并简述如何进行___________ 。
 )是制取航天工业材料——钛合金的重要原料。
)是制取航天工业材料——钛合金的重要原料。实验室反应原理为
 ,装置如下:
,装置如下:
已知:有关物质的性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
 | -23 | 76 | 与 互溶。 互溶。 |
 | -25 | 136 | 遇潮湿空气产生白雾,在550℃时能被氧气氧化。 |
(1)A处水浴加热的目的是
(2)D中浓硫酸的作用是
(3)
 与
与 互溶的原因是
互溶的原因是(4)从C处产物中分离出
 的实验方法是
的实验方法是(5)本实验开始前要做两项工作是:
①
②
您最近一年使用:0次
【推荐3】根据所学物质结构知识,请回答下列问题:
(1)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ四种类型,苏丹红Ⅰ的分子结构如图1所示。

苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在水中的溶解度会______ (填“增大”或“减小”),原因是______ 。
(2)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一种为绿色。两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液得到的白色沉淀质量为原紫色晶体的水溶液得到的沉淀质量的 。则绿色晶体配合物的化学式为
。则绿色晶体配合物的化学式为__ ,由Cl-形成的化学键类型是________ 。
(3)胆矾CuSO4•5H2O可写成[Cu(H2O)4]SO4•H2O,其结构示意图如图,有关它的说法正确的是_______ (填字母)。

A.该胆矾晶体中仅存在配位键、共价键
B.该结构中还存在金属键,极性共价键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(4)往硫酸铜溶液中逐渐滴加氨水至生成的沉淀恰好溶解,得到含有[Cu(NH3)4]2+配离子的深蓝色溶液。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_____ 。向制得的深蓝色溶液中加入______ ,将得到深蓝色晶体。
(1)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ四种类型,苏丹红Ⅰ的分子结构如图1所示。

苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在水中的溶解度会
(2)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一种为绿色。两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液得到的白色沉淀质量为原紫色晶体的水溶液得到的沉淀质量的
 。则绿色晶体配合物的化学式为
。则绿色晶体配合物的化学式为(3)胆矾CuSO4•5H2O可写成[Cu(H2O)4]SO4•H2O,其结构示意图如图,有关它的说法正确的是

A.该胆矾晶体中仅存在配位键、共价键
B.该结构中还存在金属键,极性共价键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(4)往硫酸铜溶液中逐渐滴加氨水至生成的沉淀恰好溶解,得到含有[Cu(NH3)4]2+配离子的深蓝色溶液。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
您最近一年使用:0次
【推荐1】钒和镍及其化合物是重要的合金材料和催化剂,其储氢合金可作为一种新型锌离子电池的负极材料,该电池以Zn(CF3SO3)2为电解质,以有缺陷的阳离子型ZnMn2O4为电极,成功获得了稳定的大功率电流。
(1)基态钒原子的价电子排布式为_______ ,其排布时能量最高的电子所占据能级的原子轨道有_______ 个伸展方向。
(2)VO2+与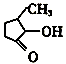 可形成配合物。
可形成配合物。 中,三种非金属元素的电负性由大到小的顺序为
中,三种非金属元素的电负性由大到小的顺序为_______ (用元素符号表示)。
(3)镍形成的配离子[Ni(NH3)6]2+、[Ni(CN)4]2-中,NH3分子的空间构型为_______ 。与CN-互为等电子体的一种分子的化学式为________ 。
(4) 三氟甲磺酸(CF3SO3H)是一种有机强酸,结构式如图1所示,通常以CS2、IF5、H2O2等为主要原料来制取。
①H2O2分子中O 原子的杂化方式为_______ 。
②三氟甲磺酸能与碘苯反应生成三氟甲磺酸苯酯和碘化氢。1个三氟甲磺酸苯酯分子中含有σ键的数目为_______ 。
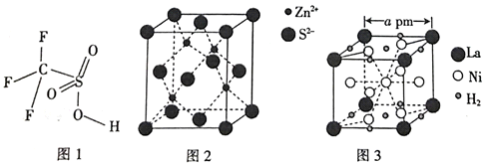
(5)硫化锌晶体的构型有多种,其中一种硫化锌的晶胞如图2 所示,该晶胞中S2-的配位数为_________ 。
(6)镧镍合金是重要的储氢材料,其储氢后的晶胞如图3所示。
①储氢前该镧镍合金的化学式为_________ 。
②该镧镍合金储氢后氢的密度为_________ (用NA表示阿伏伽德罗常数的数值)g/cm3。
(1)基态钒原子的价电子排布式为
(2)VO2+与
 可形成配合物。
可形成配合物。 中,三种非金属元素的电负性由大到小的顺序为
中,三种非金属元素的电负性由大到小的顺序为(3)镍形成的配离子[Ni(NH3)6]2+、[Ni(CN)4]2-中,NH3分子的空间构型为
(4) 三氟甲磺酸(CF3SO3H)是一种有机强酸,结构式如图1所示,通常以CS2、IF5、H2O2等为主要原料来制取。
①H2O2分子中O 原子的杂化方式为
②三氟甲磺酸能与碘苯反应生成三氟甲磺酸苯酯和碘化氢。1个三氟甲磺酸苯酯分子中含有σ键的数目为

(5)硫化锌晶体的构型有多种,其中一种硫化锌的晶胞如图2 所示,该晶胞中S2-的配位数为
(6)镧镍合金是重要的储氢材料,其储氢后的晶胞如图3所示。
①储氢前该镧镍合金的化学式为
②该镧镍合金储氢后氢的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】以 、
、 等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
(1)基态 原子的末成对电子有
原子的末成对电子有_______ 个。
(2) 、
、 等金属具有良好的导电性,从金属键的理论看,原因是
等金属具有良好的导电性,从金属键的理论看,原因是_______ 。
(3)邻苯二甲酸酐(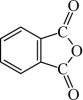 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺(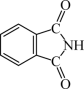 )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是_______ 。
(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为_______ 。
(5) 晶体中部分
晶体中部分 原子被
原子被 原子替代后可以改善半导体的性能,
原子替代后可以改善半导体的性能, 键中离子键成分的百分数小于
键中离子键成分的百分数小于 键,原因是
键,原因是_______ 。
(6)氧化亚铜的晶胞结构如下图所示,若最近的 与
与 的核间距为
的核间距为 ,则氧化亚铜晶体的密度是
,则氧化亚铜晶体的密度是_______  (
( 代表阿伏加德罗常数的值,列式即可)。
代表阿伏加德罗常数的值,列式即可)。

 、
、 等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:(1)基态
 原子的末成对电子有
原子的末成对电子有(2)
 、
、 等金属具有良好的导电性,从金属键的理论看,原因是
等金属具有良好的导电性,从金属键的理论看,原因是(3)邻苯二甲酸酐(
 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为
(5)
 晶体中部分
晶体中部分 原子被
原子被 原子替代后可以改善半导体的性能,
原子替代后可以改善半导体的性能, 键中离子键成分的百分数小于
键中离子键成分的百分数小于 键,原因是
键,原因是(6)氧化亚铜的晶胞结构如下图所示,若最近的
 与
与 的核间距为
的核间距为 ,则氧化亚铜晶体的密度是
,则氧化亚铜晶体的密度是 (
( 代表阿伏加德罗常数的值,列式即可)。
代表阿伏加德罗常数的值,列式即可)。
您最近一年使用:0次
【推荐3】在钢铁中添加有固定组成的铝铬合金颗粒,可以增强钢铁的耐腐蚀性、硬度和机械性能。
(1)钢铁中含有适量的碳元素。基态C原子中,核外存在___________ 对自旋相反的电子,电子占据最高能级的电子云轮廓图为___________ 形。
(2)实验测得FeCl3在蒸汽状态下实际存在形式为Fe2Cl6,其分子的球棍模型如图所示。

其中铁的配位数为___________ ;Fe2Cl6属于非极性分子的原因为___________ 。
(3)某铝铬合金的晶胞结构如图(1)所示,晶胞俯视图如图(2)所示,则该铝铬合金的化学式可表示为___________ ;若NA表示阿伏加德罗常数的值,则该晶体的密度为___________ g∙cm-3 (用含a、c和 的代数式表示)。
的代数式表示)。

(1)钢铁中含有适量的碳元素。基态C原子中,核外存在
(2)实验测得FeCl3在蒸汽状态下实际存在形式为Fe2Cl6,其分子的球棍模型如图所示。

其中铁的配位数为
(3)某铝铬合金的晶胞结构如图(1)所示,晶胞俯视图如图(2)所示,则该铝铬合金的化学式可表示为
 的代数式表示)。
的代数式表示)。
您最近一年使用:0次



