利用海洋资源可以获得很多物质 如从海水中可以得到食盐等许多化工原料,可以通过蒸馏获得淡水,从海洋植物中提取碘等.
如从海水中可以得到食盐等许多化工原料,可以通过蒸馏获得淡水,从海洋植物中提取碘等.
 一
一 从海水得到的粗盐中常含有杂质需要分离提纯,在除去悬浮物和泥沙之后,要用以下试剂①盐酸、②Na2CO3、③NaOH、④BaCl2来除去食盐水中的
从海水得到的粗盐中常含有杂质需要分离提纯,在除去悬浮物和泥沙之后,要用以下试剂①盐酸、②Na2CO3、③NaOH、④BaCl2来除去食盐水中的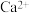 、
、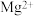 、
、 .
.
(1)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为______
a.先加NaOH,后加Na2CO3,再加BaCl2
b.先加NaOH,后加BaCl2,再加Na2CO3
C.先加BaCl2,后加NaOH,再加Na2CO3
(2)判断试剂BaCl2已经足量的方法是______________________ 。
 二
二 海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在 实验室里从海带中提取碘的流程如下:
实验室里从海带中提取碘的流程如下:
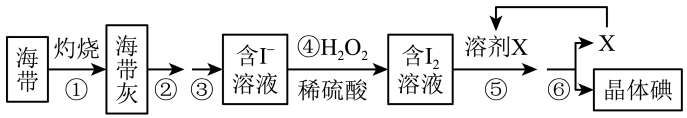
(1)实验时灼烧海带应在______________ (填仪器名称)内进行
(2)步骤④中反应的离子方程式是_______________________________ 。
(3)步骤⑤的实验操作为____________ ,应选用的一种溶剂X可以是_____________ 。
a.苯、酒精b.四氯化碳、苯c.汽油、酒精
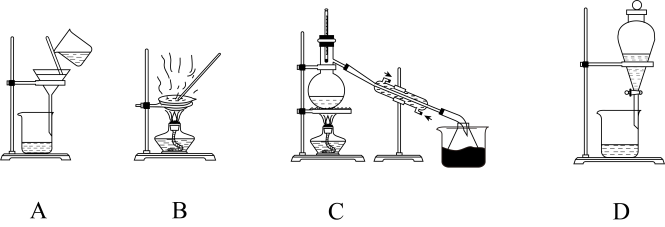
(4)步骤⑥的实验操作应选用如图中的______ 。
 如从海水中可以得到食盐等许多化工原料,可以通过蒸馏获得淡水,从海洋植物中提取碘等.
如从海水中可以得到食盐等许多化工原料,可以通过蒸馏获得淡水,从海洋植物中提取碘等. 一
一 从海水得到的粗盐中常含有杂质需要分离提纯,在除去悬浮物和泥沙之后,要用以下试剂①盐酸、②Na2CO3、③NaOH、④BaCl2来除去食盐水中的
从海水得到的粗盐中常含有杂质需要分离提纯,在除去悬浮物和泥沙之后,要用以下试剂①盐酸、②Na2CO3、③NaOH、④BaCl2来除去食盐水中的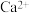 、
、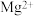 、
、 .
.(1)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为
a.先加NaOH,后加Na2CO3,再加BaCl2
b.先加NaOH,后加BaCl2,再加Na2CO3
C.先加BaCl2,后加NaOH,再加Na2CO3
(2)判断试剂BaCl2已经足量的方法是
 二
二 海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在 实验室里从海带中提取碘的流程如下:
实验室里从海带中提取碘的流程如下:
(1)实验时灼烧海带应在
(2)步骤④中反应的离子方程式是
(3)步骤⑤的实验操作为
a.苯、酒精b.四氯化碳、苯c.汽油、酒精
(4)步骤⑥的实验操作应选用如图中的

更新时间:2020/03/13 21:51:51
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
【推荐1】某研究小组制备纳米ZnO,再与金属有机框架(MOF)材料复合制备荧光材料ZnO@MOF,流程如图:
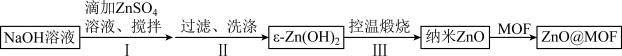
已知:①含锌组分间的转化关系:Zn2+ Zn(OH)2
Zn(OH)2

②ε−Zn(OH)2是Zn(OH)2的一种晶型,39℃ 以下稳定。
请回答:
(1)步骤I,初始滴入ZnSO4溶液时,反应的化学方程式___________ 。
(2)下列有关说法不正确的是___________ 。
A.步骤I,搅拌的作用是避免反应物浓度局部过高,使反应充分
B.步骤I,若将过量NaOH溶液滴入ZnSO4溶液制备ε−Zn(OH)2, 可提高ZnSO4的利用率
C.步骤Ⅱ,为了更好地除去杂质,可用50°C的热水洗涤
(3)步骤Ⅲ,控温煅烧的目的是___________ 。
(4)步骤Ⅲ中,实验室盛放样品的容器名称是___________ 。
(5)用(CH3COO)2Zn和过量(NH4)2CO3反应,得到的沉淀可直接控温煅烧得纳米ZnO,沉淀无需洗涤的原因是___________ 。
(6)为测定纳米ZnO产品的纯度,可用已知浓度的EDTA标准溶液滴定Zn2+。用________称量ZnO样品0.081g,在___________中用酸溶解样品,然后在________中配制一 定体积的Zn2+溶液,再用移液管量取一定体积的 Zn2+溶液,最后用滴定管盛装EDTA标准溶液,滴定Zn2+。从下列选项中选择合理的仪器___________ (按顺序填写且用字母作答)补全以上步骤。
仪器: a.烧杯 b.托盘天平 c.容量瓶 d.分析天平 e.试剂瓶
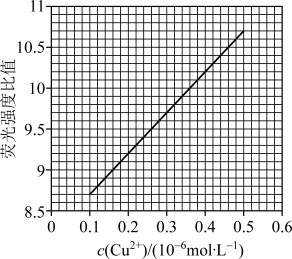
(7)制备的ZnO@MOF荧光材料可测Cu2+浓度。已知ZnO@MOF的荧光强度比值与Cu2+在一定浓度范围内的关系如图。某研究小组取7.5 ×10−3g人血浆铜蓝蛋白(相对分子质量为1.5 ×105),经预处理,将其中Cu元素全部转化为Cu2+并定容至1L。取样测得荧光强度比值为9.7,则1个人血浆铜蓝蛋白分子中含___________ 个铜原子。
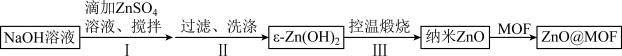
已知:①含锌组分间的转化关系:Zn2+
 Zn(OH)2
Zn(OH)2

②ε−Zn(OH)2是Zn(OH)2的一种晶型,39℃ 以下稳定。
请回答:
(1)步骤I,初始滴入ZnSO4溶液时,反应的化学方程式
(2)下列有关说法不正确的是
A.步骤I,搅拌的作用是避免反应物浓度局部过高,使反应充分
B.步骤I,若将过量NaOH溶液滴入ZnSO4溶液制备ε−Zn(OH)2, 可提高ZnSO4的利用率
C.步骤Ⅱ,为了更好地除去杂质,可用50°C的热水洗涤
(3)步骤Ⅲ,控温煅烧的目的是
(4)步骤Ⅲ中,实验室盛放样品的容器名称是
(5)用(CH3COO)2Zn和过量(NH4)2CO3反应,得到的沉淀可直接控温煅烧得纳米ZnO,沉淀无需洗涤的原因是
(6)为测定纳米ZnO产品的纯度,可用已知浓度的EDTA标准溶液滴定Zn2+。用________称量ZnO样品0.081g,在___________中用酸溶解样品,然后在________中配制一 定体积的Zn2+溶液,再用移液管量取一定体积的 Zn2+溶液,最后用滴定管盛装EDTA标准溶液,滴定Zn2+。从下列选项中选择合理的仪器
仪器: a.烧杯 b.托盘天平 c.容量瓶 d.分析天平 e.试剂瓶
(7)制备的ZnO@MOF荧光材料可测Cu2+浓度。已知ZnO@MOF的荧光强度比值与Cu2+在一定浓度范围内的关系如图。某研究小组取7.5 ×10−3g人血浆铜蓝蛋白(相对分子质量为1.5 ×105),经预处理,将其中Cu元素全部转化为Cu2+并定容至1L。取样测得荧光强度比值为9.7,则1个人血浆铜蓝蛋白分子中含

您最近一年使用:0次
【推荐2】某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属铜。请根据以下流程图,回答下列问题:

(1)⑥操作方法的名称是_______ ;操作⑨包括:蒸发浓缩、_______ 、过滤、洗涤、低温干燥。
(2)某兴趣小组同学欲鉴别④中的金属阳离子,设计如下实验:
甲同学取2.0mL④溶液,滴加氢氧化钠溶液,产生白色沉淀且很快变为灰绿色,最后变为红褐色沉淀,其中涉及氧化还原反应的化学方程式为_______ 。
乙同学取2.0mL④溶液,先加入几滴KSCN溶液,无明显现象,再加入几滴氯水,溶液变红,其中涉及氧化还原反应的离子方程式为_______ 。
(3)若按上述工艺处理1000L该工业废水,制得320g铜,则该工业废水中c(Cu2+)=_______ 。
(4)在Fe2(SO4)3溶液中,加入ag铜,完全溶解后,再加bg铁,充分反应后得到cg残余固体,且a>c。试分析残留固体的成分为________ (填元素符号,下同),所得溶液中阳离子为_______ 。

(1)⑥操作方法的名称是
(2)某兴趣小组同学欲鉴别④中的金属阳离子,设计如下实验:
甲同学取2.0mL④溶液,滴加氢氧化钠溶液,产生白色沉淀且很快变为灰绿色,最后变为红褐色沉淀,其中涉及氧化还原反应的化学方程式为
乙同学取2.0mL④溶液,先加入几滴KSCN溶液,无明显现象,再加入几滴氯水,溶液变红,其中涉及氧化还原反应的离子方程式为
(3)若按上述工艺处理1000L该工业废水,制得320g铜,则该工业废水中c(Cu2+)=
(4)在Fe2(SO4)3溶液中,加入ag铜,完全溶解后,再加bg铁,充分反应后得到cg残余固体,且a>c。试分析残留固体的成分为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子: 、Cu2+,化学小组设计了如图所示的方案对废液进行处理,以回收金属,保护环境。
、Cu2+,化学小组设计了如图所示的方案对废液进行处理,以回收金属,保护环境。
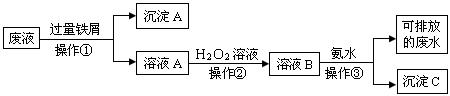
(1)操作①的名称是_______ 。加入铁屑先发生的离子反应为:_______
(2)沉淀A中含有的金属单质有_______ 。
(3)操作②中发生反应的离子方程式为_______ 。
(4)检验溶液B中含有的金属阳离子常用的试剂是_______ 。
(5)操作③中发生反应的离子方程式为_______ 。
 、Cu2+,化学小组设计了如图所示的方案对废液进行处理,以回收金属,保护环境。
、Cu2+,化学小组设计了如图所示的方案对废液进行处理,以回收金属,保护环境。
(1)操作①的名称是
(2)沉淀A中含有的金属单质有
(3)操作②中发生反应的离子方程式为
(4)检验溶液B中含有的金属阳离子常用的试剂是
(5)操作③中发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
(1)______ 分离饱和食盐水与沙子的混合物。
(2)______ 从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)______ 分离水和汽油的混合物。
(4)______ 从碘水中提取碘。
A.萃取分液 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
(1)
(2)
(3)
(4)
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】玫瑰精油被称为“液体黄金”是多种天然有机化合物的混合物,在食品,化妆品,医药,保健品等领域有重大的应用价值和经济价值。常见的玫瑰精油提取过程如下:
I.水蒸气提取法:
(1)第①步装置如下图所示。

在左侧炉中加入水。通过投料口将碾碎的玫瑰花加入,放在带孔隔板上。加热生成的水蒸气将玫瑰花中的精油带出。最终在收集瓶中得到油水混合物。将玫瑰花碾碎的意义是_______ ,水泵中的水应从_______ (填“甲”或“乙”)口流入
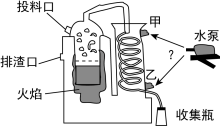
(2)第②步操作要用到的主要仪器是_______ 。
Ⅱ.萃取法

(3)步骤①用到酒精浸泡玫瑰花的原因是_______ ,步骤②的操作为_______ 。
(4)水蒸气提取法和萃取法各有优劣。你会选择哪种方法提取玫瑰精油?写出你选择的理由_______ 。
I.水蒸气提取法:
(1)第①步装置如下图所示。

在左侧炉中加入水。通过投料口将碾碎的玫瑰花加入,放在带孔隔板上。加热生成的水蒸气将玫瑰花中的精油带出。最终在收集瓶中得到油水混合物。将玫瑰花碾碎的意义是

(2)第②步操作要用到的主要仪器是
Ⅱ.萃取法

(3)步骤①用到酒精浸泡玫瑰花的原因是
(4)水蒸气提取法和萃取法各有优劣。你会选择哪种方法提取玫瑰精油?写出你选择的理由
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象。请回答:
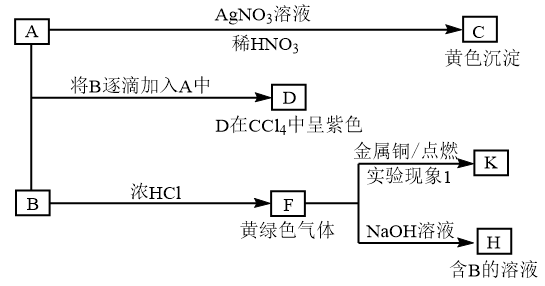
(1)写出C的化学式:____________ ,用文字描述实验现象1:______________________ 。
(2)依次写出B→F和F→H的化学方程式:_________________________________________________________ ; _________________________________________________________ 。
(3)A→D主要操作步骤如下图:
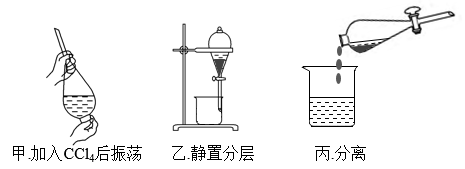
甲、乙、丙3步实验操作中,不正确 的是_______ (填“甲”、“乙”或“丙”)。
(4)将SO2气体通入D溶液,D溶液变为无色,生成两种酸。写出该反应的化学方程式:_____________________________________ 。

(1)写出C的化学式:
(2)依次写出B→F和F→H的化学方程式:
(3)A→D主要操作步骤如下图:

甲、乙、丙3步实验操作中,
(4)将SO2气体通入D溶液,D溶液变为无色,生成两种酸。写出该反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】高氯酸钠可用于制备高氯酸。以精制盐水等为原料制备高氯酸钠晶体(NaClO4·H2O)的流程如图:
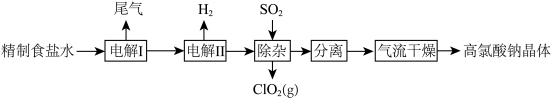
(1)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为______ 。
A.先加NaOH,后加Na2CO3,再加钡试剂
B.先加NaOH,后加钡试剂,再加Na2CO3
C.先加钡试剂,后加NaOH,再加Na2CO3
除去盐水中的Br-可以节省电解过程中的电能,其原因是_____ 。
(2)“电解Ⅰ”的目的是制备NaClO3溶液,产生的尾气除H2外,还含有_____ (填化学式)。“电解Ⅱ”的化学方程式为____ 。
(3)“除杂”的目的是除去少量的未反应的NaClO3杂质,该反应的离子方程式为_____ 。“气流干燥”时,温度控制在80~100℃,温度不能过高的原因是_____ 。

(1)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为
A.先加NaOH,后加Na2CO3,再加钡试剂
B.先加NaOH,后加钡试剂,再加Na2CO3
C.先加钡试剂,后加NaOH,再加Na2CO3
除去盐水中的Br-可以节省电解过程中的电能,其原因是
(2)“电解Ⅰ”的目的是制备NaClO3溶液,产生的尾气除H2外,还含有
(3)“除杂”的目的是除去少量的未反应的NaClO3杂质,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】海洋是一个巨大的化学资源宝库,请回答下列问题:
Ⅰ.下面是海水资源综合利用的部分流程图:
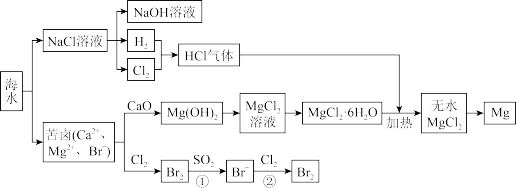
(1)由无水 MgCl2制取金属镁的常用工业方法是_______ (用化学方程式表示)。
(2)步骤①已经获得 Br2,步骤②又将 Br2还原为 Br-,其目的是_______ 。写出步骤②反应的离子方程式_______ 。由海水提溴过程中的反应可得出 Cl-、SO2、Br-还原性由强到弱的顺序是_______ 。
Ⅱ.海带灰中富含以 I-形式存在的碘元素。实验室提取 I2的途径如图所示:
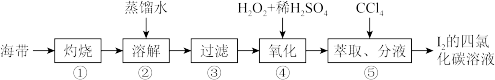
(3)灼烧海带至灰烬时所用的主要仪器名称是_______ 。
(4)向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式_______ 。反应结束后再加入 CCl4作萃取剂,振荡、静置,可以观察到 CCl4层呈_______ 色。
Ⅰ.下面是海水资源综合利用的部分流程图:

(1)由无水 MgCl2制取金属镁的常用工业方法是
(2)步骤①已经获得 Br2,步骤②又将 Br2还原为 Br-,其目的是
Ⅱ.海带灰中富含以 I-形式存在的碘元素。实验室提取 I2的途径如图所示:

(3)灼烧海带至灰烬时所用的主要仪器名称是
(4)向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】利用海水可以提取溴和镁,提取过程如图。
I
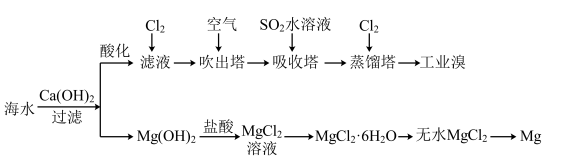
(1)提取溴的过程中,经过两次Br-→Br2转化的目的是______ ,吸收塔中发生反应的离子方程式是__________ 。
(2)从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作是____ 、浓缩、冷却、______ 、过滤、洗涤、干燥。
II以食盐为原料进行生产并综合利用的某些过程如图所示。

(1)除去粗盐中的Ca2+、Mg2+和SO 离子,加入下列沉淀剂的顺序是(填序号)
离子,加入下列沉淀剂的顺序是(填序号)____ 。
a.BaCl2 b.Na2CO3
(2)NaHCO3制取Na2CO3化学方程式是_____ 。
(3)将滤液的pH调至酸性除去的离子是______ 。
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式是_____ 。
(5)工业上,可以用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是_______ 。(已知碳酸的酸性强于次氯酸)。
I

(1)提取溴的过程中,经过两次Br-→Br2转化的目的是
(2)从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作是
II以食盐为原料进行生产并综合利用的某些过程如图所示。

(1)除去粗盐中的Ca2+、Mg2+和SO
 离子,加入下列沉淀剂的顺序是(填序号)
离子,加入下列沉淀剂的顺序是(填序号)a.BaCl2 b.Na2CO3
(2)NaHCO3制取Na2CO3化学方程式是
(3)将滤液的pH调至酸性除去的离子是
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式是
(5)工业上,可以用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是
您最近一年使用:0次
【推荐1】海带中含有碘元素,从海带中提取碘并验证其性质。提取过程如图所示:
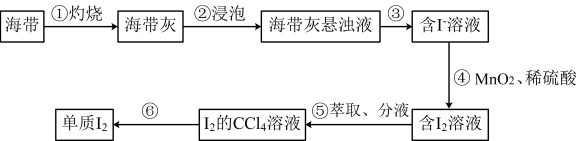
(1)验证“含 溶液”和“含
溶液”和“含 溶液”中含有的
溶液”中含有的 和
和 所需的试剂分别是
所需的试剂分别是______ 和_______ 。
(2)步骤④的反应中 被还原为
被还原为 ,反应的离子方程式为
,反应的离子方程式为__________ ; 、稀硫酸可用
、稀硫酸可用_______ 代替。
a. b.
b. c.
c. 、稀硫酸 d.
、稀硫酸 d.
(3)海带灰中含有的可溶性硫酸盐、碳酸盐等,在实验步骤___________ (填序号)中实现与碘分离。
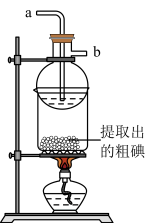
(4)某同学制得的粗碘中含有少量 ,对粗碘进行提纯的装置如图所示,采用的分离方法是
,对粗碘进行提纯的装置如图所示,采用的分离方法是________ ;a、b为冷凝水进出口,其中__________ (填“a”或“b”)接水龙头,最终能得到较多较高纯度的单质碘。

(1)验证“含
 溶液”和“含
溶液”和“含 溶液”中含有的
溶液”中含有的 和
和 所需的试剂分别是
所需的试剂分别是(2)步骤④的反应中
 被还原为
被还原为 ,反应的离子方程式为
,反应的离子方程式为 、稀硫酸可用
、稀硫酸可用a.
 b.
b. c.
c. 、稀硫酸 d.
、稀硫酸 d.
(3)海带灰中含有的可溶性硫酸盐、碳酸盐等,在实验步骤
(4)某同学制得的粗碘中含有少量
 ,对粗碘进行提纯的装置如图所示,采用的分离方法是
,对粗碘进行提纯的装置如图所示,采用的分离方法是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】以下海带提碘的实验方案可以缩短实验时间,避免氯气和四氯化碳的毒性。实验流程如下:
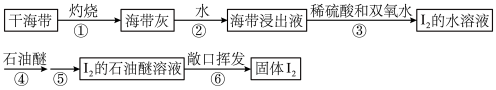
(1)步骤①所需的主要仪器有玻璃棒、______ 和______ 。
(2)步骤③中加入双氧水后发生反应的化学方程式为_________ ;选择用双氧水做氧化剂的因是________ 。
(3)检验I2的水溶液中含有单质碘的方法是取样于试管中,加入____ ,如溶液显___ 色,则可证明含有碘单质。
(4)步骤④的操作名称是_____ ;石油醚能提取碘水中的碘,说明石油醚具有的性质是________ 。
(5)步骤⑥通过敞口挥发就能得到固体碘,说明石油醚具有良好的______ 性。

(1)步骤①所需的主要仪器有玻璃棒、
(2)步骤③中加入双氧水后发生反应的化学方程式为
(3)检验I2的水溶液中含有单质碘的方法是取样于试管中,加入
(4)步骤④的操作名称是
(5)步骤⑥通过敞口挥发就能得到固体碘,说明石油醚具有良好的
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
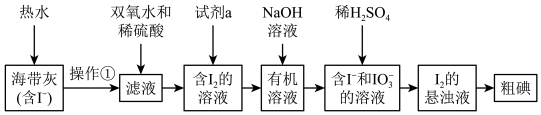
【推荐3】海洋是一个巨大的资源宝库。在海洋中生长的海带,富含碘元素。某同学设计以下实验方案,从海带中提取 。
。___________ 。
(2)如将加双氧水改为加二氧化锰也可达到实验目的,写出向滤液中加入 和稀硫酸发生反应的离子方程式:
和稀硫酸发生反应的离子方程式:___________ 。
(3)试剂a可以是___________ 。
(4)I-和 生成I2的离子方程式是
生成I2的离子方程式是___________ 。
(5)上图中,含I2的溶液经3步转化为I2的悬浊液,其目的是___________ 。
(6)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:___________ 。
 。
。
(2)如将加双氧水改为加二氧化锰也可达到实验目的,写出向滤液中加入
 和稀硫酸发生反应的离子方程式:
和稀硫酸发生反应的离子方程式:(3)试剂a可以是
(4)I-和
 生成I2的离子方程式是
生成I2的离子方程式是(5)上图中,含I2的溶液经3步转化为I2的悬浊液,其目的是
(6)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:
您最近一年使用:0次



