硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3、MgO、CaO等,生产工艺流程示意如下:
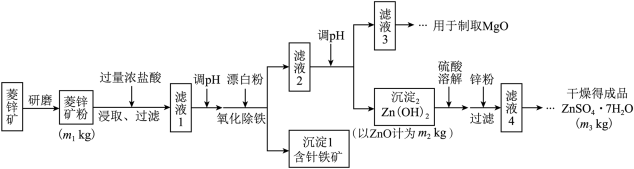
(1)将菱锌矿研磨成粉的目的是_______________________ 。
(2)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是______________ 。
(3)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为________________
工业上从“滤液3”制取MgO过程中,最合适的反应物是______________ (选填序号)。
A、大理石粉 B、石灰乳 C、纯碱溶液 D、烧碱溶液
“滤液4”之后的操作依次为______ 、_______ 、过滤,洗涤,干燥。
(4)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________ 。

(1)将菱锌矿研磨成粉的目的是
(2)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是
(3)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为
| Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
| 开始沉淀的pH | 10.4 | 6.4 | — | — |
| 沉淀完全的pH | 12.4 | 8.0 | — | — |
| 开始溶解的pH | — | 10.5 | — | — |
工业上从“滤液3”制取MgO过程中,最合适的反应物是
A、大理石粉 B、石灰乳 C、纯碱溶液 D、烧碱溶液
“滤液4”之后的操作依次为
(4)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于
更新时间:2020-03-21 12:53:21
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(FeSO4‧7H2O),再通过绿矾制备铁黄 [FeO(OH)]的流程如下:
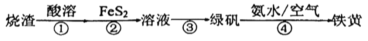
已知:步骤②涉及的离子反应为: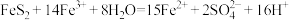
(1)步骤①中溶解烧渣的酸宜选用_______ (填“盐酸、硫酸或硝酸”)。
(2)步骤②中,每消耗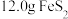 ,转移电子的物质的量为
,转移电子的物质的量为_______ mol。
(3)步骤②中, 可以用
可以用_______ 代替。
(4)步骤④中,若氨水浓度过大会使铁黄中混有_______ 杂质。
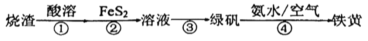
已知:步骤②涉及的离子反应为:
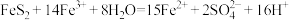
(1)步骤①中溶解烧渣的酸宜选用
(2)步骤②中,每消耗
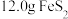 ,转移电子的物质的量为
,转移电子的物质的量为(3)步骤②中,
 可以用
可以用(4)步骤④中,若氨水浓度过大会使铁黄中混有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】废电池的锌皮(含铁单质)上常粘有ZnCl2、NH4Cl、MnO2及石蜡。工业上利用废旧锌皮制备水合硫酸锌(ZnSO4·nH2O)的流程如下:

已知:常温下,金属离子开始沉淀及完全沉淀的pH如下表所示:
通常认为溶液中离子浓度≤10-5mol·L-1为沉淀完全。请回答下列问题:
(1)“溶解”工序中除去废旧锌皮上物质的名称为_______ 。
(2)滤渣I的主要成分为_______ (填化学式)。“氧化”工序中发生反应的离子方程式为_______ 。
(3)加入NaOH溶液调pH=8后,所得沉淀应用蒸馏水进行洗涤直至滤液中不再含有Cl-,检验洗涤液中是否还含有Cl-的实验操作为_______ 。
(4)加入稀硫酸调pH时,a的取值范围为_______ 。常温下,Ksp[(Zn(OH)2]和Ksp[Fe(OH)2]中数值更小的是_______ ,其数值为_______ 。
(5)ZnSO4·nH2O失去5个结晶水时,失重率约为31.35%,则n的值为_______ 。

已知:常温下,金属离子开始沉淀及完全沉淀的pH如下表所示:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe2+ | 7.5 | 9.0 |
| Zn2+ | 6.5 | 8.0 |
| Fe3+ | 2.2 | 3.5 |
通常认为溶液中离子浓度≤10-5mol·L-1为沉淀完全。请回答下列问题:
(1)“溶解”工序中除去废旧锌皮上物质的名称为
(2)滤渣I的主要成分为
(3)加入NaOH溶液调pH=8后,所得沉淀应用蒸馏水进行洗涤直至滤液中不再含有Cl-,检验洗涤液中是否还含有Cl-的实验操作为
(4)加入稀硫酸调pH时,a的取值范围为
(5)ZnSO4·nH2O失去5个结晶水时,失重率约为31.35%,则n的值为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铁及其化合物与我们的生活生产息息相关。
(1)纳米铁粉可用于处理废水中的 :酸性条件下,纳米铁粉与废水中
:酸性条件下,纳米铁粉与废水中 反应生成Fe2+与
反应生成Fe2+与 ,其反应的离子方程式是
,其反应的离子方程式是_______ 。
(2)以硫铁矿(主要成分为FeS2)为原料制备硫酸亚铁晶体(FeSO4·7H2O)的工艺流程如下:

①焙烧所得矿渣的成分为Fe2O3、Fe3O4和SiO2,写出酸溶时Fe2O3发生反应的化学方程式:_______ 。
②酸溶时,若其他条件不变,下列措施中能提高单位时间内铁元素溶出率的有_______ 。
A.适当减小硫酸浓度 B.适当加快搅拌速率 C.将焙烧所得的矿渣粉碎
③加入铁粉的目的是_______ (用离子方程式表达)。
④检验母液中是否含有Fe3+的试剂是_______ (填化学式)。
⑤操作1为_______ 、_______ ,过滤。
⑥若FeS2焙烧时只生成Fe2O3和SO2,理论上消耗的n(FeS2):n(O2)=_______ 。
(1)纳米铁粉可用于处理废水中的
 :酸性条件下,纳米铁粉与废水中
:酸性条件下,纳米铁粉与废水中 反应生成Fe2+与
反应生成Fe2+与 ,其反应的离子方程式是
,其反应的离子方程式是(2)以硫铁矿(主要成分为FeS2)为原料制备硫酸亚铁晶体(FeSO4·7H2O)的工艺流程如下:

①焙烧所得矿渣的成分为Fe2O3、Fe3O4和SiO2,写出酸溶时Fe2O3发生反应的化学方程式:
②酸溶时,若其他条件不变,下列措施中能提高单位时间内铁元素溶出率的有
A.适当减小硫酸浓度 B.适当加快搅拌速率 C.将焙烧所得的矿渣粉碎
③加入铁粉的目的是
④检验母液中是否含有Fe3+的试剂是
⑤操作1为
⑥若FeS2焙烧时只生成Fe2O3和SO2,理论上消耗的n(FeS2):n(O2)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某研究小组利用软锰矿(主要成分为MnO2,另含有少量铝、铜、镍、硅的氧化物)作脱硫剂,通过如图简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2 (反应条件已省略)。请回答下列问题:

(1)步骤Ⅰ过滤得到的滤渣是________ (填化学式)。
(2)写出软锰矿浆吸收SO2的主要反应的离子方程式:________________ 。
(3)步骤Ⅱ加入MnCO3的目的是________________ 。
(4)步骤Ⅲ加入MnS的目的是除去Ni2+、Cu2+,加入MnS优点是________________ 。
(5)写出步骤Ⅳ中KMnO4与MnSO4溶液反应的离子方程式:________________ 。
(6)已知:Ksp(MnCO3)=2.2×10-11,请用化学用语表示MnCO3饱和溶液中存在的沉溶平衡:___________ 。当体系中Mn2+恰好沉淀完全时,溶液中碳酸根离子浓度为:________ 。

(1)步骤Ⅰ过滤得到的滤渣是
(2)写出软锰矿浆吸收SO2的主要反应的离子方程式:
(3)步骤Ⅱ加入MnCO3的目的是
(4)步骤Ⅲ加入MnS的目的是除去Ni2+、Cu2+,加入MnS优点是
(5)写出步骤Ⅳ中KMnO4与MnSO4溶液反应的离子方程式:
(6)已知:Ksp(MnCO3)=2.2×10-11,请用化学用语表示MnCO3饱和溶液中存在的沉溶平衡:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】 可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为
可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为 ,含
,含 、
、 、
、 等杂质)为原料生产
等杂质)为原料生产 和金属Al的工艺流程如图。
和金属Al的工艺流程如图。

已知:
I.“焙烧”过程中,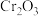 反应转化为
反应转化为
Ⅱ.若溶液中相关离子的物质的量浓度为c,则常温时,lgc与溶液pH的关系如图所示。
Ⅲ.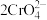 (黄色)
(黄色) (橙色)
(橙色)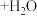
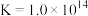 。
。
回答下列问题:

(1)“焙烧”时, 发生反应的化学方程式为
发生反应的化学方程式为__________ 。
(2)“水浸”后滤渣主要成分为__________ (填化学式);“调pH”时通入的“气体X”是__________ 。
(3)常温下,图像上M点对应的溶液
__________ 。
(4)用稀硫酸进行“酸浸”,调节溶液pH的最大值为__________  。“沉铝”后的母液Ⅱ的主要成分为
。“沉铝”后的母液Ⅱ的主要成分为__________ 。
(5)加入 “析铬”时,
“析铬”时, 被还原的离子方程式为
被还原的离子方程式为__________ 。
 可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为
可用于油漆颜料及羊毛处理。工业上以高铁铬铁矿(主要成分为 ,含
,含 、
、 、
、 等杂质)为原料生产
等杂质)为原料生产 和金属Al的工艺流程如图。
和金属Al的工艺流程如图。
已知:
I.“焙烧”过程中,
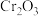 反应转化为
反应转化为
Ⅱ.若溶液中相关离子的物质的量浓度为c,则常温时,lgc与溶液pH的关系如图所示。
Ⅲ.
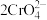 (黄色)
(黄色) (橙色)
(橙色)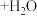
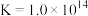 。
。回答下列问题:

(1)“焙烧”时,
 发生反应的化学方程式为
发生反应的化学方程式为(2)“水浸”后滤渣主要成分为
(3)常温下,图像上M点对应的溶液

(4)用稀硫酸进行“酸浸”,调节溶液pH的最大值为
 。“沉铝”后的母液Ⅱ的主要成分为
。“沉铝”后的母液Ⅱ的主要成分为(5)加入
 “析铬”时,
“析铬”时, 被还原的离子方程式为
被还原的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】钛酸钡(BaTiO3)具有优良的铁电,压电和绝缘性能,在电子陶瓷中使用广泛。某兴趣小组设计方案在实验室里制备钛酸钡并测定其纯度,制备简易流程如下:

已知:室温下,TiCl4为无色液体,易挥发。
(1)“共沉”在如图装置中完成,仪器A的进水口是___________ (填“a”或“b”):仪器B的名称是___________ ;“共沉”时反应的化学方程式为___________

(2)“减压过滤”如图装置,减压的目的是___________

(3)在实验室中研细固体一般使用仪器名称是___________ ,煅烧”时反应的化学方程式为___________
(4)产品纯度与“共沉”反应时间和“煅烧”时间的关系如下图所示,你认为最佳“共沉”反应时间和“煅烧”时间分别为___________ h、___________ h。


已知:室温下,TiCl4为无色液体,易挥发。
(1)“共沉”在如图装置中完成,仪器A的进水口是

(2)“减压过滤”如图装置,减压的目的是

(3)在实验室中研细固体一般使用仪器名称是
(4)产品纯度与“共沉”反应时间和“煅烧”时间的关系如下图所示,你认为最佳“共沉”反应时间和“煅烧”时间分别为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】I.以黄铁矿(主要成分为FeS2)为原料制备绿矾晶体(FeSO4•7H2O)的工艺流程如图:

回答下列问题:
(1)焙烧时黄铁矿要粉碎,其目的是_____ 。
(2)SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式_____ 。
(3)从还原得到的溶液中获得硫酸亚铁晶体(FeSO4•7H2O)的操作:_____ 、_____ 、过滤、洗涤、干燥。
II.作为推行“低碳经济”的重要科技进步,太阳能光伏发电成为重要的新型能源。太阳能光伏发电最关键的材料是高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅(Si)的主要方法,生产流程示意如图:

(4)石英砂的主要成分是SiO2,SiO2是_____ (酸性氧化物或碱性氧化物)。
(5) “精馏”也是蒸馏的一种形式,通过蒸馏可把液体混合物分离开,原理是利用混合物各成分的_____ (填“熔点”或“沸点”)不同。
(6)整个制备过程必须达到无水无氧,在H2还原SiHCl3过程中若混入O2,除了生成SiO2外,还可能引起的后果是_____ 。
(7)为达到绿色化学和资源综合利用的目的,在生产过程中物质A需要循环使用,A的化学式是_____ 。

回答下列问题:
(1)焙烧时黄铁矿要粉碎,其目的是
(2)SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式
(3)从还原得到的溶液中获得硫酸亚铁晶体(FeSO4•7H2O)的操作:
II.作为推行“低碳经济”的重要科技进步,太阳能光伏发电成为重要的新型能源。太阳能光伏发电最关键的材料是高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅(Si)的主要方法,生产流程示意如图:

(4)石英砂的主要成分是SiO2,SiO2是
(5) “精馏”也是蒸馏的一种形式,通过蒸馏可把液体混合物分离开,原理是利用混合物各成分的
(6)整个制备过程必须达到无水无氧,在H2还原SiHCl3过程中若混入O2,除了生成SiO2外,还可能引起的后果是
(7)为达到绿色化学和资源综合利用的目的,在生产过程中物质A需要循环使用,A的化学式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】红帘石矿的主要成分为Fe3O4、Al2O3、MnCO3、MgO少量MnO2 等。工业上将红帘石处理后运用阴离子膜电解法的新技术提取金属钰并制得绿色高效的水处理剂(K2FeO4)。工业流程如下:
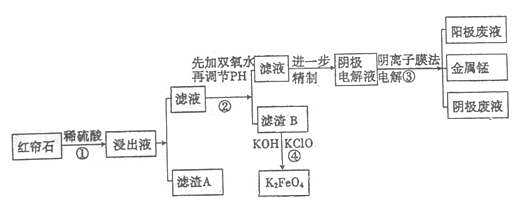
(1)在稀硫酸浸取矿石的过程中,MnO2可将Fe2+氧化为Fe3+,写出该反应的离子方程式:________________________________ 。
(2)浸出液中的阳离子除H+、Fe2+、Fe3+外还有_______ (填离子符号)。
(3)已知:不同金属离子生成生成氢氧化物沉淀所需的pH如下表:
步骤②中调节溶液的pH 等于6,调节pH的试剂最好选用下列哪种试剂:_______ (填选项字母,下同)滤渣B除掉杂质后可进一步制取K2FeO4,除掉滤渣B中杂质最好选用下列哪种试剂:_____ 。
a.稀盐酸b.KOH c.氨水d.MnCO3e.CaCO3
(4)滤渣B经反应④生成高效水处理剂的离子方程式_________________________ 。
(5)电解装置如图所示,箭头表示溶液中阴离子移动的方向;阳极电解液是稀硫酸,若阴极上只有锰单质析出,当生成11g锰时,另一个电极上产生的气体在标准状况下的体积为________ L。


(1)在稀硫酸浸取矿石的过程中,MnO2可将Fe2+氧化为Fe3+,写出该反应的离子方程式:
(2)浸出液中的阳离子除H+、Fe2+、Fe3+外还有
(3)已知:不同金属离子生成生成氢氧化物沉淀所需的pH如下表:
| 离子 | Fe3+ | A13+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 | 9.6 |
| 完全沉淀的pH | 3.7 | 4.7 | 9.6 | 9.8 | 11.1 |
步骤②中调节溶液的pH 等于6,调节pH的试剂最好选用下列哪种试剂:
a.稀盐酸b.KOH c.氨水d.MnCO3e.CaCO3
(4)滤渣B经反应④生成高效水处理剂的离子方程式
(5)电解装置如图所示,箭头表示溶液中阴离子移动的方向;阳极电解液是稀硫酸,若阴极上只有锰单质析出,当生成11g锰时,另一个电极上产生的气体在标准状况下的体积为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】MnCO3是重要的微量元素肥料之一,广泛用作脱硫的催化剂、颜料、锰盐原料等。以软锰矿(主要成分是MnO2,含SiO2、Fe2O3等少量杂质)为主要原料制备碳酸锰(MnCO3)是一种工业生产方法。其工业流程如下:

已知:几种金属离子沉淀的pH如表
回答下列问题:
(1)对矿石进行粉碎的目的是_______ 。
(2)“浸锰”时采用0.1 mol۰L-1稀硫酸而不采用较 浓H2SO4的原因是_______ 。
(3)“浸锰”过程中Fe2O3与SO2反应的离子方程式为:Fe2O3 + SO2+2H+=2Fe2+ + + H2O,该反应是经历以下两步反应实现的:
+ H2O,该反应是经历以下两步反应实现的:
i.Fe2O3 + 6H+ = 2Fe3+ + 3H2O
ii.……
写出ⅱ的离子方程式:_______ 。
(4)“氧化”过程中被MnO2氧化的物质有_______ 。
(5)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是_______ 。

(6)在“调pH”步骤中,调节合适的pH为____ ,若将溶液的pH调为5,则溶液中Fe3+浓度为_____ mol۰L-1.(已知:Ksp[Fe(OH)3]=4.0×10-38)
(7)加入NH4HCO3溶液“沉锰”,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:____ 。

已知:几种金属离子沉淀的pH如表
| 金属离子 | Fe2+ | Fe3+ | Mn2+ |
| 开始沉淀的pH | 7.5 | 3.2 | 8.8 |
| 完全沉淀的pH | 9.7 | 3.7 | 10.4 |
回答下列问题:
(1)对矿石进行粉碎的目的是
(2)“浸锰”时采用0.1 mol۰L-1稀硫酸而不采用
(3)“浸锰”过程中Fe2O3与SO2反应的离子方程式为:Fe2O3 + SO2+2H+=2Fe2+ +
 + H2O,该反应是经历以下两步反应实现的:
+ H2O,该反应是经历以下两步反应实现的:i.Fe2O3 + 6H+ = 2Fe3+ + 3H2O
ii.……
写出ⅱ的离子方程式:
(4)“氧化”过程中被MnO2氧化的物质有
(5)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是

(6)在“调pH”步骤中,调节合适的pH为
(7)加入NH4HCO3溶液“沉锰”,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:
您最近一年使用:0次



