已知N、P同属于元素周期表的第ⅤA族元素,N在第二周期,P在第三周期。 分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N—H键间的夹角是
分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N—H键间的夹角是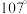 。
。
(1) 分子的空间结构为
分子的空间结构为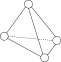 ,它是一种
,它是一种_____ (填“极性”或“非极性”)分子。
(2) 分子与
分子与 分子的构型关系
分子的构型关系_____ (填“相同”“相似”或“不相似”),P—H键_____ (填“有”或“无”)极性, 分子
分子_______ (填“有”或“无”)极性。
(3) 是一种淡黄色油状液体,下列对
是一种淡黄色油状液体,下列对 的有关描述不正确的是
的有关描述不正确的是___ (填字母)。
a.该分子呈平面三角形
b.该分子中的化学键为极性键
c.该分子为极性分子
d.因N—Cl键的键能大,故 稳定
稳定
 分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N—H键间的夹角是
分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N—H键间的夹角是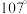 。
。(1)
 分子的空间结构为
分子的空间结构为 ,它是一种
,它是一种(2)
 分子与
分子与 分子的构型关系
分子的构型关系 分子
分子(3)
 是一种淡黄色油状液体,下列对
是一种淡黄色油状液体,下列对 的有关描述不正确的是
的有关描述不正确的是a.该分子呈平面三角形
b.该分子中的化学键为极性键
c.该分子为极性分子
d.因N—Cl键的键能大,故
 稳定
稳定
19-20高二下·河南安阳·阶段练习 查看更多[3]
河南省林州市第一中学2019-2020学年高二4月月考(实验班)化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第三节 分子结构与物质的性质 第1课时 共价键的极性(已下线)2.3.1 共价键的极性 范德华力-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)
更新时间:2020-04-08 11:50:29
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】东晋《华阳国志·南中志》卷四中已有关于白铜的记载。云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
⑴镍元素基态核外电子排布式为____________________ 。
⑵硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是____________ 。
⑶单质铜及镍都是由___________ 键形成的晶体;元素铜与镍的第二电离能分别为:ICu = 1959kJ/mol,INi =1753kJ/mol,ICu > INi的原因是 ________________________ 。
⑷某镍白铜合金的立方晶胞结构如图所示。

若合金的密度为dg/cm3,晶胞参数a =______________ nm。
⑴镍元素基态核外电子排布式为
⑵硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是
⑶单质铜及镍都是由
⑷某镍白铜合金的立方晶胞结构如图所示。

若合金的密度为dg/cm3,晶胞参数a =
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】[化学——选修3:物质结构与性质]碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态原子中,核外存在______ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是_____________ 。
(3)CS2分子中,共价键的类型有_____________ ,C原子的杂化轨道类型是_______ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______________ 。
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于_____ 晶体。
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接_____ 个六元环,每个六元环占有___ 个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接________ 个六元环,六元环中最多有________ 个C原子在同一平面。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)碳在形成化合物时,其键型以共价键为主,原因是
(3)CS2分子中,共价键的类型有
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2017年冬季,我国北方大部分地区出现严重雾霾天气,引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等。城市雾霾中还含有铜等重金属元素。
(1)N元素原子核外电子云的形状有___________ 种;基态铜原子的价电子排布式为___________ ,金属铜的晶体中,铜原子的堆积方式为___________ 。
(2)N和O中第一电离能较小的元素是___________ ;SO42-的空间构型___________ 。
(3)雾霾中含有少量的水,组成水的氢元素和氧元素也能形成化合物H2O2,其中心原子的杂化轨道类型为___________ ,H2O2难溶于CC14,其原因为___________ 。
(4)PM2.5富含大量的有毒、有害物质,如NO、CH3COOONO2(PAN)等。1mol PAN中含σ键数目为___________ ;NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配位数为___________ 。
(5)测定大气中PM2.5浓度的方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,晶胞边长为540pm,则该晶体的密度___________ g/cm3(只列式不计算)

(1)N元素原子核外电子云的形状有
(2)N和O中第一电离能较小的元素是
(3)雾霾中含有少量的水,组成水的氢元素和氧元素也能形成化合物H2O2,其中心原子的杂化轨道类型为
(4)PM2.5富含大量的有毒、有害物质,如NO、CH3COOONO2(PAN)等。1mol PAN中含σ键数目为
(5)测定大气中PM2.5浓度的方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,晶胞边长为540pm,则该晶体的密度

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氟及其化合物的用途十分广泛。回答下列问题:
(1)CuF的熔点为1008℃,熔化呈液态时能导电。CuCl的熔点为326℃,能升华,熔化呈液态时不导电。
①CuF的熔点比CuCl的高,原因是_______ 。
②已知Cu、Zn的第二电离能分别为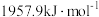 、
、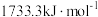 ,前者高于后者的原因是
,前者高于后者的原因是_______ 。
(2)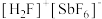 (氟锑酸,是一种超强酸),其中阳离子
(氟锑酸,是一种超强酸),其中阳离子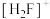 的空间构型为
的空间构型为_______ 。
(1)CuF的熔点为1008℃,熔化呈液态时能导电。CuCl的熔点为326℃,能升华,熔化呈液态时不导电。
①CuF的熔点比CuCl的高,原因是
②已知Cu、Zn的第二电离能分别为
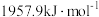 、
、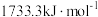 ,前者高于后者的原因是
,前者高于后者的原因是(2)
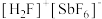 (氟锑酸,是一种超强酸),其中阳离子
(氟锑酸,是一种超强酸),其中阳离子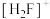 的空间构型为
的空间构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】锌是一种重要的金属,锌及其化合物有着广泛的应用。
(1)葡萄糖酸锌[CH2OH(CHOH4COO)2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式______________________ ;葡萄糖[CH2OH(CHOH)4CHO]分子中碳原子杂化方式是_________________________ 。
(2)Zn2+也能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子空间构型为______ ;在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在下图中
表示[Zn(NH3)4]2+中Zn2+与N之间的化学键_______ 。

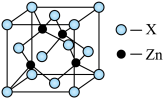
(3)下图表示锌与某种元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为_______ ;该化合物的晶体熔点比干冰高得多,原因是_____ 。
(1)葡萄糖酸锌[CH2OH(CHOH4COO)2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式
(2)Zn2+也能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子空间构型为
表示[Zn(NH3)4]2+中Zn2+与N之间的化学键

(3)下图表示锌与某种元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。

(1)基态硫原子价层电子排布式为___________ ;其核外有___________ 个运动状态不同的电子;其最外层有___________ 个未成对电子;其最高能级的轨道有___________ 个伸展方向,电子云形状为___________ 。
(2) 、
、 、
、 的沸点由高到低顺序为
的沸点由高到低顺序为___________
(3) (硒)与硫同主族,位于元素周期表第
(硒)与硫同主族,位于元素周期表第___________ 周期第___________ 族。
(4)化合物Ⅲ也是一种汞解毒剂。下列关于上述物质的说法正确的有___________ 。
A.在Ⅰ和Ⅳ中S原子均采取 杂化
杂化
B.在Ⅱ中所有元素中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等

(1)基态硫原子价层电子排布式为
(2)
 、
、 、
、 的沸点由高到低顺序为
的沸点由高到低顺序为(3)
 (硒)与硫同主族,位于元素周期表第
(硒)与硫同主族,位于元素周期表第(4)化合物Ⅲ也是一种汞解毒剂。下列关于上述物质的说法正确的有
A.在Ⅰ和Ⅳ中S原子均采取
 杂化
杂化B.在Ⅱ中所有元素中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)蓝矾 的结构如图所示:
的结构如图所示:

 的空间结构是
的空间结构是___________ ,其中S原子的杂化轨道类型是___________ ;基态O原子的价层电子排布图为___________ 。
(2)气态 分子的空间结构为
分子的空间结构为___________ ;将纯液态 冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图所示,此固态
冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图所示,此固态 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是___________ 。

(3)已知 为V形,中心氯原子周围有四个价层电子对。
为V形,中心氯原子周围有四个价层电子对。 的中心氯原子的杂化轨道类型为
的中心氯原子的杂化轨道类型为___________ 。
(4)二氧化钛 是常用的具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米
是常用的具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米 催化的一个实例如图所示。
催化的一个实例如图所示。

化合物甲的分子中采取 杂化方式的碳原子个数为
杂化方式的碳原子个数为___________ ,化合物乙中采取 杂化的原子对应元素的第一电离能由小到大的顺序为
杂化的原子对应元素的第一电离能由小到大的顺序为___________ 。
 的结构如图所示:
的结构如图所示:
 的空间结构是
的空间结构是(2)气态
 分子的空间结构为
分子的空间结构为 冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图所示,此固态
冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图所示,此固态 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是
(3)已知
 为V形,中心氯原子周围有四个价层电子对。
为V形,中心氯原子周围有四个价层电子对。 的中心氯原子的杂化轨道类型为
的中心氯原子的杂化轨道类型为(4)二氧化钛
 是常用的具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米
是常用的具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米 催化的一个实例如图所示。
催化的一个实例如图所示。
化合物甲的分子中采取
 杂化方式的碳原子个数为
杂化方式的碳原子个数为 杂化的原子对应元素的第一电离能由小到大的顺序为
杂化的原子对应元素的第一电离能由小到大的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】西瓜膨大剂别名氯吡苯脲,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。已知其相关性质如下表所示:
(1)氯吡苯脲晶体中,氮原子的杂化方式为___ 。
(2)两种组成均为CoCl3·4NH3的配合物分别呈绿色和紫色。已知绿色的配合物内界结构对称,请在图a和图b中用元素符号标出氯原子的位置___ 、___ 。


| 分子式 | C12H10ClN3O |
| 结构简式 |  |
| 外观 | 白色结晶粉末 |
| 熔点 | 170~172℃ |
| 溶解性 | 易溶于水 |
(1)氯吡苯脲晶体中,氮原子的杂化方式为
(2)两种组成均为CoCl3·4NH3的配合物分别呈绿色和紫色。已知绿色的配合物内界结构对称,请在图a和图b中用元素符号标出氯原子的位置


您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表为元素周期表的一部分,其中字母代表相应的元素。

试回答下列问题:
(1)元素h的基态原子的核外电子排布式为_______ 。
(2)c、d、e、f元素原子的第一电离能( )由小到大的顺序为
)由小到大的顺序为_______ (用相应元素符号表示)。
(3)表中所列的元素之间可以形成多种化合物,其中邻甲基苯甲醛( )分子中碳原子轨道的杂化类型为
)分子中碳原子轨道的杂化类型为_____ 。1mol苯甲醛( )分子中含有σ键的物质的量为
)分子中含有σ键的物质的量为______ mol。
(4)一种由表中元素形成的离子与单质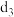 互为等电子体,其离子符号为
互为等电子体,其离子符号为_______ 。

试回答下列问题:
(1)元素h的基态原子的核外电子排布式为
(2)c、d、e、f元素原子的第一电离能(
 )由小到大的顺序为
)由小到大的顺序为(3)表中所列的元素之间可以形成多种化合物,其中邻甲基苯甲醛(
 )分子中碳原子轨道的杂化类型为
)分子中碳原子轨道的杂化类型为 )分子中含有σ键的物质的量为
)分子中含有σ键的物质的量为(4)一种由表中元素形成的离子与单质
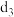 互为等电子体,其离子符号为
互为等电子体,其离子符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】双氧水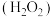 是一种医用消毒杀菌剂,已知
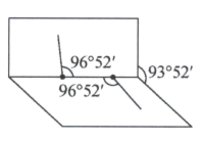
是一种医用消毒杀菌剂,已知 分子的结构如图所示:
分子的结构如图所示: 分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书面角为93°52',而两个
分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书面角为93°52',而两个 键与
键与 键的夹角均为96°52′。试回答:
键的夹角均为96°52′。试回答:
(1) 分子中存在
分子中存在___________ 键和___________ 键,为___________ 分子。(填“极性”或“非极性”)
(2) 难溶于
难溶于 ,其原因是
,其原因是___________ 。
(3) 分子中氧元素的化合价为
分子中氧元素的化合价为___________ 价。
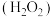 是一种医用消毒杀菌剂,已知
是一种医用消毒杀菌剂,已知 分子的结构如图所示:
分子的结构如图所示: 分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书面角为93°52',而两个
分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书面角为93°52',而两个 键与
键与 键的夹角均为96°52′。试回答:
键的夹角均为96°52′。试回答:
(1)
 分子中存在
分子中存在(2)
 难溶于
难溶于 ,其原因是
,其原因是(3)
 分子中氧元素的化合价为
分子中氧元素的化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)下列分子中若有手性原子,请用“*”标出其手性碳原子_______ 、_______ 。
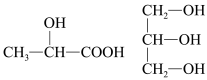
(2)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填编号)_______ 。
(3)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4_______ H2SO3;HClO3_______ HClO4;
(4)根据价层电子对互斥理论判断下列问题:H2S中心原子的杂化方式为_______ 杂化,VSEPR构型为_______ ,分子的立体构型为_______ 。
(5)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于_______ 。
(1)下列分子中若有手性原子,请用“*”标出其手性碳原子
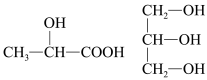
(2)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填编号)
(3)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4
(4)根据价层电子对互斥理论判断下列问题:H2S中心原子的杂化方式为
(5)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于
您最近一年使用:0次

 、
、 、
、 六种分子,试回答下列问题:
六种分子,试回答下列问题:

