某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0 g石灰石样品,把25.0g质量分数为10%的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
请计算:
(1)2.0g石灰石样品中碳酸钙的质量为___,石灰石中碳酸钙的质量分数为_____。
(2)请你继续计算反应生成溶液中氯化钙的质量分数(计算过程和结果均保留一位小数)。__________
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 稀盐酸的累计加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0 g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.3g | 0.3g |
请计算:
(1)2.0g石灰石样品中碳酸钙的质量为___,石灰石中碳酸钙的质量分数为_____。
(2)请你继续计算反应生成溶液中氯化钙的质量分数(计算过程和结果均保留一位小数)。__________
11-12九年级上·山东枣庄·期末 查看更多[7]
山东省东营市河口区胜利三十九中2020-2021学年九年级上学期10月月考化学试题2016年广东省韶关市新丰县黄磜中学中考模拟化学试题(已下线)2011届山东省枣庄市齐村中学初三上学期命题比赛化学卷人教新课标初三下册第十章酸和碱专项训练2(已下线)2011届江苏省宜兴市和桥学区九年级5月模拟考试化学试卷(已下线)2011届广东省惠州八中初三上学期期中考试化学卷(已下线)2011年北京市西城区初三第一学期期末化学卷
更新时间:2016-11-27 08:33:15
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】下图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器。
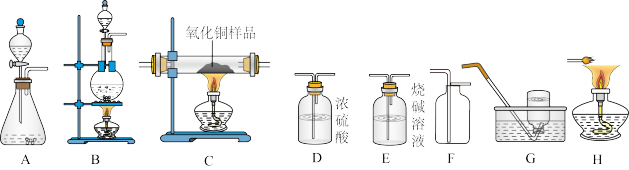
试根据题目要求,回答下列问题:
⑴请写出能用装置A制备的一种气体的化学反应方程式_____ ,该气体可选用装置 _____ 来收集(填装置序号),其选择依据是 _____ 。
⑵小颖同学欲用干燥、纯净的一氧化碳气体还原某氧化铜样品(杂质只有铜),并测定其纯度。
【查阅资料】
将草酸(H2C2O4)晶体与浓硫酸混合加热,会产生一氧化碳等气体,其反应原理为:H2C2O4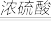 CO↑+CO2↑+H2O。
CO↑+CO2↑+H2O。
①若小颖同学选用草酸来制取CO,其发生装置她应选择_____ (填装置序号)。
【定量实验】
②小颖同学先用电子秤称取了1.00g氧化铜样品,放入装置C中的玻璃管内并组装好所有相关仪器,再将草酸分解得到的气体产物按照以下仪器的连接顺序进行实验:混合气体→D→C→E→H,最后,通过测量反应前后装置E的质量变化进行计算。(已知:CO+CuO Cu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是
Cu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是 _____ 。
③请你分析上述实验方案存在的不足之处及对应的改进方法 _____ 。
④实验改进后,小颖同学对实验所得的正确数据进行分析处理(设所发生的反应均完全进行):通过测定,当装置C中的氧化铜全部被还原后,装置E的质量增加了0.33g,则该样品中氧化铜的质量分数为_____ (结果精确至0.1%)。
⑤小黄同学提出了异议,他认为若②中实验方案不加以改进,也能正确测算出该样品中氧化铜的纯度,他的计算依据或方法为:_____ 。

试根据题目要求,回答下列问题:
⑴请写出能用装置A制备的一种气体的化学反应方程式
⑵小颖同学欲用
【查阅资料】
将草酸(H2C2O4)晶体与浓硫酸混合加热,会产生一氧化碳等气体,其反应原理为:H2C2O4
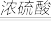 CO↑+CO2↑+H2O。
CO↑+CO2↑+H2O。①若小颖同学选用草酸来制取CO,其发生装置她应选择
【定量实验】
②小颖同学先用电子秤称取了1.00g氧化铜样品,放入装置C中的玻璃管内并组装好所有相关仪器,再将草酸分解得到的气体产物按照以下仪器的连接顺序进行实验:混合气体→D→C→E→H,最后,通过测量反应前后装置E的质量变化进行计算。(已知:CO+CuO
 Cu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是
Cu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是 ③请你分析上述实验方案存在的不足之处
④实验改进后,小颖同学对实验所得的正确数据进行分析处理(设所发生的反应均完全进行):通过测定,当装置C中的氧化铜全部被还原后,装置E的质量增加了0.33g,则该样品中氧化铜的质量分数为
⑤小黄同学提出了异议,他认为若②中实验方案不加以改进,也能正确测算出该样品中氧化铜的纯度,他的计算依据或方法为:
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】化学兴趣小组在实验室用含硫酸铜的废液和氯化钡溶液反应制取少量氯化铜溶液,并测定该废液中铜离子的含量。实验过程和相关数据如下:用烧杯称取含硫酸铜的废液120.0 g,滴加氯化钡溶液至126.6 g时,恰好完全反应,过滤,称得滤液质量为200.0 g。请计算:(废液中杂质不参加反应)
(1)反应后生成沉淀的质量是________g;
(2)所得氯化铜溶液中溶质的质量分数(写出计算过程);
(3)原硫酸铜溶液中铜离子的质量分数是___________(精确到0.1%)。
(1)反应后生成沉淀的质量是________g;
(2)所得氯化铜溶液中溶质的质量分数(写出计算过程);
(3)原硫酸铜溶液中铜离子的质量分数是___________(精确到0.1%)。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】28.7g的氯化钠和硝酸钠的混合物,溶于100g水中,向所得溶液中加入134g的硝酸银溶液,恰好完全反应,得到溶液的质量是234g.计算:原混合物中钠元素的质量分数.(已知:AgNO3+NaCl=AgCl↓+NaNO3;计算结果精确到1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】实验室有一份在空气中潮解部分变质的氢氧化钠样品,质量为1.86g。某实验小组将这份样品完全溶解,配成 50g 溶液,然后缓慢滴入 7.3%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。滴加过程中,多次测得溶液 pH 和溶液总质量,部分数据如下表所示:
请分析计算:
(1)实验中生成二氧化碳的质量为_______ g。
(2)求样品中氢氧化钠的质量(请写出计算过程)。
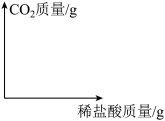
(3)请在下图中画出稀盐酸质量与二氧化碳质量关系的图像(标出关键点的数据)。
(4)当恰好完全反应时,该溶液的溶质质量分数是____ 。(结果保留两位小数)。
| 测量次数 | 第 1 次 | 第 2 次 | 第 3 次 | 第 4 次 | 第 5 次 |
| 滴加的盐酸总质量/g | 0 | 5 | 20 | 30 | 35 |
| 溶液总质量/g | 50 | 55 | 69.56 | 79.56 | 84.56 |
| 溶液 pH | 12.4 | 12.1 | 7.0 | 2.2 | 2.1 |
(1)实验中生成二氧化碳的质量为
(2)求样品中氢氧化钠的质量(请写出计算过程)。
(3)请在下图中画出稀盐酸质量与二氧化碳质量关系的图像(标出关键点的数据)。

(4)当恰好完全反应时,该溶液的溶质质量分数是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某化工厂生产的轻质碳酸钙粉末中含有少量的氯化钙,小明所在的化学兴趣小组要测定该碳酸钙粉末中碳酸钙的质量分数。小明取50g样品放入烧杯中,然后向其中加入稀盐酸反应情况如图甲所示,反应过程中的质量变化如图乙所示。试计算
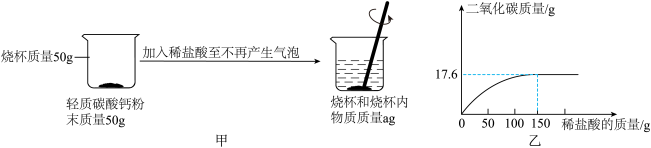
(1)甲图中a的值为_____。
(2)计算参加反应的氯化氢的质量____。
(3)计算该轻质碳酸钙粉末中碳酸钙的质量分数____。

(1)甲图中a的值为_____。
(2)计算参加反应的氯化氢的质量____。
(3)计算该轻质碳酸钙粉末中碳酸钙的质量分数____。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐3】某化学兴趣小组在实验室用硫酸铜溶液和氯化钡溶液反应制取少量氯化铜溶液。他们的实验过程和相关数据如下(BaSO4不溶于水)。
第一步:称得烧杯的质量是100 g。
第二步:反应前称得烧杯、氯化钡溶液及硫酸铜溶液的总质量是346.6 g。
第三步:两者恰好完全反应后,过滤,称得烧杯及滤液的总质量是300 g。
请计算:
(1)反应后生成沉淀的质量是_______________。
(2)所得氯化铜溶液中溶质的质量分数为________(写出计算过程,精确到0.1%)。
第一步:称得烧杯的质量是100 g。
第二步:反应前称得烧杯、氯化钡溶液及硫酸铜溶液的总质量是346.6 g。
第三步:两者恰好完全反应后,过滤,称得烧杯及滤液的总质量是300 g。
请计算:
(1)反应后生成沉淀的质量是_______________。
(2)所得氯化铜溶液中溶质的质量分数为________(写出计算过程,精确到0.1%)。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐1】为测定某AgNO3溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定。现取待测液50.0 g,滴定过程如图所示。
(滴定反应为:AgNO3+HCl=AgCl↓+HNO3,Ag的相对原子质量为108,计算结果均保留1位小数)
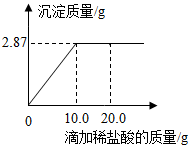
(1)AgNO3的相对分子质量为:_____;
(2)计算AgNO3溶液的溶质质量分数;
(3)计算恰好完全反应时,所得溶液的溶质质量分数。
(滴定反应为:AgNO3+HCl=AgCl↓+HNO3,Ag的相对原子质量为108,计算结果均保留1位小数)

(1)AgNO3的相对分子质量为:_____;
(2)计算AgNO3溶液的溶质质量分数;
(3)计算恰好完全反应时,所得溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】家里蒸馒头用的纯碱中含有少量的氯化钠,课外探究小组的同学欲测定某超市出售的纯碱样品是否符合标准(标明中碳酸钠的含量为≥96%)。他们取该纯碱样品11.0g,全部溶解在100.0g水中,再加入氯化钙溶液141.0g,恰好完全反应。过滤干燥后,称得沉淀质量为10.0g。请计算:
(1)纯碱样品中碳酸钠的质量;
(2)该样品是否合格;
(3)反应后所得滤液中溶质的质量分数。
(1)纯碱样品中碳酸钠的质量;
(2)该样品是否合格;
(3)反应后所得滤液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】某工厂生产的纯碱中含有一定量的氯化钠杂质,现取22g该样品完全溶解在100g水中,当加入128.8g稀盐酸时恰好完全反应,得到242g的不饱和溶液。请计算:
(1)纯碱中钠、碳、氧元素的质量比为________;
(2)生成CO2的质量为_______g;
(3)所得溶液中溶质的质量分数(写出计算过程) ______。
(1)纯碱中钠、碳、氧元素的质量比为________;
(2)生成CO2的质量为_______g;
(3)所得溶液中溶质的质量分数(写出计算过程) ______。
您最近一年使用:0次



