某研究小组发现,将适量不溶于水的淀粉放入过氧化氢溶液中,过氧化氢溶液的分解速率加快,对于此现象,该小组同学进行了如下探究:
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【作出猜想】淀粉能作过氧化氢分解的催化剂
【实验验证】
(1)写出淀粉催化过氧化氢分解的符号表达式_______ ;
(2)小组对比探究淀粉与二氧化锰的催化效果,实验以生成25mL氧气为标准,数据见下表:
上述实验中“待测数据”是指_______ ;
(3)若a>b,可得出的结论是_______ 。
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【作出猜想】淀粉能作过氧化氢分解的催化剂
【实验验证】
| 实验步骤 | 实验现象 | 结论及解释 |
Ⅰ.  | A中无明显现象,B中迅速产生大量能使带火星木条复燃的气体 | ①产生的气体是氧气 ②淀粉能 |
| Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应结束,将剩余物质过滤、洗涤、干燥、称量 | ①又能迅速产生大量使带火星木条复燃的气体 ②淀粉质量为a g | 淀粉的 |
(2)小组对比探究淀粉与二氧化锰的催化效果,实验以生成25mL氧气为标准,数据见下表:
| 实验编号 | 3%过氧化氢溶液的体积 | 其他物质质量 | 待测数据 |
| Ⅰ | 20 ml | 淀粉 0.5g | a |
| Ⅱ | 20 ml | 二氧化锰 0.5g | b |
(3)若a>b,可得出的结论是
更新时间:2020-12-15 17:03:47
|
相似题推荐
【推荐1】某化学兴趣小组对实验制取氧气及催化剂展开了探究,请回答下列问题:
【探究一】影响过氧化氢分解速率的因素有哪些?兴趣小组同学做了五组实验,实验数据如下表:
(1)能说明过氧化氢的分解速率与其浓度有关的实验是______ (填实验序号)。
(2)对比①②两组实验,可得出过氧化氢分解速率与温度的关系:当过氧化氢溶液的体积和浓度等其它条件相同时______ 。
(3)根据实验数据反映出来的规律,表中数据t的合理范围是:______ <t<______ 。
(4)为完成上述实验中收集氧气及数据的测定需要用到的部分装置如图1所示,与c连接的是______ (填“a”或“b”)端。进行操作时,集气瓶中未装满水,对实验测量结果______ (填“会”或“不会”)产生影响。
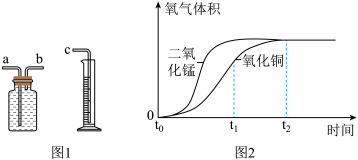
(5)该兴趣小组探究了不同的金属氧化物对过氧化氢分解速率的影响。他们在等体积的两个锥形瓶中加入40mL5%的H2O2溶液,分别加入MnO2、CuO后,根据实验数据绘制了产生的氧气体积和时间变化的曲线如图2。观察该图回答问题:
①通过图像除了能得出二氧化锰催化效果比氧化铜好,还能得出的结论是______ 。
②由氧化铜催化的反应,t1~t2时间段反应速率逐渐变______ (填“快”或“慢”),原因可能是______ 。
【探究一】影响过氧化氢分解速率的因素有哪些?兴趣小组同学做了五组实验,实验数据如下表:
| 实验序号 | H2O2溶液的 浓度 | H2O2溶液的 体积/mL | MnO2的 用量/g | 温度/℃ | 收集O2的 体积/mL | 所需 时间/S |
| ① | 20 | 2 | 0.1 | 85 | 20 | 3.8 |
| ② | 20 | 2 | 0.1 | 55 | 20 | 10.5 |
| ③ | 15 | 2 | 0.1 | 20 | 20 | 21.6 |
| ④ | 15 | 2 | 0.1 | 55 | 20 | t |
| ⑤ | 15 | 2 | 0.2 | 20 | 20 | 2.8 |
| ⑥ | 5 | 2 | 0.2 | 20 | 20 | 7.4 |
(2)对比①②两组实验,可得出过氧化氢分解速率与温度的关系:当过氧化氢溶液的体积和浓度等其它条件相同时
(3)根据实验数据反映出来的规律,表中数据t的合理范围是:
(4)为完成上述实验中收集氧气及数据的测定需要用到的部分装置如图1所示,与c连接的是

(5)该兴趣小组探究了不同的金属氧化物对过氧化氢分解速率的影响。他们在等体积的两个锥形瓶中加入40mL5%的H2O2溶液,分别加入MnO2、CuO后,根据实验数据绘制了产生的氧气体积和时间变化的曲线如图2。观察该图回答问题:
①通过图像除了能得出二氧化锰催化效果比氧化铜好,还能得出的结论是
②由氧化铜催化的反应,t1~t2时间段反应速率逐渐变
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】学习了二氧化锰对过氧化氢分解有催化作用的知识后,某兴趣小组同学在课外进行了有关过氧化氢分解反应的再探究。
【探究一】影响过氧化氢分解速率的因素有哪些? 兴趣小组同学做了四个实验,实验数据如下表:
(1)对比③④两组实验,可得出过氧化氢分解速率与温度的关系:当过氧化氢溶液的体积和浓度等其它条件相同时,_____ 。
(2)能说明过氧化氢的分解速率与其质量分数有关的实验是______ 填实验序号)。
【探究二】其他金属氧化物能否起到类似 MnO2 的催化作用?
兴趣小组同学用天平称量 0.2 g CuO,用量筒量取 5 mL 5% 的H2O2溶液,进行如下图所示实验(①~⑦代表实验操作步骤)。
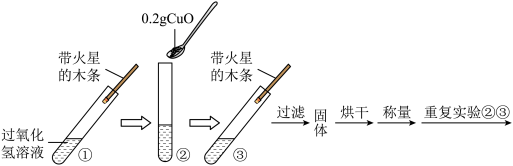
(3)小组同学通过上述实验得出结论:CuO 可作过氧化氢分解的催化剂,支持该结论的实验证据是_____ 。
(4)欲比较不同催化剂 CuO 和 MnO2对H2O2 分解速率的影响,实验时需要控制的变量有_____ 。
(5)过氧化氢能被MnO2 催化分解放出氧气的文字(或符号)表达式为_____ 。
【探究一】影响过氧化氢分解速率的因素有哪些? 兴趣小组同学做了四个实验,实验数据如下表:
| 实验 序号 | H2O2 溶液的溶质质量分数% | H2O2 溶液的体积/mL | 温 度 /℃ | MnO2的用量/g | 收集O2的体积/mL | 反应 时间 |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16 s |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6 s |
| ③ | 30 | 5 | 35 | 0 | 4 | 98 min |
| ④ | 30 | 5 | 55 | 0 | 4 | 2 0min |
(2)能说明过氧化氢的分解速率与其质量分数有关的实验是
【探究二】其他金属氧化物能否起到类似 MnO2 的催化作用?
兴趣小组同学用天平称量 0.2 g CuO,用量筒量取 5 mL 5% 的H2O2溶液,进行如下图所示实验(①~⑦代表实验操作步骤)。

(3)小组同学通过上述实验得出结论:CuO 可作过氧化氢分解的催化剂,支持该结论的实验证据是
(4)欲比较不同催化剂 CuO 和 MnO2对H2O2 分解速率的影响,实验时需要控制的变量有
(5)过氧化氢能被MnO2 催化分解放出氧气的文字(或符号)表达式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组同学对实验室用氯酸钾制备氧气的条件进行如下探究。
【问题一】哪种金属氧化物最适合做氯酸钾分解的催化剂?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用。
分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
(1)实验室用氯酸钾制取氧气,需要在较低的温度下进行催化,最好选用_____ 做催化剂。
【问题二】它是否比二氧化锰催化效果好?
【实验设计】
Ⅰ、将 3.0g 氯酸钾与 1.0g 二氧化锰均匀混合加热将
Ⅱ、将 Xg 氯酸钾与 1.0g 所选金属氧化物均匀混合加热
Ⅲ、反应结束,称量金属氧化物的质量为 Yg
【实验分析】
(2)实验Ⅱ、Ⅲ中 X、Y 的值分别为_____ 、_____ 。
(3)通过比较_____ 能达到实验目的。
【实验结论】
(4)该金属氧化物也能作氯酸钾分解的催化剂,实验Ⅱ反应的符号表达式为_____ 。
【问题一】哪种金属氧化物最适合做氯酸钾分解的催化剂?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用。
分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
种类 反应程度及温度 | 氧化铁(Fe2O3) | 氧化铝 (Al2O3) | 氧化铜(CuO) | 氧化镁 (MgO) |
| 开始反应温度(℃) | 420 | 515 | 305 | 490 |
| 剧烈反应温度(℃) | 490 | 540 | 350 | 545 |
(1)实验室用氯酸钾制取氧气,需要在较低的温度下进行催化,最好选用
【问题二】它是否比二氧化锰催化效果好?
【实验设计】
Ⅰ、将 3.0g 氯酸钾与 1.0g 二氧化锰均匀混合加热将
Ⅱ、将 Xg 氯酸钾与 1.0g 所选金属氧化物均匀混合加热
Ⅲ、反应结束,称量金属氧化物的质量为 Yg
【实验分析】
(2)实验Ⅱ、Ⅲ中 X、Y 的值分别为
(3)通过比较
【实验结论】
(4)该金属氧化物也能作氯酸钾分解的催化剂,实验Ⅱ反应的符号表达式为
您最近一年使用:0次
【推荐1】某学习小组的同学对过氧化氢分解进行探究。
【探究一】影响过氧化氢分解快慢的因素
分别取5mL过氧化氢溶液进行实验测定产生4mL氧气所需时间,实验结果记录如下:
(1)对比①②可知,其他条件相同时,温度越高,过氧化氢分解越快,则t1______ (填“﹥”“﹤”或“﹦”)t2。
(2)能说明过氧化氢分解快慢与过氧化氢溶液的浓度有关的实验是___________ (填实验序号),合理的结论是___________
交流探讨:二氧化锰属于金属氧化物,其他金属氧化物能否起到类似二氧化锰的催化作用?
【探究二】探究氧化铁是否对过氧化氢分解起催化作用
得出结论:过氧化氢分解的快慢受催化剂、___________ 、___________ 等因素的影响。
【探究一】影响过氧化氢分解快慢的因素
分别取5mL过氧化氢溶液进行实验测定产生4mL氧气所需时间,实验结果记录如下:
| 实验序号 | 过氧化氢溶液的浓度% | 温度/℃ | 二氧化锰粉末用量/g | 反应时间 |
| ① | 30 | 35 | 0 | t1 |
| ② | 30 | 55 | 0 | t2 |
| ③ | 5 | 20 | 0.1 | 3s |
| ④ | 15 | 20 | 0.1 | 1s |
(1)对比①②可知,其他条件相同时,温度越高,过氧化氢分解越快,则t1
(2)能说明过氧化氢分解快慢与过氧化氢溶液的浓度有关的实验是
交流探讨:二氧化锰属于金属氧化物,其他金属氧化物能否起到类似二氧化锰的催化作用?
【探究二】探究氧化铁是否对过氧化氢分解起催化作用
| 操作步骤 | 实验情况记录 | 结论 | |
| ① | 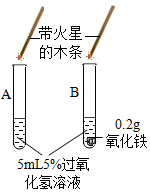 | A试管上方带火星的木条未复燃,B中出现气泡快,带火星的木条复燃 | 氧化铁 过氧化氢分解 |
| ② | 将B试管中的混合物过滤,把滤渣烘干、称量 | 固体质量为 | 氧化铁质量不变 |
| ③ | 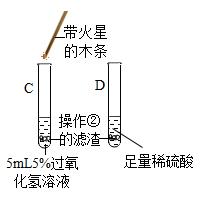 | C试管上方带火星木条 | 氧化铁可做过氧化氢分解的催化剂 |
得出结论:过氧化氢分解的快慢受催化剂、
您最近一年使用:0次
【推荐2】实验室常用加热氯酸钾(KClO3)与二氧化锰(MnO2)混合物的方法制取氧气:
(1)写出反应的符号表达式_______ ,二氧化锰是_______ 色固体,其在反应中起_______ 作用。小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除MnO2、CuO(氧化铜)外,Fe2O3(氧化铁)也可作氯酸钾分解的催化剂。
【完成实验】按下表进行实验并获得相关数据(分解温度越低,催化效果越好)
【分析数据、得出结论】
(2)实验D中KClO3、Fe2O3的质量比应该为_______ ;由实验_______ (填实验编号)与实验D对比,证明氧化铁也可作氯酸钾分解的催化剂。
(3)该实验中所用的三种催化剂,催化效果最好的是_______ ;在加热等量的氯酸钾固体时,使用不同的催化剂,最终产生氧气的量是否相等?_______ 。(填“是”或“否”)
【反思】若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后_______ 和_______ 不变。
(1)写出反应的符号表达式
【提出猜想】除MnO2、CuO(氧化铜)外,Fe2O3(氧化铁)也可作氯酸钾分解的催化剂。
【完成实验】按下表进行实验并获得相关数据(分解温度越低,催化效果越好)
| 实验编号 | 实验药品 | 分解温度(℃) |
| A | KClO3 | 580 |
| B | KC1O3、MnO2(质量比1:1) | 350 |
| C | KClO3、CuO(质量比l:1) | 370 |
| D | KC1O3、Fe2O3(质量比1:1) | 390 |
【分析数据、得出结论】
(2)实验D中KClO3、Fe2O3的质量比应该为
(3)该实验中所用的三种催化剂,催化效果最好的是
【反思】若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】春节时家里人给爷爷买了一台便携式制氧器,如图1所示。小明很感兴趣,与同学们开启了探究学习之旅。
【提出问题】该制氧器的工作原理是什么?
【阅读说明书】如图2所示:

【交流讨论】
(1)联想实验室制取氧气的反应原理,根据反应条件,确定A剂不是氯酸钾或高锰酸钾。根据A剂的_________________ ,确定A剂不是过氧化氢溶液。
【查阅资料】白色颗粒过碳酸钠(化学式2Na2CO3·3H2O2)溶于水时,分解生成碳酸钠(Na2CO3)和过氧化氢,是很好的固体氧释放剂。
【作出猜想】
(2)A剂可能是过碳酸钠,将其放入水中时,生成碳酸钠和过氧化氢。B剂是二氧化锰,它在过氧化氢分解时起_________________ 作用。
【实验验证】
(3)选择图3所示仪器中的__________ (填字母),组装好气体发生装置,依次加入过碳酸钠、水和二氧化锰,有大量气泡生成。
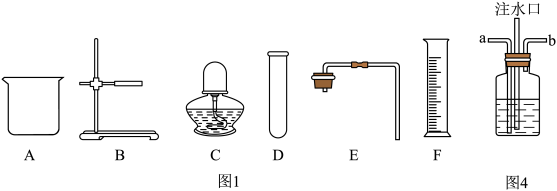
(4)用排水法收集产生的气体并用带火星的木条检验,证明产生的气体是氧气。这其中利用了氧气的物理性质和化学性质分别是______________ 。
(5)向反应后的溶液中,滴加稀盐酸产生气体,气体能使澄清石灰水变浑浊,证明溶液中含有碳酸钠。写出气体使澄清石灰水变浑浊的化学方程式:____________ 。
使用制氧器中的A剂和B剂代替过碳酸钠和二氧化锰重复进行上述(1)~(3)步实验,发现实验现象完全相同,证明猜想正确。
【反思应用】
(6)该制氧机配备的湿化瓶装置,类似于图4,在人吸氧时方便观察到瓶中的气泡。关于该装置,下列说法错误的是_________________(填字母)。
(7)若自己设计制作简易的家用制氧机时,除需考虑反应原理、方法、材料等的选择外,还需考虑很多方面的因素,例如:_________________ (写一条)。
【提出问题】该制氧器的工作原理是什么?
【阅读说明书】如图2所示:

【交流讨论】
(1)联想实验室制取氧气的反应原理,根据反应条件,确定A剂不是氯酸钾或高锰酸钾。根据A剂的
【查阅资料】白色颗粒过碳酸钠(化学式2Na2CO3·3H2O2)溶于水时,分解生成碳酸钠(Na2CO3)和过氧化氢,是很好的固体氧释放剂。
【作出猜想】
(2)A剂可能是过碳酸钠,将其放入水中时,生成碳酸钠和过氧化氢。B剂是二氧化锰,它在过氧化氢分解时起
【实验验证】
(3)选择图3所示仪器中的

(4)用排水法收集产生的气体并用带火星的木条检验,证明产生的气体是氧气。这其中利用了氧气的物理性质和化学性质分别是
(5)向反应后的溶液中,滴加稀盐酸产生气体,气体能使澄清石灰水变浑浊,证明溶液中含有碳酸钠。写出气体使澄清石灰水变浑浊的化学方程式:
使用制氧器中的A剂和B剂代替过碳酸钠和二氧化锰重复进行上述(1)~(3)步实验,发现实验现象完全相同,证明猜想正确。
【反思应用】
(6)该制氧机配备的湿化瓶装置,类似于图4,在人吸氧时方便观察到瓶中的气泡。关于该装置,下列说法错误的是_________________(填字母)。
| A.b导管连接制氧机 | B.b导管连接人吸氧气的鼻塞 |
| C.使用该装置可以观测是否有氧气输出 | D.使用该装置可以观测氧气输出的速率 |
(7)若自己设计制作简易的家用制氧机时,除需考虑反应原理、方法、材料等的选择外,还需考虑很多方面的因素,例如:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】教材“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
[提出问题]
(1)氧化铁(化学式Fe2O3)能否作过氧化氢溶液分解的催化剂?
[提出验证]
[实验结论]
(2)实验②、③证明:氧化铁的________ 和_______ 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(3)请用化学式表示氧化铁催化过氧化氢的反应_________ 。
[实验评论]
(4)实验设计④的目的是__________ 。
[知识拓展]
(5)查阅资料得知,氧化铜、硫酸铜溶液、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂,下列有关催化剂的说法正确的是______ (填字母序号)
A同一个化学反应可以有多种催化剂
B MnO2 只能作为氧化氢溶液分解的催化剂
C催化剂只加快反应速率
D作催化剂的物质不能是其他反应的反应物或生成物
[提出问题]
(1)氧化铁(化学式Fe2O3)能否作过氧化氢溶液分解的催化剂?
[提出验证]
| 实验步骤 | 实验现象 |
| ①分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管加入a克氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象。 | A试管中 B试管中无明显现象。 |
| ②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管内,如此反复多次试验,观察现象。 | 试管内均产生大量气泡。带火星木条均复燃 |
| ③将实验②中的剩余物小心过滤,并将所得滤渣进行过滤、洗涤、干燥、 | 所得固体质量仍为a克 |
| ④分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中放入a克氧化铁粉末,向D试管中加入a克二氧化锰粉末,观察现象。 | 现象略 |
[实验结论]
(2)实验②、③证明:氧化铁的
(3)请用化学式表示氧化铁催化过氧化氢的反应
[实验评论]
(4)实验设计④的目的是
[知识拓展]
(5)查阅资料得知,氧化铜、硫酸铜溶液、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂,下列有关催化剂的说法正确的是
A同一个化学反应可以有多种催化剂
B MnO2 只能作为氧化氢溶液分解的催化剂
C催化剂只加快反应速率
D作催化剂的物质不能是其他反应的反应物或生成物
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】今年春节前夕,我国北方遭遇冰雪灾害。为了清除道路上的冰雪,有关部门投入了大量工业盐融雪剂用于除冰雪。同学们从新闻中得知:①使用工业盐融雪剂后,道路两旁树木、农作物大量死亡;②桥梁路面除冰不得使用工业盐融雪剂。
【提出问题】工业盐融雪剂对树木、农作物和桥梁为什么会造成危害?
【查找资料】(1)工业盐的主要成分是NaCl和NaNO2。
(2)土壤盐碱化会造成树木、农作物死亡。
【提出猜想】猜想一:工业盐溶液可能显碱性;
猜想二:工业盐溶液对钢铁可能有更强的腐蚀性。
【实验探究】同学们对猜想一和猜想二进行了探究,请你帮他们完成下列实验报告:
【反思与应用】
对于道路除冰,请你提出更好的建议_______ 。
【提出问题】工业盐融雪剂对树木、农作物和桥梁为什么会造成危害?
【查找资料】(1)工业盐的主要成分是NaCl和NaNO2。
(2)土壤盐碱化会造成树木、农作物死亡。
【提出猜想】猜想一:工业盐溶液可能显碱性;
猜想二:工业盐溶液对钢铁可能有更强的腐蚀性。
【实验探究】同学们对猜想一和猜想二进行了探究,请你帮他们完成下列实验报告:
| 实验操作 | 实验现象 | 实验结论 | |
| 猜想一 | 工业盐溶液显碱性,会造成道路两旁的土壤盐碱化 | ||
| 猜想二 | 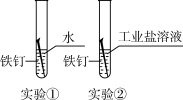 | 实验①:6-7天后明显生锈 实验②:2-3天后明显生锈 |
【反思与应用】
对于道路除冰,请你提出更好的建议
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
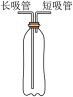
【推荐3】小艾同学用如图所示的自制装置进行“人体吸入和呼出气体成分”的探究。
【提出假设】人体呼出气体中二氧化碳的含量高于吸入气体中二氧化碳的含量
【进行实验】
(1)步骤I说明自制装置的气密性_______ (填“良好”或“不良”)。
(2)若装置气密性良好,将步骤I中“缓慢吹气”改为“缓慢吸气”,预期观察到的现象为_______ 。
(3)步骤Ⅱ中的现象_______ (填“能”或“不能”)证明呼出气体中二氧化碳的含量高于吸入气体中二氧化碳的含量,原因是______ 。
(4)步骤Ⅲ中,观察到______ (填现象),证明假设成立。

【提出假设】人体呼出气体中二氧化碳的含量高于吸入气体中二氧化碳的含量
【进行实验】
| 步骤 | 操作 | 现象 |
| I | 在饮料瓶中装水至没过长吸管底端,对着短吸管缓慢吹气 | 水从长吸管端快速流出 |
| Ⅱ | 将饮料瓶中装满水,对着短管吹气,用排水法收集呼出气体;将燃着的小木条快速伸入饮料瓶中 | 饮料瓶中木条熄灭 |
| Ⅲ | 将水倒掉,向饮料瓶中加入澄清石灰水至没过长吸管底,从短吸管端吸气30秒,观察石灰水的变化;再从长吸管端吹气30秒,观察石灰水的变化 |
(1)步骤I说明自制装置的气密性
(2)若装置气密性良好,将步骤I中“缓慢吹气”改为“缓慢吸气”,预期观察到的现象为
(3)步骤Ⅱ中的现象
(4)步骤Ⅲ中,观察到
您最近一年使用:0次



