解题方法
1 . 逻辑推理是化学学习中常用的一种思维方法,下列推理正确的是
| A.中和反应生成盐和水,而生成盐和水的反应不一定是中和反应 |
| B.物质在氧气中燃烧是氧化反应,所以所有的氧化反应都发光放热 |
| C.化学变化常常伴随有能量变化,所以有能量变化的一定是化学变化 |
| D.碱溶液的pH>7,所以pH>7的溶液一定是碱溶液 |
您最近一年使用:0次
解题方法
2 . 逻辑推理是学习化学的一种重要方法,下列推理正确的是
| A.中和反应生成盐和水,生成盐和水的反应一定是中和反应 |
| B.有机物都含有碳元素,所以含有碳元素的化合物一定是有机物 |
| C.酸性溶液能使紫色石蕊变红,能使紫色石蕊变红的溶液一定显酸性 |
| D.置换反应有单质和化合物生成,但有单质和化合物生成的反应不一定是置换反应 |
您最近一年使用:0次
解题方法
3 . 分析推理是化学学习中常用的思维方法。下列推理正确的是
| A.离子是带电的原子或原子团,因此带电的微粒一定是离子 |
| B.单质是由一种元素组成的,因此由一种元素组成的纯净物一定是单质 |
| C.质子数决定元素种类,所以质子数相同的粒子一定属于同种元素 |
| D.由一种分子构成的物质是纯净物,所以纯净物都是由一种分子构成的 |
您最近一年使用:0次
名校
解题方法
4 . 推理是化学学习中常用的思维方法,下列推理中正确的是
| A.化合物是由不同种元素组成的,所以由不同种元素组成的纯净物一定是化合物 |
| B.碱溶液能跟某些非金属氧化物反应,所以碱溶液能吸收CO气体 |
| C.溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数也一定减小 |
| D.阴离子都带负电荷,所以带负电荷的微粒都是阴离子 |
您最近一年使用:0次
5 . 推理和归纳是学习化学的重要方法。以下说法正确的是
| A.均一稳定的混合物是溶液,碘酒均一稳定,则碘酒属于溶液 |
| B.酸碱中和反应生成盐和水,则生成盐和水的反应都是中和反应 |
| C.碳酸盐与盐酸反应放出气体,则与盐酸反应放出气体的物质一定是碳酸盐 |
| D.碱溶液能使酚酞溶液变红,那么能使酚酞溶液变红的溶液一定是碱溶液 |
您最近一年使用:0次
解题方法
6 . 氢氧化钠溶液敞口放置在空气中,容易与空气中的二氧化碳气体反应而变质,兴趣小组同学欲探究氢氧化钠溶液变质后溶质的成分。
【提出问题】氢氧化钠溶液变质后溶质的成分是什么?
【猜想假设】猜想一:NaOH、Na2CO3;猜想二:Na2CO3
【设计实验】
(1)请完善下面的表格。
【反思评价】
(2)小明认为可用Ba(OH)2溶液代替步骤一中的BaCl2溶液进行实验,大家一致认为此方案不可行,理由是___________ 。
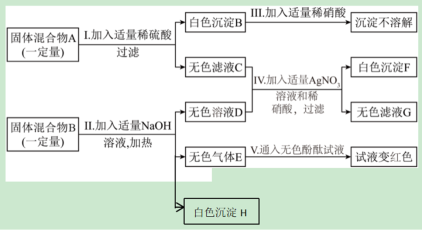
(3)已知某固体混合物中A中可能含有KNO3、Na2CO3、BaCl2、CuO四种物质中的两种,固体混合物中B中可能含有MgCl2、Fe2O3、NH4NO3、NH4Cl四种物质中的两种或多种。为探究固体混合物A、固体混合物B中的组成,按下图所示进行实验,出现的现象如图中所述。(设过程中所有发生的反应都恰好完全反应)
①无色气体E的化学式为___________ ,白色沉淀F为___________ (填化学式)。
②写出步骤Ⅰ中生成白色沉淀B的化学方程式为___________ 。
③在无色滤液G中一定含有的阳离子是___________ 。
④根据上述实验现象推断,在固体混合物A中,一定含有的物质是___________ (填化学式)。
⑤根据上述实验现象判断,在固体混合物B中NH4Cl___________ (一定或可能)存在;其理由是:___________ 。
【提出问题】氢氧化钠溶液变质后溶质的成分是什么?
【猜想假设】猜想一:NaOH、Na2CO3;猜想二:Na2CO3
【设计实验】
(1)请完善下面的表格。
| 实验方案及操作步骤 | 实验现象 | 实验结论 |
| 步骤一:取瓶中变质后的氢氧化钠溶液少量于试管中,加入足量BaCl2溶液充分反应,过滤。 | 产生白色沉淀 | 猜想一成立 |
| 步骤二:取步骤一中的滤液少量于试管中,向其中滴加 | 溶液变红色 |
【反思评价】
(2)小明认为可用Ba(OH)2溶液代替步骤一中的BaCl2溶液进行实验,大家一致认为此方案不可行,理由是
(3)已知某固体混合物中A中可能含有KNO3、Na2CO3、BaCl2、CuO四种物质中的两种,固体混合物中B中可能含有MgCl2、Fe2O3、NH4NO3、NH4Cl四种物质中的两种或多种。为探究固体混合物A、固体混合物B中的组成,按下图所示进行实验,出现的现象如图中所述。(设过程中所有发生的反应都恰好完全反应)
①无色气体E的化学式为
②写出步骤Ⅰ中生成白色沉淀B的化学方程式为
③在无色滤液G中一定含有的阳离子是
④根据上述实验现象推断,在固体混合物A中,一定含有的物质是
⑤根据上述实验现象判断,在固体混合物B中NH4Cl
您最近一年使用:0次
解题方法
7 . 推理是化学学习中常用的思维方式,下列推理正确的是
| A.碱溶液能使酚酞试液变红,则能使酚酞试液变红的溶液一定呈碱性 |
| B.溶液是均一稳定的混合物,则均一稳定的物质一定是溶液 |
| C.离子是带电的原子或原子团,所以带电的微粒一定是离子 |
| D.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
您最近一年使用:0次
解题方法
8 . 分析推理是化学学习中最常用的思维方法,下列说法正确的是
| A.离子是带电荷的粒子,则带电荷的粒子一定是离子 |
| B.氧化物中一定含有氧元素,则含有氧元素的化合物一定是氧化物 |
| C.燃烧有发光放热现象出现,则有发光放热现象的变化一定是燃烧 |
| D.碱性溶液能使酚酞溶液变红,则能使酚酞溶液变红的溶液一定呈碱性 |
您最近一年使用:0次
2024-04-20更新
|
75次组卷
|
4卷引用:2024年山东省德州市德城区一模化学试题
2024年山东省德州市德城区一模化学试题2024年山东省德州市陵城区九年级第一次练兵考试化学试题(已下线)2024年中考押题预测卷01(南京卷)-化学(已下线)2024年中考押题预测卷(苏州卷)-化学(含考试版、全解全析、参考答案、答题卡)
解题方法
9 . 纯碱是一种重要的化工原料,广泛用于玻璃、造纸、纺织和洗涤剂的生产。某化学兴趣小组对纯碱的制备、性质及用途等开展项目式学习。
任务一了解纯碱的制备——“侯氏制碱法”
“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收两种气体,生成碳酸氢钠和氯化铵(NH4Cl),再加热碳酸氢钠即可制得纯碱。碳酸氢钠溶解度较小,在反应后的溶液中通常以晶体形式析出。
(1)饱和氯化钠溶液吸收的两种气体是_______(填字母序号)。
(2)写出饱和氯化钠溶液吸收(1)中的两种气体生成碳酸氢钠和氯化铵的反应方程式_______ 。
任务二探究纯碱的性质——Na2CO3溶液呈碱性
【查阅资料】①溶液呈碱性,是因为溶液中存在较多的OH-。
②Na2CO3在水中全部解离出Na+和CO 。
。
③CaCl2溶液呈中性,Ca2+、Cl-对溶液的酸碱性没有影响。
【提出猜想】
(3)猜想一:H2O单独起作用,产生较多的OH-,使溶液呈碱性。
猜想二:Na+与H2O作用,产生较多的OH-,使溶液呈碱性。
猜想三:_______ 。
(4)【实验探究】
【解释与结论】同学们和老师交流,得知CO 和H2O作用,产生较多的OH-和另一种阴离子。
和H2O作用,产生较多的OH-和另一种阴离子。
【拓展与延伸】
(5)结合任务二的所有信息和结论,运用初中化学所学知识,经过分析推理可得出:Na2CO3溶液中含有的阴离子是_______ 。
任务三探究纯碱的用途——用于生产洗涤剂
【查阅资料】Na2CO3可用于生产洗涤剂。Na2CO3溶液呈碱性,可清洗油污,溶液碱性越强,去油污效果越好。
【实验探究】兴趣小组继续对影响Na2CO3溶液去油污效果的因素进行探究。
用不同温度的水,配制溶质质量分数分别为2%、6%和10%的Na2CO3溶液,并测定溶液pH,记录数据如表:
【解释与结论】
(6)实验①、②、③对比,可得出的结论是_______ 。
(7)要证明Na2CO3溶液的溶质质量分数变化与pH变化关系,可选择的3个实验的编号是_______ 。
【拓展与应用】
(8)下列物质可用于去油污的是_______(填字母序号)。
任务一了解纯碱的制备——“侯氏制碱法”
“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收两种气体,生成碳酸氢钠和氯化铵(NH4Cl),再加热碳酸氢钠即可制得纯碱。碳酸氢钠溶解度较小,在反应后的溶液中通常以晶体形式析出。
(1)饱和氯化钠溶液吸收的两种气体是_______(填字母序号)。
| A.Cl2 | B.NH3 | C.SO2 | D.CO2 |
任务二探究纯碱的性质——Na2CO3溶液呈碱性
【查阅资料】①溶液呈碱性,是因为溶液中存在较多的OH-。
②Na2CO3在水中全部解离出Na+和CO
 。
。③CaCl2溶液呈中性,Ca2+、Cl-对溶液的酸碱性没有影响。
【提出猜想】
(3)猜想一:H2O单独起作用,产生较多的OH-,使溶液呈碱性。
猜想二:Na+与H2O作用,产生较多的OH-,使溶液呈碱性。
猜想三:
(4)【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| (1)向试管中加入一定量的蒸馏水,滴入2滴酚酞溶液 | 溶液无明显变化 | 猜想一不成立 |
| (2)向试管中加入一定量的NaCl溶液,滴入2滴酚酞溶液 | 溶液无明显变化 | 猜想二不成立 |
| (3)①向试管中加入一定量的Na2CO3溶液,滴入2滴酚酞溶液 ②往①所得溶液中逐滴加入CaCl2溶液至过量 | ①溶液由无色变红色 ② | 猜想三成立 |
【解释与结论】同学们和老师交流,得知CO
 和H2O作用,产生较多的OH-和另一种阴离子。
和H2O作用,产生较多的OH-和另一种阴离子。【拓展与延伸】
(5)结合任务二的所有信息和结论,运用初中化学所学知识,经过分析推理可得出:Na2CO3溶液中含有的阴离子是
任务三探究纯碱的用途——用于生产洗涤剂
【查阅资料】Na2CO3可用于生产洗涤剂。Na2CO3溶液呈碱性,可清洗油污,溶液碱性越强,去油污效果越好。
【实验探究】兴趣小组继续对影响Na2CO3溶液去油污效果的因素进行探究。
用不同温度的水,配制溶质质量分数分别为2%、6%和10%的Na2CO3溶液,并测定溶液pH,记录数据如表:
| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
| 溶液温度(℃) | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 40 | 70 |
| 溶液pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
(6)实验①、②、③对比,可得出的结论是
(7)要证明Na2CO3溶液的溶质质量分数变化与pH变化关系,可选择的3个实验的编号是
【拓展与应用】
(8)下列物质可用于去油污的是_______(填字母序号)。
| A.NaCl | B.NaOH | C.K2CO3 | D.CaCO3 |
您最近一年使用:0次
解题方法
10 . 推理是学习化学重要的方法之一,下列叙述正确的是
| A.由氢离子和酸根离子构成的化合物是酸,所以酸中一定含有氢元素 |
| B.化合物含有多种元素,所以含有多种元素的物质一定是化合物 |
| C.浓盐酸敞口放置溶质质量分数会减小,是因为其与空气中的成分发生了化学反应 |
| D.酸溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的一定是酸溶液 |
您最近一年使用:0次



