名校
解题方法
1 . 工业制取碳化硅的化学反应方程式如下,请将方程式补充完整,并标出电子转移的方向数目:_______ 。
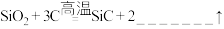
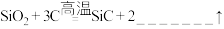
您最近一年使用:0次
2 . 写出钠和氯气的反应方程式,并分析得失电子情况,化合价的变化,以及指明氧化剂与还原剂______ 。
您最近一年使用:0次
解题方法
3 . 分析下列氧化还原反应中元素化合价变化情况,指出氧化剂和还原剂。
(1)
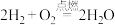
(2)

(3)
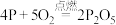
您最近一年使用:0次
解题方法
4 . 在四大基本反应类型中
您最近一年使用:0次
解题方法
5 . 铝热法是铝与某些金属氧化物反应获得高熔点金属单质的方法。工业上可用于制造无碳或低碳铁合金。铝粉和赤铁矿发生铝热反应的化学方程式为:Fe2O3+2Al 2Fe+Al2O3,在上述反应中,Al元素的化合价
2Fe+Al2O3,在上述反应中,Al元素的化合价___________ (填“升高”或“降低”),Al被___________ (填“氧化”或“还原”)。Fe2O3作___________ 剂,具有___________ 性。
 2Fe+Al2O3,在上述反应中,Al元素的化合价
2Fe+Al2O3,在上述反应中,Al元素的化合价
您最近一年使用:0次
解题方法
6 . 完成下列问题。
(1)在Fe3O4+4CO 3Fe+4CO2反应中,
3Fe+4CO2反应中,_______ 是氧化剂,_________ 是还原剂,_______ 元素被氧化,_______ 元素被还原,氧化产物是_______ 。
(2)在H+、Fe2+、Fe3+、S2-、S中,只有氧化性的是_______ ,只有还原性的是_______ ,即有氧化性又有还原性的是_______ 。
(1)在Fe3O4+4CO
 3Fe+4CO2反应中,
3Fe+4CO2反应中,(2)在H+、Fe2+、Fe3+、S2-、S中,只有氧化性的是
您最近一年使用:0次
解题方法
7 . 对于反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)MnO2在反应中___________ 电子(填“得到”或“失去”),所含元素化合价___________ (填“升高”或“降低”),发生___________ 反应(填“氧化”或“还原”)。
(2)HCl在反应中___________ 电子(填“得到”或“失去”),所含元素化合价___________ (填“升高”或“降低”),发生___________ 反应(填“氧化”或“还原”)。
(3)Fe+CuSO4=FeSO4+Cu。
①___________ (填元素)化合价降低,___________ (填物质)发生还原反应。
②___________ (填元素)化合价升高,___________ (填物质)发生氧化反应。
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(1)MnO2在反应中
(2)HCl在反应中
(3)Fe+CuSO4=FeSO4+Cu。
①
②
您最近一年使用:0次
解题方法
8 . 甲烷在空气中燃烧,甲烷发生了___ 反应。
您最近一年使用:0次
名校
解题方法
9 . 某汽车安全气囊的产气药主要含有KClO4、Fe2O3、NaHCO3、NaN3等物质。当汽车发生碰撞时,产气药产生大量气体使气囊迅速膨胀,从而起到保护作用。
回答下列问题:
(1)KClO4、Fe2O3、NaHCO3、NaN3四种物质中,属于氧化物的是___________ 。
(2)KClO4是助氧化剂,其中氯元素的化合价为___________ 。
(3)Fe2O3是主氧化剂,与Na发生置换反应,还原产物为___________ 。
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为___________ 。
(5)NaN3是气体发生剂,受热分解产生N2和Na,N2和Na的物质的量之比为___________ 。
回答下列问题:
(1)KClO4、Fe2O3、NaHCO3、NaN3四种物质中,属于氧化物的是
(2)KClO4是助氧化剂,其中氯元素的化合价为
(3)Fe2O3是主氧化剂,与Na发生置换反应,还原产物为
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为
(5)NaN3是气体发生剂,受热分解产生N2和Na,N2和Na的物质的量之比为
您最近一年使用:0次
10 . 水煤气因其燃烧速度快、抗爆性好等优点,广泛应用于燃料和化工原料。制备水煤气的主要反应方程式为: 。
。
(1)作还原剂的物质是_______ ,碳元素的化合价_____ (填“升高”或“降低”)。
(2)若反应中消耗了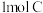 ,则生成CO的物质的量为
,则生成CO的物质的量为________ mol,转移电子的物质的量为______ mol。
 。
。(1)作还原剂的物质是
(2)若反应中消耗了
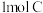 ,则生成CO的物质的量为
,则生成CO的物质的量为
您最近一年使用:0次



