2023高一上·全国·专题练习
解题方法
1 . 从元素化合价升降的角度认识氧化还原反应
(1)Fe+CuSO4=FeSO4+Cu。
①___________ 化合价降低,___________ 发生还原反应。
②___________ 化合价升高,___________ 发生氧化反应。
(2)结论:物质所含元素___________ 是氧化反应;物质所含元素___________ 是还原反应;凡是有___________ 的反应,都是氧化还原反应。
(1)Fe+CuSO4=FeSO4+Cu。
①
②
(2)结论:物质所含元素
您最近一年使用:0次
2 . I.已知:2Na+2H2O=2NaOH+H2↑
(1)用双线桥标出该反应中电子转移的方向和数目___________ 。
(2)该反应中___________ 被还原(填化学式)。
(3)请描述钠与水反应的实验现象___________ 。
Ⅱ.有反应:
(4)该反应所属的基本反应类型是___________ 。
(5)在反应中铁元素的化合价变化是___________ ,该元素的原子___________ (填“失去”或“得到”)电子。
(6)发生还原反应的是___________ (填化学式)。
(1)用双线桥标出该反应中电子转移的方向和数目
(2)该反应中
(3)请描述钠与水反应的实验现象
Ⅱ.有反应:

(4)该反应所属的基本反应类型是
(5)在反应中铁元素的化合价变化是
(6)发生还原反应的是
您最近一年使用:0次
2023-06-08更新
|
653次组卷
|
2卷引用:广东省揭阳市普宁市勤建学校2022-2023学年高一上学期第一次调研考试化学试题
解题方法
3 . 填空。
(1)在下列反应中,HCl作还原剂的是________ 为还原产物的是_______ (填序号,下同),HCl作氧化剂的是___________ 。
①K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
②Cl2+H2O=HCl+HClO
③2NaCl+H2SO4(浓) Na2SO4+2HCl↑
Na2SO4+2HCl↑
④Fe+2HCl=FeCl2+H2↑
(2)用双线桥法表明反应①中电子转移的方向和数目___________ 。
(3)下列变化中,涉及氧化还原反应的是___________ (填序号)。
①金属的冶炼②钢铁的锈蚀③食物的腐烂④澄清石灰水变浑浊
(4)下列4种基本类型的反应中,一定是氧化还原反应的是___________ (填序号),一定不是氧化还原反应的是___________ (填序号),可能是氧化还原反应的是___________ (填序号)。
①化合反应②分解反应③置换反应④复分解反应
(5)书写下列反应的离子方程式
①NaOH溶液和H2SO4溶液:___________ ;
②Fe与CuSO4溶液反应:___________ ;
③Na2CO3溶液与Ca(OH)2溶液反应:___________ 。
(1)在下列反应中,HCl作还原剂的是
①K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
②Cl2+H2O=HCl+HClO
③2NaCl+H2SO4(浓)
 Na2SO4+2HCl↑
Na2SO4+2HCl↑④Fe+2HCl=FeCl2+H2↑
(2)用双线桥法表明反应①中电子转移的方向和数目
(3)下列变化中,涉及氧化还原反应的是
①金属的冶炼②钢铁的锈蚀③食物的腐烂④澄清石灰水变浑浊
(4)下列4种基本类型的反应中,一定是氧化还原反应的是
①化合反应②分解反应③置换反应④复分解反应
(5)书写下列反应的离子方程式
①NaOH溶液和H2SO4溶液:
②Fe与CuSO4溶液反应:
③Na2CO3溶液与Ca(OH)2溶液反应:
您最近一年使用:0次
2023-06-07更新
|
621次组卷
|
3卷引用:广东实验中学附属江门学校2022-2023学年高一上学期期中考试化学试题
4 . 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中Na2O2是_______ (填氧化剂、还原剂)
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:_______ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为_______ mol
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中Na2O2是
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
您最近一年使用:0次
5 . 工业上常用绿矾( )做处理剂,处理废水中含有的重铬酸根离子(
)做处理剂,处理废水中含有的重铬酸根离子( ),反应的离子方程式如下:
),反应的离子方程式如下: 。
。
(1)在该反应中,氧化剂是_______ (填离子符号,下同),被氧化的是_______ 。
(2)该反应每消耗1mol 离子,生成
离子,生成 的物质的量为
的物质的量为_______ mol,转移电子的物质的量为_______ mol。
 )做处理剂,处理废水中含有的重铬酸根离子(
)做处理剂,处理废水中含有的重铬酸根离子( ),反应的离子方程式如下:
),反应的离子方程式如下: 。
。(1)在该反应中,氧化剂是
(2)该反应每消耗1mol
 离子,生成
离子,生成 的物质的量为
的物质的量为
您最近一年使用:0次
2023-01-07更新
|
402次组卷
|
2卷引用:北京市石景山区2022-2023学年高一上学期期末考试化学试题
名校
解题方法
6 . 根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题。
(1)氧化剂_______ ,还原剂_______
(2)氧化产物_______ ,还原产物_______
(3)用双线桥的方法表示该反应的电子转移情况_______
(1)氧化剂
(2)氧化产物
(3)用双线桥的方法表示该反应的电子转移情况
您最近一年使用:0次
名校
解题方法
7 . 化工厂用浓氨水检验氯气管道是否漏气,利用的反应如下: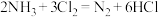 。
。
(1)作还原剂的物质是_______ ,氯元素的化合价_______ (填“升高”或“降低”)。
(2)如果在反应中每生成6个HCl分子,则消耗Cl2的分子个数是_______ ,转移电子的数目为_______ 个。
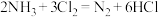 。
。(1)作还原剂的物质是
(2)如果在反应中每生成6个HCl分子,则消耗Cl2的分子个数是
您最近一年使用:0次
解题方法
8 . 用双线桥表示下列氧化还原反应的情况:
(1)Zn + 2HCl = ZnCl2 + H2 ↑_________ 。
(2)2Al + 3CuSO4 = 3Cu + Al2(SO4)3_________ 。
(3)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O_________ 。
(4)2Na2O2 + 2H2O = 4NaOH + O2↑_________ 。
(1)Zn + 2HCl = ZnCl2 + H2 ↑
(2)2Al + 3CuSO4 = 3Cu + Al2(SO4)3
(3)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(4)2Na2O2 + 2H2O = 4NaOH + O2↑
您最近一年使用:0次
解题方法
9 . I.分析下列氧化还原反应的电子转移方向和数目,并指出氧化剂和还原剂。
(1)Zn+CuSO4=ZnSO4+Cu_______
(2)Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2_______
(3)4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O_______
II.分析下列反应并按要求填空。
(4)2Fe+3Cl2 2FeCl3
2FeCl3
氧化剂是_______ ,还原剂是_______ ;发生氧化反应的是_______ ,发生还原反应的是_______ 。
(5)
氧化剂是_______ ,还原剂是_______ ;被氧化的元素是_______ ,被还原的元素是_______ 。
(6)2H2S+SO2=3S↓+2H2O
氧化剂是_______ ,还原剂是_______ ;氧化产物是_______ ,还原产物是_______ 。
(1)Zn+CuSO4=ZnSO4+Cu
(2)Fe2O3+3CO
 2Fe+3CO2
2Fe+3CO2(3)4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2OII.分析下列反应并按要求填空。
(4)2Fe+3Cl2
 2FeCl3
2FeCl3氧化剂是
(5)

氧化剂是
(6)2H2S+SO2=3S↓+2H2O
氧化剂是
您最近一年使用:0次
解题方法
10 . 指出下列反应的氧化剂和还原剂
(1)2H2+O2=2H2O:氧化剂_______ ;还原剂_______ 。
(2)4P+5O2=2P2O5:氧化剂_______ ;还原剂_______ 。
(3)Fe+H2SO4=FeSO4+H2:氧化剂_______ ;还原剂_______ 。
(4)WO3+3H2=W+3H2O:氧化剂_______ ;还原剂_______ 。
(1)2H2+O2=2H2O:氧化剂
(2)4P+5O2=2P2O5:氧化剂
(3)Fe+H2SO4=FeSO4+H2:氧化剂
(4)WO3+3H2=W+3H2O:氧化剂
您最近一年使用:0次



