1 . 下列“实验操作及事实”与“实验结论”相符的一组是
| A.蓝色石蕊试纸上滴加新制氯水先变红后褪色,则新制氯水无酸性只有漂白性 |
B.向 溶液中加入少量铜粉固体溶解,则氧化性: 溶液中加入少量铜粉固体溶解,则氧化性: |
C.金属钠在空气中燃烧后生成淡黄色固体,该淡黄色固体是 |
| D.向某固体中加入稀盐酸产生气泡,该固体一定是碳酸盐 |
您最近一年使用:0次
名校
2 . 某化合物的结构如下图所示。已知W、X、Y、Z为原子序数依次增大的短周期元素,W、X的原子序数之和等于Y的原子序数,Z的最外层电子数等于X的原子序数。下列说法中,不正确的是


| A.Z元素可能位于第三周期 |
| B.该化合物分子中X、Y、Z原子都满足8电子结构 |
| C.X、Y、Z分别与W形成的化合物都不含非极性共价键 |
| D.在一定条件下,X、Z分别与W形成的简单化合物均能与氯气反应 |
您最近一年使用:0次
2023-05-01更新
|
522次组卷
|
2卷引用:吉林省延边第一中学2023-2024学年高三上学期第二次模考化学试题
3 . 近年我国在科学技术领域取得了举世瞩目的成就。对下列成就的相关叙述中错误的是
A.核电站反应堆所用铀棒中含有的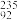 U与 U与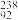 U互为同位素 U互为同位素 |
| B.冬奥会场馆使用CO2跨临界直冷制冰属于化学变化 |
| C.国家速滑馆“冰丝带”主体结构中大量使用的钢属于金属材料 |
| D.“天宫课堂”制备的纳米材料分散到水中,形成分散质粒子直径为1~100nm的分散系属于胶体 |
您最近一年使用:0次
解题方法
4 . 如图是铁及其化合物的“价—类”二维图,下列有关叙述正确的是
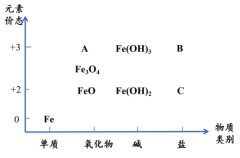

| A.Fe3O4为磁铁矿的主要成分,其中铁元素的化合价为+3价 |
| B.可用酸性KMnO4溶液检验C中阳离子 |
| C.A为黑色晶体,常用于涂料的生产 |
| D.C转化为B的反应类型为复分解反应 |
您最近一年使用:0次
解题方法
5 . 下列说法正确的是
| A.新制的氯水可保存在无色玻璃试剂瓶中 |
| B.氯气、次氯酸、次氯酸盐均具有漂白性,可以用于漂白各种产品 |
| C.氢气在氯气中安静地燃烧,火焰呈苍白色,瓶口有白雾 |
| D.氯气、液氯、氯水是同一种物质,均可以储存在钢瓶中 |
您最近一年使用:0次
解题方法
6 . 某化学兴趣小组同学利用以下装置制备干燥的氯气并对氯气的性质进行探究。
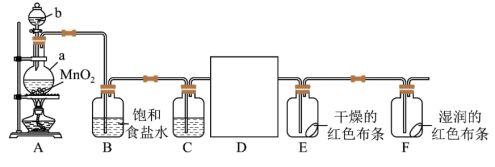
(1)A装置中b仪器名称_____ 。
(2)仪器a中发生反应的离子方程式为_____ ,D为收集干燥的氯气仪器,可以选择_____ (填序号)。

(3)下列有关该实验的说法中不正确的是______ (填字母)。
a.B中饱和食盐水主要作用之一是除去氯气中的氯化氢气体
b.C中试剂是浓硫酸,目的是干燥氯气
c.E中红色布条不褪色,F中红色布条褪色,证明氯气具有漂白性
d.尾气处理时,所用试剂可以选用澄清石灰水
(4)新冠肺炎疫情期间,“84消毒液”被广泛应用于物体表面杀菌消毒。制备“84消毒液”的化学反应方程式为______ 。
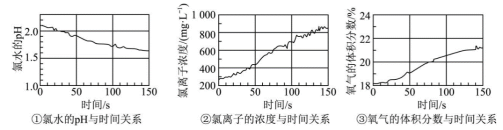
(5)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:_____ 。
(6)该兴趣小组在40℃条件下,将一定量的Cl2通入一定量的NaOH溶液中,得到的产物中含有NaCl、NaClO和NaClO3,已知Cl-和ClO-的个数比为8:3,则此过程中氧化剂和还原剂的个数之比为_____ 。

(1)A装置中b仪器名称
(2)仪器a中发生反应的离子方程式为

(3)下列有关该实验的说法中不正确的是
a.B中饱和食盐水主要作用之一是除去氯气中的氯化氢气体
b.C中试剂是浓硫酸,目的是干燥氯气
c.E中红色布条不褪色,F中红色布条褪色,证明氯气具有漂白性
d.尾气处理时,所用试剂可以选用澄清石灰水
(4)新冠肺炎疫情期间,“84消毒液”被广泛应用于物体表面杀菌消毒。制备“84消毒液”的化学反应方程式为
(5)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:

(6)该兴趣小组在40℃条件下,将一定量的Cl2通入一定量的NaOH溶液中,得到的产物中含有NaCl、NaClO和NaClO3,已知Cl-和ClO-的个数比为8:3,则此过程中氧化剂和还原剂的个数之比为
您最近一年使用:0次
解题方法
7 . 实验室配制480mL0.2mol/L的NaOH溶液并探究NaOH的部分性质,实验如下:
(1)需用托盘天平称量NaOH固体______ g。
(2)下列的实验操作可能导致配制的溶液浓度偏低的是_____ 。
a.容量瓶内原来存有少量的水 b.定容时液面超过刻度线,用胶头滴管吸出
c.没有洗涤烧杯和玻璃棒 d.定容时俯视刻度线
(3)取一定体积该溶液于试管中,再向其中通入一定量的CO2气体,充分反应后向所得溶液中逐滴加入1mol/L盐酸,所加入盐酸溶液的体积与产生CO2气体体积(标准状况)的关系如图所示:
①当盐酸的体积加入到35mL时,所得溶液中所含溶质为______ (填化学式),溶质的物质的量之比为_____ 。
②写出AB段所发生反应的离子方程式______ 。
(4)下列有关Na2CO3、NaHCO3和Na2O2的说法中不正确的是_____ 。
a.相同条件下的溶解度:Na2CO3>NaHCO3
b.Na2O2中阳离子与阴离子个数比1:1
c.可以用通入足量CO2的方法除去NaHCO3溶液中的Na2CO3杂质
d.mgNa2CO3和mgNaHCO3固体中分别加入几滴水后,测得温度较高的是Na2CO3
(1)需用托盘天平称量NaOH固体
(2)下列的实验操作可能导致配制的溶液浓度偏低的是
a.容量瓶内原来存有少量的水 b.定容时液面超过刻度线,用胶头滴管吸出
c.没有洗涤烧杯和玻璃棒 d.定容时俯视刻度线
(3)取一定体积该溶液于试管中,再向其中通入一定量的CO2气体,充分反应后向所得溶液中逐滴加入1mol/L盐酸,所加入盐酸溶液的体积与产生CO2气体体积(标准状况)的关系如图所示:
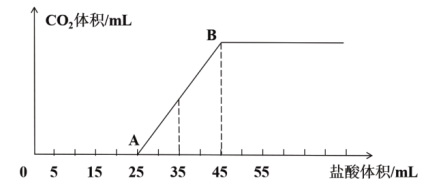
①当盐酸的体积加入到35mL时,所得溶液中所含溶质为
②写出AB段所发生反应的离子方程式
(4)下列有关Na2CO3、NaHCO3和Na2O2的说法中不正确的是
a.相同条件下的溶解度:Na2CO3>NaHCO3
b.Na2O2中阳离子与阴离子个数比1:1
c.可以用通入足量CO2的方法除去NaHCO3溶液中的Na2CO3杂质
d.mgNa2CO3和mgNaHCO3固体中分别加入几滴水后,测得温度较高的是Na2CO3
您最近一年使用:0次
名校
解题方法
8 . 为探究“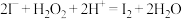 ”碘离子氧化过程进行如下实验.
”碘离子氧化过程进行如下实验.
下列说法不正确的是
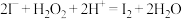 ”碘离子氧化过程进行如下实验.
”碘离子氧化过程进行如下实验.编号 | 1 | 2 |
实验内容 |
|
|
实验现象 | 随着液体不断滴入,产生大量气体;溶液变黄并不断加深至棕黄色后又变浅 | 随着液体不断滴入,溶液变黄,摇匀后又褪色,不断重复直至析出紫色沉淀 |
A.实验1中溶液变浅是因为 |
B.实验2中出现紫色沉淀是因为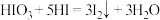 |
C.实验1中产生大量气体的原因是 被氧化的过程大量放热 被氧化的过程大量放热 |
| D.实验2相较于实验1,可节约H2O2用量且有利于反应终点观察 |
您最近一年使用:0次
2023-03-08更新
|
800次组卷
|
3卷引用:2024届吉林省延边州高三教学质量检测(一模)化学试题
名校
解题方法
9 . 向含废水中加入 ,铁元素会形成如图所示的
,铁元素会形成如图所示的 胶团,在静电吸附作用下,胶团可以除去废水中的
胶团,在静电吸附作用下,胶团可以除去废水中的 价砷元素,下列说法正确的是
价砷元素,下列说法正确的是

 ,铁元素会形成如图所示的
,铁元素会形成如图所示的 胶团,在静电吸附作用下,胶团可以除去废水中的
胶团,在静电吸附作用下,胶团可以除去废水中的 价砷元素,下列说法正确的是
价砷元素,下列说法正确的是
| A.废水中的含砷微粒是带正电荷的离子 |
B.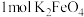 可以形成的胶团数目小于 可以形成的胶团数目小于 |
C.增大废水的 , , 胶粒的吸附絮凝效能提升 胶粒的吸附絮凝效能提升 |
D. 可以还原废水中的含砷微粒到 可以还原废水中的含砷微粒到 价 价 |
您最近一年使用:0次
2022-12-09更新
|
1232次组卷
|
5卷引用:吉林省延边第一中学2023届高三下学期第七次模拟考试理科综合化学试题
名校
解题方法
10 . 草酸亚铁晶体(FeC2O4•2H2O)常用作生产锂电池、涂料、着色剂以及感光材料的原材料,难溶于水,受热易分解。
I.制备草酸亚铁晶体:
①称取硫酸亚铁铵晶体5g,放入250mL三颈烧瓶中,加入10滴左右1.0mol•L-1H2SO4溶液和15mL蒸馏水加热溶解;
②加入25mL饱和草酸溶液,加热搅拌至沸腾停止加热,静置;
③待黄色晶体FeC2O4•2H2O沉淀后倾析,洗涤,加入约20mL蒸馏水搅拌并温热5min,静置,弃去上层清液,即得黄色草酸亚铁晶体。

(1)B的名称是____ ;B的出水口是____ (填“上口”或“下口”)。
(2)硫酸亚铁铵晶体中可能混有Fe3+,检验其是否含有Fe3+的试剂是____ 溶液,若混有Fe3+,观察到的现象是____ 。
II.将一定质量的草酸亚铁晶体(FeC2O4•2H2O)在氩气气氛中进行热重分析示意图(TG%表示残留固体质量占原样品总质量的百分数)。

(3)B处时残留物的化学式为____ 。
(4)取上述分解得到的600℃时的固体放在空气中继续加热时其质量增加,发生反应的化学方程式为____ 。
I.制备草酸亚铁晶体:
①称取硫酸亚铁铵晶体5g,放入250mL三颈烧瓶中,加入10滴左右1.0mol•L-1H2SO4溶液和15mL蒸馏水加热溶解;
②加入25mL饱和草酸溶液,加热搅拌至沸腾停止加热,静置;
③待黄色晶体FeC2O4•2H2O沉淀后倾析,洗涤,加入约20mL蒸馏水搅拌并温热5min,静置,弃去上层清液,即得黄色草酸亚铁晶体。

(1)B的名称是
(2)硫酸亚铁铵晶体中可能混有Fe3+,检验其是否含有Fe3+的试剂是
II.将一定质量的草酸亚铁晶体(FeC2O4•2H2O)在氩气气氛中进行热重分析示意图(TG%表示残留固体质量占原样品总质量的百分数)。

(3)B处时残留物的化学式为
(4)取上述分解得到的600℃时的固体放在空气中继续加热时其质量增加,发生反应的化学方程式为
您最近一年使用:0次
2022-10-29更新
|
177次组卷
|
4卷引用:吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题





