名校
解题方法
1 . 某种钾盐具有鲜艳的颜色,其阴离子结构如图所示。X、Y、Z为原子序数依次增加的短周期元素,X的一种同位素可以用于测定文物的年代,Y的一种氧化物是红棕色气体,Z的最高化合价与最低化合价的代数和为4,W在自然界中的含量位居第四。下列说法正确的是

| A.W的化合价为+3 |
| B.原子半径:Z>Y>X |
| C.Y的氧化物对应的水化物一定为强酸 |
| D.在该阴离子中,所有原子均满足最外层8电子结构 |
您最近一年使用:0次
解题方法
2 . 硫酸四氨合铜(Ⅱ)晶体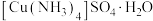 为深蓝色,易溶于水,不溶于乙醇等有机溶剂,加热时易失氨。某研究小组拟用粗
为深蓝色,易溶于水,不溶于乙醇等有机溶剂,加热时易失氨。某研究小组拟用粗 (含少量
(含少量 )合成硫酸四氨合铜晶体并测定其纯度。
)合成硫酸四氨合铜晶体并测定其纯度。
I.硫酸四氨合铜(Ⅱ)晶体制备与提纯
步骤①:称取 粗
粗 倒入烧杯中,加入适量稀硫酸溶解,将溶液加热至沸腾,边搅拌边逐滴加入
倒入烧杯中,加入适量稀硫酸溶解,将溶液加热至沸腾,边搅拌边逐滴加入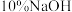 溶液至pH为3.5,继续加热溶液片刻,趁热过滤,得到
溶液至pH为3.5,继续加热溶液片刻,趁热过滤,得到 溶液。
溶液。
步骤②:___________ ,调pH为3.5的目的是___________ 。
(2)写出操作①中发生的离子反应方程式___________ 。
(3)操作③中洗涤步骤中可选用的洗涤液是___________ 。
A.乙醇与乙醚的混合液 B.蒸馏水 C.饱和硫酸钠溶液
(4)某同学认为操作②也可以通过蒸发浓缩、冷却结晶获得所要晶体,你___________ (填“是”或“否”)同意他的观点,并说明理由___________ 。
Ⅱ.硫酸四氨合铜(Ⅱ)晶体纯度测定
步骤①:准确称取 固体于烧杯中,加稀硫酸溶解,配制为
固体于烧杯中,加稀硫酸溶解,配制为 的溶液。
的溶液。
步骤②:量取上述试液 于锥形瓶中,加入
于锥形瓶中,加入 水和KI固体(稍过量)
水和KI固体(稍过量)
步骤③:用 标准溶液(
标准溶液( )滴定至溶液呈淡黄色,加入淀粉溶液
)滴定至溶液呈淡黄色,加入淀粉溶液 ,溶液变为蓝色,再加入
,溶液变为蓝色,再加入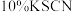 溶液
溶液 ,继续用
,继续用 标准溶液滴定至蓝色刚好消失,重复操作3次,平均用量为
标准溶液滴定至蓝色刚好消失,重复操作3次,平均用量为 。
。
已知:①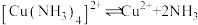 ,
,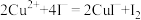 ,
, 沉淀表面易吸附
沉淀表面易吸附 。
。
② 比
比 更难溶。③
更难溶。③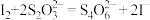 。
。
(5)硫酸四氨合铜晶体纯度是___________ (写出用m、V表示的计算表达式。)。
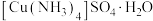 为深蓝色,易溶于水,不溶于乙醇等有机溶剂,加热时易失氨。某研究小组拟用粗
为深蓝色,易溶于水,不溶于乙醇等有机溶剂,加热时易失氨。某研究小组拟用粗 (含少量
(含少量 )合成硫酸四氨合铜晶体并测定其纯度。
)合成硫酸四氨合铜晶体并测定其纯度。I.硫酸四氨合铜(Ⅱ)晶体制备与提纯
步骤①:称取
 粗
粗 倒入烧杯中,加入适量稀硫酸溶解,将溶液加热至沸腾,边搅拌边逐滴加入
倒入烧杯中,加入适量稀硫酸溶解,将溶液加热至沸腾,边搅拌边逐滴加入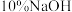 溶液至pH为3.5,继续加热溶液片刻,趁热过滤,得到
溶液至pH为3.5,继续加热溶液片刻,趁热过滤,得到 溶液。
溶液。步骤②:

(2)写出操作①中发生的离子反应方程式
(3)操作③中洗涤步骤中可选用的洗涤液是
A.乙醇与乙醚的混合液 B.蒸馏水 C.饱和硫酸钠溶液
(4)某同学认为操作②也可以通过蒸发浓缩、冷却结晶获得所要晶体,你
Ⅱ.硫酸四氨合铜(Ⅱ)晶体纯度测定
步骤①:准确称取
 固体于烧杯中,加稀硫酸溶解,配制为
固体于烧杯中,加稀硫酸溶解,配制为 的溶液。
的溶液。步骤②:量取上述试液
 于锥形瓶中,加入
于锥形瓶中,加入 水和KI固体(稍过量)
水和KI固体(稍过量)步骤③:用
 标准溶液(
标准溶液( )滴定至溶液呈淡黄色,加入淀粉溶液
)滴定至溶液呈淡黄色,加入淀粉溶液 ,溶液变为蓝色,再加入
,溶液变为蓝色,再加入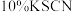 溶液
溶液 ,继续用
,继续用 标准溶液滴定至蓝色刚好消失,重复操作3次,平均用量为
标准溶液滴定至蓝色刚好消失,重复操作3次,平均用量为 。
。已知:①
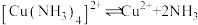 ,
,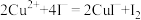 ,
, 沉淀表面易吸附
沉淀表面易吸附 。
。②
 比
比 更难溶。③
更难溶。③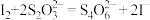 。
。(5)硫酸四氨合铜晶体纯度是
您最近一年使用:0次
名校
解题方法
3 . 主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Y最外层电子数之和为11,W与Y同族且都是复合化肥的营养元素,Z的氢化物遇水可产生最轻的气体。下列说法正确的是
| A.X的氧化物所含化学键类型相同 |
| B.Y和W最高价氧化物水化物的酸性:Y>W |
| C.Z的金属性比X弱 |
| D.简单离子半径最大的是Y |
您最近一年使用:0次
名校
4 . 前四周期元素X、Y、Z、W、Q原子序数依次增大,其中Y、Z同周期,Z、W同主族;X、Y、Z是人体内含量最高的三种元素,X、Y、Z、W、Q五原子核外电子数之和为51。下列叙述合理的是
A.原子半径 |
| B.X、Y形成的化合物沸点低于X、Z形成的化合物 |
| C.这些元素组成的三元化合物都可溶于水 |
D. 的一种化合物常加于煤中,避免煤燃烧产生的 的一种化合物常加于煤中,避免煤燃烧产生的 的某种氧化物污染空气 的某种氧化物污染空气 |
您最近一年使用:0次
2024-06-04更新
|
211次组卷
|
2卷引用:2024届四川省成都市第七中学高三下学期5月模拟考试理科综合试题-高中化学
名校
解题方法
5 . 某小组同学为探究FeSO4的性质设计了如下实验。
Ⅰ.新配制0.1 mol·L−1 FeSO4溶液450 mL:
(1)配制0.1 mol·L−1 FeSO4溶液450 mL,需用托盘天平准确称取绿矾(FeSO4·7H2O)
_______ g,其部分实验操作示意图如下,正确的步骤顺序为_______ (填序号)。
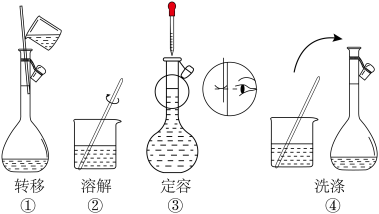
Ⅱ.取2 mL新配制的FeSO4溶液,按下图进行实验并观察到如下现象:
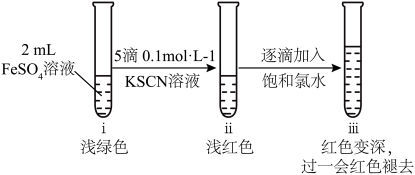
(2)ⅱ中溶液呈浅红色,说明FeSO4溶液中存在_______ (填离子符号)。
(3)ⅲ中溶液红色变深的主要原因是_______ (用离子方程式表示)。
Ⅲ.探究ⅲ中“红色褪去”的原因:
查阅资料:SCN−具有还原性,能被氯气氧化为(SCN)2。
根据查阅资料,甲、乙两位同学提出了如下猜想:
(4)乙同学的猜想是_______ 。为验证甲、乙两位同学的猜想,设计如下实验:将褪色后的溶液分为两等份,一份滴加KSCN溶液,呈血红色;另一份加入氯化铁溶液,无明显现象,则_______ 同学猜想是正确的。
Ⅳ.丙和丁同学探究无水FeSO4在450 ℃、不同氛围中的分解产物:
① 丙同学在450 ℃、空气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体m g,产生的气体通入品红溶液,无明显变化,通入氯化钡溶液中有白色沉淀生成;
② 丁同学在450 ℃、氮气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体也是m g,产生的气体依次通入氯化钡溶液和品红溶液,氯化钡溶液中有白色沉淀,品红溶液褪色。
(5)则m =_______ g,FeSO4固体在空气氛围中加热时反应的化学方程式为_______ 。
Ⅰ.新配制0.1 mol·L−1 FeSO4溶液450 mL:
(1)配制0.1 mol·L−1 FeSO4溶液450 mL,需用托盘天平准确称取绿矾(FeSO4·7H2O)

Ⅱ.取2 mL新配制的FeSO4溶液,按下图进行实验并观察到如下现象:

(2)ⅱ中溶液呈浅红色,说明FeSO4溶液中存在
(3)ⅲ中溶液红色变深的主要原因是
Ⅲ.探究ⅲ中“红色褪去”的原因:
查阅资料:SCN−具有还原性,能被氯气氧化为(SCN)2。
根据查阅资料,甲、乙两位同学提出了如下猜想:
| 猜想 | |
| 甲 | +3价铁又被还原成+2价铁 |
| 乙 |
(4)乙同学的猜想是
Ⅳ.丙和丁同学探究无水FeSO4在450 ℃、不同氛围中的分解产物:
① 丙同学在450 ℃、空气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体m g,产生的气体通入品红溶液,无明显变化,通入氯化钡溶液中有白色沉淀生成;
② 丁同学在450 ℃、氮气氛围中加热15.2 g FeSO4,直至固体质量不变,得到纯净的红棕色固体也是m g,产生的气体依次通入氯化钡溶液和品红溶液,氯化钡溶液中有白色沉淀,品红溶液褪色。
(5)则m =
您最近一年使用:0次
2024-06-01更新
|
162次组卷
|
2卷引用:2024届四川省成都市蓉城名校联盟高三下学期第三次模拟考试理科综合试题-高中化学
名校
解题方法
6 . 已知甲、乙、丙、丁、戊是元素周期表中原子序数依次增大的短周期主族元素,它们的最外层电子数之和是27,甲和丁、乙和戊同主族,甲和乙同周期且相邻。下列说法错误的是
| A.简单离子还原性强弱顺序:乙 > 戊 > 丁 |
| B.简单离子半径大小顺序:甲 > 乙 > 丙 |
| C.氢化物的稳定性不一定是:甲 > 丁 |
| D.甲和丙可形成既含共价键又含离子键的离子化合物 |
您最近一年使用:0次
2024-06-01更新
|
134次组卷
|
2卷引用:2024届四川省成都市蓉城名校联盟高三下学期第三次模拟考试理科综合试题-高中化学
名校
解题方法
7 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.将1molCl2通入足量水中,转移的电子数为NA |
| B.常温常压下,11.2LN2含有的原子数大于NA |
C.1 mol·L−1NaHSO4溶液中含有的 数目为NA 数目为NA |
| D.总质量为2.0 g的H218O和D2O的物质中含有的中子数为NA |
您最近一年使用:0次
2024-06-01更新
|
194次组卷
|
2卷引用:2024届四川省成都市蓉城名校联盟高三下学期第三次模拟考试理科综合试题-高中化学
名校
8 . 化合物A 是一种重要的医药中间体,由原子序数依次增大的W、X、Y、Z 四种短周期元素组成,其结构如图所示,下列有关说法不正确的是
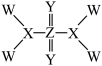
| A.X、Y形成的原子个数之比为1:2的二元化合物有2种 |
| B.X、Y、Z分别形成的简单氢化物中,Y的氢化物沸点最高 |
| C.简单离子半径大小:Z>X>Y |
| D.Z的低价态氧化物能使氧化漂白石蕊溶液 |
您最近一年使用:0次
名校
9 . 由重晶石矿(主要成分是 ,含
,含 等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
 ,含
,含 等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是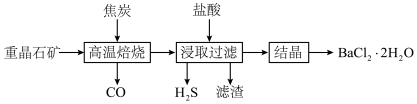
| A.“高温焙烧”前将原料研磨处理,能加快“高温焙烧”的反应速率 |
B.“高温焙烧”时只有 被C还原 被C还原 |
| C.“浸取过滤”发生的主要反应是氧化还原反应 |
| D.“高温焙烧”和“结晶”两处操作均需用到蒸发皿 |
您最近一年使用:0次
名校
解题方法
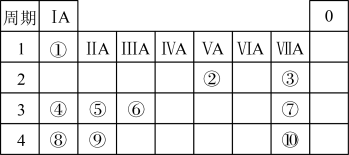
10 . 下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。针对表中①~⑩号元素回答下列问题。______ ,⑨元素的原子结构示意图为______ 。
(2)②、③、④、⑤、⑥这五种元素分别形成的简单离子中离子半径最小的是______ (填离子符号)。
(3)镓(Ga)与⑥同主族,其氢氧化物为两性氢氧化物,请写出氢氧化镓与NaOH反应的化学方程式______ 。
(4)表中元素⑦和⑩的最高价氧化物对应水化物的酸性最强的是______ (填化学式)。
(5)元素④和⑥相比,金属性较强的是______ (填元素符号),下列能证明这一事实的有______ (填序号)。
A.在化合物中④的化合价比⑥的低
B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强
D.④单质的熔点比⑥单质的低
(2)②、③、④、⑤、⑥这五种元素分别形成的简单离子中离子半径最小的是
(3)镓(Ga)与⑥同主族,其氢氧化物为两性氢氧化物,请写出氢氧化镓与NaOH反应的化学方程式
(4)表中元素⑦和⑩的最高价氧化物对应水化物的酸性最强的是
(5)元素④和⑥相比,金属性较强的是
A.在化合物中④的化合价比⑥的低
B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强
D.④单质的熔点比⑥单质的低
您最近一年使用:0次



