1 . 下列关于 的说法不正确的是
的说法不正确的是
 的说法不正确的是
的说法不正确的是A. 的电子式为 的电子式为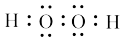 |
B. 是一种绿色氧化剂的原因是氧化产物为 是一种绿色氧化剂的原因是氧化产物为 |
C. 能杀菌消毒的原理是 能杀菌消毒的原理是 的氧化性 的氧化性 |
D. 的漂白原理与 的漂白原理与 的漂白原理不同 的漂白原理不同 |
您最近一年使用:0次
2 . 光照下,氧化锌纳米棒具有优异的光催化活性,可用于制备过氧化氢,反应机理如图所示( 表示电子跃迁产生的空穴)。下列叙述错误的是
表示电子跃迁产生的空穴)。下列叙述错误的是
 表示电子跃迁产生的空穴)。下列叙述错误的是
表示电子跃迁产生的空穴)。下列叙述错误的是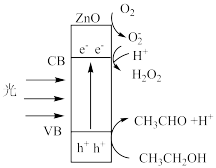
| A.反应过程中吸收了光能,说明总反应为吸热反应 |
B.中间体 含有单电子,结构不稳定、反应活性强 含有单电子,结构不稳定、反应活性强 |
C.理论上生成 和 和 的物质的量之比为1:1 的物质的量之比为1:1 |
D.乙醇发生的反应可表示为 |
您最近一年使用:0次
3 . 应用元素周期律分析下列推断,其中正确的是
| A.硒(Se)位于元素周期表的第VIA族,其最高价氧化物对应水化物的酸性比硫酸弱 |
| B.气态氢化物的稳定性HF弱于HCl |
| C.铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应 |
| D.第二周期非金属元素的气态氢化物溶于水后,水溶液均呈酸性 |
您最近一年使用:0次
4 . 下列化合物不能由两种单质直接化合而成的是
①CuS ② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
①CuS ②
 ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
| A.②④⑥ | B.②④⑥⑦ | C.①③⑤ | D.①③⑤⑦ |
您最近一年使用:0次
5 . 联合多种工业制备是节能环保,高效生产,减少损耗的重要途径。钛和钛合金性能优良,广泛用于航空、造船和化学工业中。以钛铁矿(主要成分为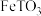 (其中
(其中 为
为 价),含有少量
价),含有少量 、
、 )为主要原料制取
)为主要原料制取 单质和绿矾
单质和绿矾 ,同时联合氯碱工业生产甲醇的工艺流程如图1所示。
,同时联合氯碱工业生产甲醇的工艺流程如图1所示。
回答下列问题:
(1)酸浸后,溶液中钛元素主要以 形式存在,则在酸浸工序中发生的主要反应的化学方程式为
形式存在,则在酸浸工序中发生的主要反应的化学方程式为______ 。
(2)某化学兴趣小组在实验室模拟该工艺流程,保持其他反应条件不变,测得加入铁屑还原体系中 (Ⅲ)含量随反应温度的变化如图2所示。为达到实验目的,最佳反应温度为
(Ⅲ)含量随反应温度的变化如图2所示。为达到实验目的,最佳反应温度为______ 。______ (填标号)。
a.工序①为趁热过滤、洗涤、干燥
b.先用适量稀硫酸洗涤绿矾并将洗涤液与滤液合并,可提高钛的产率
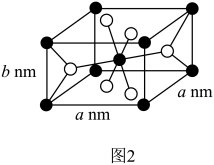
(4)灼烧后的成分为 ,可用作钛白颜料,该物质的一种晶胞结构(四方晶体)如图3所示。该晶体的密度为
,可用作钛白颜料,该物质的一种晶胞结构(四方晶体)如图3所示。该晶体的密度为______  (用含
(用含 、
、 、
、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(5)工序②生成的气体 为可燃性气体,生成气体
为可燃性气体,生成气体 的反应方程式为
的反应方程式为______ 。
(6)还原工序中通入氩气的目的是______ 。
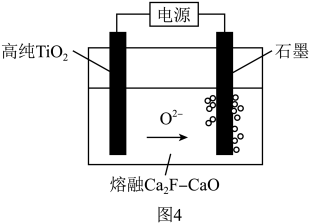
(7)利用图4装置可获得金属钛。在较低的阴极电位下, 中的氧解离进入熔融盐,最后只剩下纯钛,另一极产生
中的氧解离进入熔融盐,最后只剩下纯钛,另一极产生 、
、 和可燃性气体
和可燃性气体 。产生可燃性气体
。产生可燃性气体 的电极反应式为
的电极反应式为______ 。
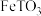 (其中
(其中 为
为 价),含有少量
价),含有少量 、
、 )为主要原料制取
)为主要原料制取 单质和绿矾
单质和绿矾 ,同时联合氯碱工业生产甲醇的工艺流程如图1所示。
,同时联合氯碱工业生产甲醇的工艺流程如图1所示。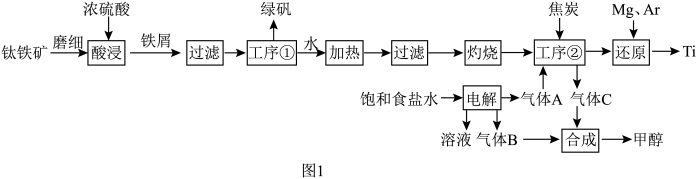

回答下列问题:
(1)酸浸后,溶液中钛元素主要以
 形式存在,则在酸浸工序中发生的主要反应的化学方程式为
形式存在,则在酸浸工序中发生的主要反应的化学方程式为(2)某化学兴趣小组在实验室模拟该工艺流程,保持其他反应条件不变,测得加入铁屑还原体系中
 (Ⅲ)含量随反应温度的变化如图2所示。为达到实验目的,最佳反应温度为
(Ⅲ)含量随反应温度的变化如图2所示。为达到实验目的,最佳反应温度为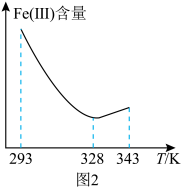
a.工序①为趁热过滤、洗涤、干燥
b.先用适量稀硫酸洗涤绿矾并将洗涤液与滤液合并,可提高钛的产率
(4)灼烧后的成分为
 ,可用作钛白颜料,该物质的一种晶胞结构(四方晶体)如图3所示。该晶体的密度为
,可用作钛白颜料,该物质的一种晶胞结构(四方晶体)如图3所示。该晶体的密度为 (用含
(用含 、
、 、
、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(5)工序②生成的气体
 为可燃性气体,生成气体
为可燃性气体,生成气体 的反应方程式为
的反应方程式为(6)还原工序中通入氩气的目的是
(7)利用图4装置可获得金属钛。在较低的阴极电位下,
 中的氧解离进入熔融盐,最后只剩下纯钛,另一极产生
中的氧解离进入熔融盐,最后只剩下纯钛,另一极产生 、
、 和可燃性气体
和可燃性气体 。产生可燃性气体
。产生可燃性气体 的电极反应式为
的电极反应式为
您最近一年使用:0次
解题方法
6 . 氧化铁黄(又称羟基铁),化学式为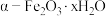 或
或 ,针状结构,呈黄色粉末状,是一种粒径小于
,针状结构,呈黄色粉末状,是一种粒径小于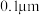 ,在透明介质中有很好分散性的铁系颜料,着色力强,不溶于碱,微溶于酸。工业以硫酸渣(含
,在透明介质中有很好分散性的铁系颜料,着色力强,不溶于碱,微溶于酸。工业以硫酸渣(含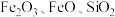 等)为原料制备铁黄
等)为原料制备铁黄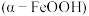 的一种工艺流程如图所示:
的一种工艺流程如图所示: 的
的 的
的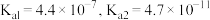 。
。
回答下列问题:
(1)铁黄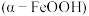 中铁元素的化合价为
中铁元素的化合价为___________ ,其在元素周期表___________ 族。
(2)“滤渣”的主要成分为___________ (填化学式)。
(3)“沉铁”过程中生成 的化学方程式为
的化学方程式为___________ 。
(4)常温下加入的 溶液呈
溶液呈___________ (填“酸性”“碱性”或“中性”)。
(5)铁黄产品也可以用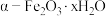 表示,为了测定所制备铁黄的x值,进行如下操作:用分析天平准确称量
表示,为了测定所制备铁黄的x值,进行如下操作:用分析天平准确称量 样品置于坩埚中加热、冷却后称量,经过重复操作,当达到恒重时,残留固体质量为
样品置于坩埚中加热、冷却后称量,经过重复操作,当达到恒重时,残留固体质量为 ,则
,则
___________ 。
(6)非整比铁氧化合物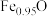 具有
具有 型晶体结构,由于
型晶体结构,由于 ,所以晶体存在缺陷,设晶胞中
,所以晶体存在缺陷,设晶胞中 为x个,
为x个, 为y个,则
为y个,则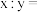
___________ (计算值写最简整数比)。
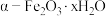 或
或 ,针状结构,呈黄色粉末状,是一种粒径小于
,针状结构,呈黄色粉末状,是一种粒径小于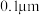 ,在透明介质中有很好分散性的铁系颜料,着色力强,不溶于碱,微溶于酸。工业以硫酸渣(含
,在透明介质中有很好分散性的铁系颜料,着色力强,不溶于碱,微溶于酸。工业以硫酸渣(含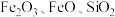 等)为原料制备铁黄
等)为原料制备铁黄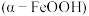 的一种工艺流程如图所示:
的一种工艺流程如图所示: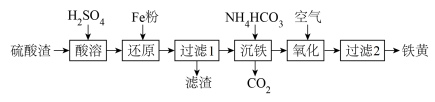
 的
的 的
的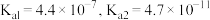 。
。回答下列问题:
(1)铁黄
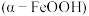 中铁元素的化合价为
中铁元素的化合价为(2)“滤渣”的主要成分为
(3)“沉铁”过程中生成
 的化学方程式为
的化学方程式为(4)常温下加入的
 溶液呈
溶液呈(5)铁黄产品也可以用
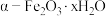 表示,为了测定所制备铁黄的x值,进行如下操作:用分析天平准确称量
表示,为了测定所制备铁黄的x值,进行如下操作:用分析天平准确称量 样品置于坩埚中加热、冷却后称量,经过重复操作,当达到恒重时,残留固体质量为
样品置于坩埚中加热、冷却后称量,经过重复操作,当达到恒重时,残留固体质量为 ,则
,则
(6)非整比铁氧化合物
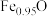 具有
具有 型晶体结构,由于
型晶体结构,由于 ,所以晶体存在缺陷,设晶胞中
,所以晶体存在缺陷,设晶胞中 为x个,
为x个, 为y个,则
为y个,则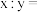
您最近一年使用:0次
2024·云南昆明·三模
解题方法
7 . 一氧化二氯( )是国际公认的高效安全的灭菌消毒剂,易溶于水。某学习小组设计如图所示实验装置,利用
)是国际公认的高效安全的灭菌消毒剂,易溶于水。某学习小组设计如图所示实验装置,利用 和潮湿的碳酸钠制备
和潮湿的碳酸钠制备 。装置乙中无其它气体生成,装置丙中生成HClO。以下装置中发生反应的方程式书写错误的是
。装置乙中无其它气体生成,装置丙中生成HClO。以下装置中发生反应的方程式书写错误的是
 )是国际公认的高效安全的灭菌消毒剂,易溶于水。某学习小组设计如图所示实验装置,利用
)是国际公认的高效安全的灭菌消毒剂,易溶于水。某学习小组设计如图所示实验装置,利用 和潮湿的碳酸钠制备
和潮湿的碳酸钠制备 。装置乙中无其它气体生成,装置丙中生成HClO。以下装置中发生反应的方程式书写错误的是
。装置乙中无其它气体生成,装置丙中生成HClO。以下装置中发生反应的方程式书写错误的是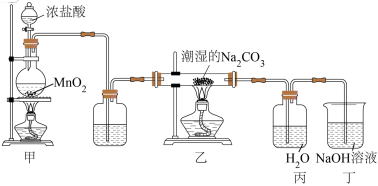
A.甲: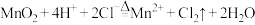 |
B.乙: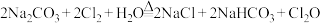 |
C.丙: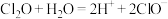 |
D.丁: |
您最近一年使用:0次
2024-05-17更新
|
172次组卷
|
3卷引用:2024届云南省昆明市高三5月市统考三诊一模考试理综试卷-高中化学
8 . 二氧化氯(ClO2)是一种高效消毒剂,易溶于水,沸点为11.0℃,浓度高时极易爆炸。某研究小组在实验室按如图所示的装置,用干燥的氯气与固体亚氯酸钠制备二氧化氯,请回答下列问题:___________ ,其作用是___________ 。
(2)仪器a的名称为___________ ,装置E的作用是___________ 。
(3)装置D中冰水的主要作用是___________ ,往D中通入氯气的同时还通入干燥的空气,其主要目的是___________ 。
(4)装置D内发生反应的化学方程式为___________ 。
(5)已知:利用NaClO2溶液制备NaClO2晶体的过程中,需使用38℃~60℃的温水洗涤,洗涤的方法为___________ 。
(6)工业上可在酸性条件下用双氧水与NaClO3反应制备ClO2,该反应的离子方程式为
___________ 。

(2)仪器a的名称为
(3)装置D中冰水的主要作用是
(4)装置D内发生反应的化学方程式为
(5)已知:利用NaClO2溶液制备NaClO2晶体的过程中,需使用38℃~60℃的温水洗涤,洗涤的方法为
(6)工业上可在酸性条件下用双氧水与NaClO3反应制备ClO2,该反应的离子方程式为
您最近一年使用:0次
解题方法
9 . 为探索某工厂的废金属屑(主要成分为Fe、Cu、Al、Al2O3、Fe2O3等)的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、胆矾晶体(CuSO4·5H2O,M=250g/mol)和水处理剂高铁酸钾(K2FeO4)
(1)试剂X是___________ ;试剂Y是___________ 。
(2)分离溶液A和固体B的操作中,所需要的玻璃仪器除了烧杯外还需要___________ 。
(3)写出溶液A转化为固体C的离子方程式___________ 。
(4)在步骤Ⅱ时,小组成员小明用下图装置进行试验,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,你的建议是___________ 。___________ 。___________ 。
(7)该小组同学取用100.0g该废金属屑,经过实验,最终得到胆矾晶体25.0g,该废料中铜的质量分数约为___________ 。

(1)试剂X是
(2)分离溶液A和固体B的操作中,所需要的玻璃仪器除了烧杯外还需要
(3)写出溶液A转化为固体C的离子方程式
(4)在步骤Ⅱ时,小组成员小明用下图装置进行试验,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,你的建议是
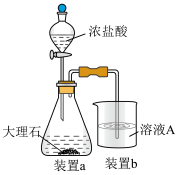
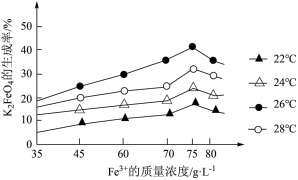
(7)该小组同学取用100.0g该废金属屑,经过实验,最终得到胆矾晶体25.0g,该废料中铜的质量分数约为
您最近一年使用:0次
名校
10 . 室温下,下列各组离子一定能与指定溶液大量共存的是
A.无色透明溶液: |
B. 的溶液: 的溶液: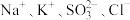 |
C.使酚酞变红色的溶液: |
D. 的 的 溶液: 溶液: |
您最近一年使用:0次



