解题方法
1 . 砷 在元素周期表中与氮同主族,砷及其化合物被运用在农药、医药和染料等领域中。某含砷工业废水经处理可转化为粗
在元素周期表中与氮同主族,砷及其化合物被运用在农药、医药和染料等领域中。某含砷工业废水经处理可转化为粗 ,流程如下:
,流程如下:
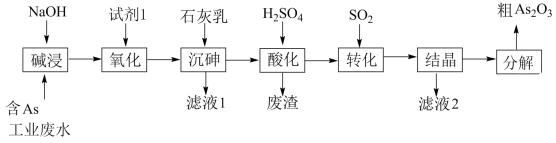
已知:
①含 工业废水主要以亚砷酸(
工业废水主要以亚砷酸( )形式存在,
)形式存在, 为三元弱酸,受热分解为
为三元弱酸,受热分解为 ;
;
② 微溶于水,
微溶于水, 难溶于水。
难溶于水。
回答下列问题:
(1)砷元素在元素周期表中的位置为_______ 。
(2)“碱浸”中发生反应的离子方程式为_______ 。
(3)从绿色化学角度考虑,“试剂1”可以选择_______ (填化学式)。
(4)“沉砷”在流程中的目的是_______ ;“沉砷”的最佳温度是 ,温度高于
,温度高于 时,随温度升高转化率下降,可能的原因是
时,随温度升高转化率下降,可能的原因是_______ 。
(5)“废渣”的主要成分是_______ ,“转化”中发生反应的化学方程式为_______ 。
(6)从综合利用的角度考虑“滤液2”可返回_______ 步骤中循环再利用。
 在元素周期表中与氮同主族,砷及其化合物被运用在农药、医药和染料等领域中。某含砷工业废水经处理可转化为粗
在元素周期表中与氮同主族,砷及其化合物被运用在农药、医药和染料等领域中。某含砷工业废水经处理可转化为粗 ,流程如下:
,流程如下:
已知:
①含
 工业废水主要以亚砷酸(
工业废水主要以亚砷酸( )形式存在,
)形式存在, 为三元弱酸,受热分解为
为三元弱酸,受热分解为 ;
;②
 微溶于水,
微溶于水, 难溶于水。
难溶于水。回答下列问题:
(1)砷元素在元素周期表中的位置为
(2)“碱浸”中发生反应的离子方程式为
(3)从绿色化学角度考虑,“试剂1”可以选择
(4)“沉砷”在流程中的目的是
 ,温度高于
,温度高于 时,随温度升高转化率下降,可能的原因是
时,随温度升高转化率下降,可能的原因是(5)“废渣”的主要成分是
(6)从综合利用的角度考虑“滤液2”可返回
您最近一年使用:0次
名校
2 . 1869年俄国化学家门捷列夫制出第一张元素周期表,元素周期表体现了元素位置、结构和性质的关系。短周期元素A、B、C、D、E原子序数递增,由它们组成的新型化合物CA4B5D8·4A2D可用于电讯器材、高级玻璃的制造,其受热分解产物中有两种常见的10电子分子,二者反应生成一种弱碱,B、E同主族,E是同周期离子半径最小的。
(1)画出E的离子结构示意图______ ,在元素周期表中的位置为______ 。
(2)100—200℃时只生成一种气体,该气体电子式为______ 。
(3)试比较B、C、E元素所形成最高价氧化物对应水化物的酸性由强到弱的顺序为(写化学式)______ ,并从原子结构角度解释其原因__ 。
(4)请依据推断比较D、E两种元素离子半径的大小______ 。
(5)C的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)该化合物500℃热分解后生成的固体氧化物可与Mg单质发生置换反应,写出化学方程式______ 。
(1)画出E的离子结构示意图
(2)100—200℃时只生成一种气体,该气体电子式为
(3)试比较B、C、E元素所形成最高价氧化物对应水化物的酸性由强到弱的顺序为(写化学式)
(4)请依据推断比较D、E两种元素离子半径的大小
(5)C的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的离子方程式为
(6)该化合物500℃热分解后生成的固体氧化物可与Mg单质发生置换反应,写出化学方程式
您最近一年使用:0次
名校
解题方法
3 . (I)俄美科学家联合小组宣布合成出114号元素(Fl)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中的位置为:_______ ,属于_______ 元素(填“金属”或“非金属”)。
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
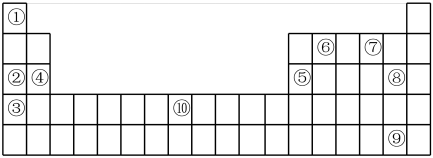
(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是_______ (填化学式)。
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为_______ ;
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为_______ ;
(5)元素⑩的名称为_______ ,其单质与⑧的单质反应的化学方程式为_______ ;
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是_______
A.L2+、R2-的核外电子数相等
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物具有两性
D.简单氢化物的沸点为HnT>HnR
E.T与R可形成的化合物TR2、TR3
F.Q与M的单质均能与盐酸、NaOH溶液反应放出氢气
(1)该元素在周期表中的位置为:
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:

(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为
(5)元素⑩的名称为
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物具有两性
D.简单氢化物的沸点为HnT>HnR
E.T与R可形成的化合物TR2、TR3
F.Q与M的单质均能与盐酸、NaOH溶液反应放出氢气
您最近一年使用:0次
名校
解题方法
4 . 短周期元素X、Y、Z、W的原子序数递增,且Z为金属元素,X、W同主族。单质X、Z、W可分别与单质Y化合生成最高价化合物甲、乙、丙。结合如图转化关系,下列判断正确的是
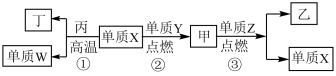

A.反应①可表示为 | B.X位于元素周期表第二周期V主族 |
| C.甲、丙、丁均为酸性氧化物 | D.乙的电子式为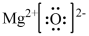 |
您最近一年使用:0次
2022-04-23更新
|
1012次组卷
|
3卷引用: 山东省青岛第五十八中学2022-2023学年高一下学期3月月考化学试题
名校
解题方法
5 . X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W分别与Y形成的最高价化合物为甲、乙、丙。结合如图转化关系,下列判断错误的是( )
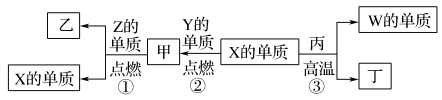

| A.反应③可用于工业上制取W的单质 | B.X位于元素周期表第二周期ⅣA族 |
| C.甲、丙、丁均为酸性化合物 | D.工业上可以用乙来作耐火材料 |
您最近一年使用:0次
2020-01-17更新
|
1246次组卷
|
6卷引用:江西省宁冈中学2022-2023学年高一下学期6月期末化学试题



