1 . 2−氯乙醇(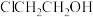 )是重要的有机溶剂和有机合成原料,主要用作合成橡胶的原料以及染料、农药、医药的中间体。氯乙醇的工业生产常用1991年Gomberg提出的方法——将乙烯和氯气同时通入水中制得。某校同学设计下列装置进行2−氯乙醇制备实验(部分加热装置及夹持仪器已省略):
)是重要的有机溶剂和有机合成原料,主要用作合成橡胶的原料以及染料、农药、医药的中间体。氯乙醇的工业生产常用1991年Gomberg提出的方法——将乙烯和氯气同时通入水中制得。某校同学设计下列装置进行2−氯乙醇制备实验(部分加热装置及夹持仪器已省略):
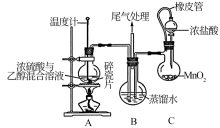
已知装置A中发生的主反应: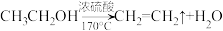 ;
;
主要副反应: 。
。
回答下列问题:
(1)配制浓硫酸和乙醇混合溶液的方法是___________ 。
a.搅拌下将浓硫酸慢慢加入到乙醇中 b.搅拌下将乙醇慢慢加入到浓硫酸中
(2)装置A圆底烧瓶中加碎瓷片的目的是___________ 。
(3)装置C中橡皮管的作用是___________ 。
(4)装置B中生成2−氯乙醇的过程的化学反应方程式有___________ 。
(5)反应结束后,装置B的溶液中2−氯乙醇质量分数的测定步骤如下(假定含氯物质只有2−氯乙醇和HCl,密度为 ,2−氯乙醇的摩尔质量为
,2−氯乙醇的摩尔质量为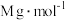 。):
。):
步骤1:吸取2.00mL装置B中的溶液于锥形瓶中,加入NaOH溶液,加热,使2−氯乙醇中的氯元素转化为 ,用硝酸酸化后加入a mL 0.1000
,用硝酸酸化后加入a mL 0.1000
 标准溶液,然后加入几滴铁铵矾[
标准溶液,然后加入几滴铁铵矾[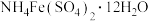 ]的溶液,用0.1000
]的溶液,用0.1000 的
的 标准溶液回滴过量的
标准溶液回滴过量的 (
(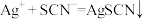 ),消耗
),消耗 溶液b mL。
溶液b mL。
步骤2:另取2.00mL装置B中的溶液于锥形瓶中,加入a mL 0.1000
 标准溶液,加入几滴铁铵矾的溶液,用0.1000
标准溶液,加入几滴铁铵矾的溶液,用0.1000 的
的 标准溶液回滴过量的
标准溶液回滴过量的 ,消耗
,消耗 溶液c mL。
溶液c mL。
①铁铵矾溶液的作用是___________ 。
②装置B的溶液中2−氯乙醇的质量分数为___________ 。
③在滴定终点到达之前的滴定过程中,两种沉淀表面会吸附部分 ,需不断剧烈摇动锥形瓶。若步骤2中为未按此要求操作,则测定结果会
,需不断剧烈摇动锥形瓶。若步骤2中为未按此要求操作,则测定结果会___________ (选填“偏高”“偏低”或“无影响”)。
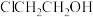 )是重要的有机溶剂和有机合成原料,主要用作合成橡胶的原料以及染料、农药、医药的中间体。氯乙醇的工业生产常用1991年Gomberg提出的方法——将乙烯和氯气同时通入水中制得。某校同学设计下列装置进行2−氯乙醇制备实验(部分加热装置及夹持仪器已省略):
)是重要的有机溶剂和有机合成原料,主要用作合成橡胶的原料以及染料、农药、医药的中间体。氯乙醇的工业生产常用1991年Gomberg提出的方法——将乙烯和氯气同时通入水中制得。某校同学设计下列装置进行2−氯乙醇制备实验(部分加热装置及夹持仪器已省略): 
已知装置A中发生的主反应:
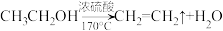 ;
;主要副反应:
 。
。回答下列问题:
(1)配制浓硫酸和乙醇混合溶液的方法是
a.搅拌下将浓硫酸慢慢加入到乙醇中 b.搅拌下将乙醇慢慢加入到浓硫酸中
(2)装置A圆底烧瓶中加碎瓷片的目的是
(3)装置C中橡皮管的作用是
(4)装置B中生成2−氯乙醇的过程的化学反应方程式有
(5)反应结束后,装置B的溶液中2−氯乙醇质量分数的测定步骤如下(假定含氯物质只有2−氯乙醇和HCl,密度为
 ,2−氯乙醇的摩尔质量为
,2−氯乙醇的摩尔质量为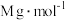 。):
。):步骤1:吸取2.00mL装置B中的溶液于锥形瓶中,加入NaOH溶液,加热,使2−氯乙醇中的氯元素转化为
 ,用硝酸酸化后加入a mL 0.1000
,用硝酸酸化后加入a mL 0.1000
 标准溶液,然后加入几滴铁铵矾[
标准溶液,然后加入几滴铁铵矾[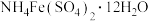 ]的溶液,用0.1000
]的溶液,用0.1000 的
的 标准溶液回滴过量的
标准溶液回滴过量的 (
(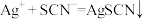 ),消耗
),消耗 溶液b mL。
溶液b mL。步骤2:另取2.00mL装置B中的溶液于锥形瓶中,加入a mL 0.1000

 标准溶液,加入几滴铁铵矾的溶液,用0.1000
标准溶液,加入几滴铁铵矾的溶液,用0.1000 的
的 标准溶液回滴过量的
标准溶液回滴过量的 ,消耗
,消耗 溶液c mL。
溶液c mL。①铁铵矾溶液的作用是
②装置B的溶液中2−氯乙醇的质量分数为
③在滴定终点到达之前的滴定过程中,两种沉淀表面会吸附部分
 ,需不断剧烈摇动锥形瓶。若步骤2中为未按此要求操作,则测定结果会
,需不断剧烈摇动锥形瓶。若步骤2中为未按此要求操作,则测定结果会
您最近一年使用:0次
名校
解题方法
2 . LiCoO2(钴酸锂)是锂离子电池的正极材料。以某海水为原料制备钴酸锂的一种流程如下:

已知如下信息:
①该海水中含浓度较大的LiCl,含少量MgCl2、CaCl2、MnCl2等。
②碳酸锂的溶解度与温度关系如图所示:
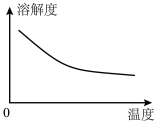
③常温下,几种难溶物质的溶度积数据如下:
请回答下列问题:
(1)LiCoO2中钴的化合价为________ 。滤渣1主要成分有MgCO3、Mg(OH)2、CaCO3和__________ (填化学式)。
(2)调节pH=5的目的是__________ 。
(3)“沉锂”包括过滤、洗涤等,宜用_________ (填“热水”或“冷水”)洗涤Li2CO3。加入纯碱的量与锂回收率的关系如表所示:
从生产成本考虑,宜选择_______ (填序号)方案投料。
(4)“除杂2”中调pH=13时c(Mg2+)=_________ mol·L-1。
(5)“合成”中采用高温条件,放出一种能使澄清石灰水变浑浊的气体。写出“合成”发生反应的化学方程式________ 。
(6)在“合成”中制备1 mol LiCoO2转移电子的物质的量为__________ 。

已知如下信息:
①该海水中含浓度较大的LiCl,含少量MgCl2、CaCl2、MnCl2等。
②碳酸锂的溶解度与温度关系如图所示:

③常温下,几种难溶物质的溶度积数据如下:
| 物质 | Li2CO3 | MgCO3 | CaCO3 | MnCO3 | Mg(OH)2 |
| Ksp | 2.5×102 | 6.8×106 | 2.8×109 | 2.3×1011 | 6.0×1010 |
(1)LiCoO2中钴的化合价为
(2)调节pH=5的目的是
(3)“沉锂”包括过滤、洗涤等,宜用
| 序号 |  | 沉淀质量/g | 碳酸锂含量/% | 锂回收率/% |
| ① | 0.9∶1 | 10.09 | 92.36 | 77.67 |
| ② | 1.0∶1 | 10.97 | 90.19 | 82.46 |
| ③ | 1.1∶1 | 11.45 | 89.37 | 85.27 |
| ④ | 1.2∶1 | 12.14 | 84.82 | 85.45 |
(4)“除杂2”中调pH=13时c(Mg2+)=
(5)“合成”中采用高温条件,放出一种能使澄清石灰水变浑浊的气体。写出“合成”发生反应的化学方程式
(6)在“合成”中制备1 mol LiCoO2转移电子的物质的量为
您最近一年使用:0次
2020-04-23更新
|
240次组卷
|
3卷引用:四川省雅安中学2019-2020学年高二下学期5月月考理综化学试题
解题方法
3 . 甲醇(CH3OH)是一种用途广泛的基础有机原料和优质燃料。
(1)甲醇通过一系列反应可生成某有机物,结构简式如图。此有机物分子中有个_______ 手性碳原子。

(2)甲醇的同系物乙醇,在一定条件下可发生消去反应生成乙烯,乙烯分子中H-C-H键角_______ 120º(填 “大于”或“小于” )。
(3)在一定条件下,甲醇(沸点64.7℃)可转化为乙酸甲酯(CH3COOCH3,沸点57.1℃)。
①乙酸甲酯中σ键和π键的个数之比为_______ 。
②甲醇与乙酸甲酯的混合物因沸点接近而不易分离,工业上用蒸馏的方法分离二者时常先加适量水,理由为_______ 。
(4)科研团队通过皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管合成T-碳,T-碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,晶胞结构及俯视图如图所示。

①T-碳与金刚石互称为_______ 。一个T-碳晶胞中含有_______ 个碳原子。
②T-碳的密度约为金刚石的一半。则T-碳晶胞的边长和金刚石晶胞的边长之比_______ 。
(1)甲醇通过一系列反应可生成某有机物,结构简式如图。此有机物分子中有个

(2)甲醇的同系物乙醇,在一定条件下可发生消去反应生成乙烯,乙烯分子中H-C-H键角
(3)在一定条件下,甲醇(沸点64.7℃)可转化为乙酸甲酯(CH3COOCH3,沸点57.1℃)。
①乙酸甲酯中σ键和π键的个数之比为
②甲醇与乙酸甲酯的混合物因沸点接近而不易分离,工业上用蒸馏的方法分离二者时常先加适量水,理由为
(4)科研团队通过皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管合成T-碳,T-碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,晶胞结构及俯视图如图所示。

①T-碳与金刚石互称为
②T-碳的密度约为金刚石的一半。则T-碳晶胞的边长和金刚石晶胞的边长之比
您最近一年使用:0次



