解题方法
1 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)钠在空气中燃烧生成_______ (填“Na2O”或“Na2O2”);
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种_______ (填“酸性”“碱性”或“两性”)氧化物;
(3)我国古代建筑红墙碧瓦,庄严巍峨。可用作建筑外墙红色涂料的是________ (填“ ”或“
”或“ ”)。
”)。
(1)钠在空气中燃烧生成
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种
(3)我国古代建筑红墙碧瓦,庄严巍峨。可用作建筑外墙红色涂料的是
 ”或“
”或“ ”)。
”)。
您最近一年使用:0次
解题方法
2 . 如图为元素周期表的一部分。回答下列问题:
(1)O的原子序数是___________ 。
(2)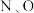 和F三种元素中,非金属性最强的是
和F三种元素中,非金属性最强的是___________ (填元素符号)。
(3)F和 的原子半径大小:F
的原子半径大小:F___________  (填“
(填“ ”或“
”或“ ”)。
”)。
(4) 在氢气中燃烧的化学方程式为
在氢气中燃烧的化学方程式为___________ 。
| N | O | F |
| Cl |
(2)
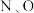 和F三种元素中,非金属性最强的是
和F三种元素中,非金属性最强的是(3)F和
 的原子半径大小:F
的原子半径大小:F (填“
(填“ ”或“
”或“ ”)。
”)。(4)
 在氢气中燃烧的化学方程式为
在氢气中燃烧的化学方程式为
您最近一年使用:0次
解题方法
3 . 化学与生活息息相关。请根据题意填空:
(1)___________ (填“ ”或“
”或“ ”)可以与水反应生成氧气用于解决鱼塘缺氧问题。
”)可以与水反应生成氧气用于解决鱼塘缺氧问题。
(2)用于做面食的苏打 与小苏打
与小苏打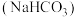 外观相似。某同学取少量两种物质分别置于干燥的坩埚中,盖上盖子加热,盖子内壁有大量水珠附着的是
外观相似。某同学取少量两种物质分别置于干燥的坩埚中,盖上盖子加热,盖子内壁有大量水珠附着的是___________ (填“苏打”或“小苏打”)。
(3)向盛有 溶液中加适量铁粉,溶液颜色
溶液中加适量铁粉,溶液颜色___________ (填“由黄色变为绿色”或“由绿色变为黄色”)。
(1)
 ”或“
”或“ ”)可以与水反应生成氧气用于解决鱼塘缺氧问题。
”)可以与水反应生成氧气用于解决鱼塘缺氧问题。(2)用于做面食的苏打
 与小苏打
与小苏打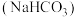 外观相似。某同学取少量两种物质分别置于干燥的坩埚中,盖上盖子加热,盖子内壁有大量水珠附着的是
外观相似。某同学取少量两种物质分别置于干燥的坩埚中,盖上盖子加热,盖子内壁有大量水珠附着的是(3)向盛有
 溶液中加适量铁粉,溶液颜色
溶液中加适量铁粉,溶液颜色
您最近一年使用:0次
名校
4 . 如图为元素周期表的一部分。请回答下列问题:
(1)N的原子序数是___________ 。
(2)C、N和O三种元素中,非金属性最强的是___________ 。
(3)O和S的原子半径大小:O___________ S(填“>”或“<”)。
(4)S在空气中燃烧的化学方程式为___________ 。
| C | N | O |
| S |
(2)C、N和O三种元素中,非金属性最强的是
(3)O和S的原子半径大小:O
(4)S在空气中燃烧的化学方程式为
您最近一年使用:0次
2023-06-28更新
|
188次组卷
|
3卷引用:2023年湖南省普通高中学业水平考试化学试题
5 . 单质碘有非常重要的用途,从海带燃烧后所得的海带灰中提取碘是单质碘的制备方法之一:海带燃烧后所得的海带灰中含有 ,从中获得
,从中获得 ,再由
,再由 制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:

请回答下列问题:
(1)步骤③的实验操作名称是______ (填“过滤”或“蒸发”);
(2)含碘离子溶液中加氧化剂转化为含单质碘的水溶液,能达到该目的的物质是______ (填“氯水”或“稀盐酸”);
(3)I-被氧化为I2的离子方程式为____________ ;
(4)工业上合成氨的反应为: ,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为
,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为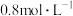
①用N2表示该反应的速率为______ ;
②其他条件不变时,升高温度,该反应的反应速率将______ (填“增大”或“减小”)。
 ,从中获得
,从中获得 ,再由
,再由 制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
请回答下列问题:
(1)步骤③的实验操作名称是
(2)含碘离子溶液中加氧化剂转化为含单质碘的水溶液,能达到该目的的物质是
(3)I-被氧化为I2的离子方程式为
(4)工业上合成氨的反应为:
 ,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为
,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为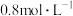
①用N2表示该反应的速率为
②其他条件不变时,升高温度,该反应的反应速率将
您最近一年使用:0次
6 . 根据元素周期表中1~20号元素的性质和递变规律,回答下列问题:
(1)原子序数为8的元素名称是______ ;
(2)硫化氢的电子式是______ ;
(3)氟(F)和氯(Cl)均为第ⅦA族元素,则两种元素的非金属性强弱是F______ (填“>”或“<”)Cl;
(4)钾和硫两种元素的最高价氧化物对应的水化物相互反应的离子方程式为____________ 。
(1)原子序数为8的元素名称是
(2)硫化氢的电子式是
(3)氟(F)和氯(Cl)均为第ⅦA族元素,则两种元素的非金属性强弱是F
(4)钾和硫两种元素的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
7 . 化学是一门实用性很强的科学。请根据题意填空:
(1)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有______ (填“钠”或“钾”)元素;
(2)在金属元素中,有一类金属既可单独使用,也可用于生产合金。在合金中加入该类金属,能大大改善合金的性能,因而,该类金属又被称为“冶金工业的维生素”。则该类金属是______ (填“稀土金属”或“碱土金属”);
(3)中国古代最早的指南针“司南”,其具有磁性作用是因为主要含有______ (填“Fe2O3”或“Fe3O4”)。
(1)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有
(2)在金属元素中,有一类金属既可单独使用,也可用于生产合金。在合金中加入该类金属,能大大改善合金的性能,因而,该类金属又被称为“冶金工业的维生素”。则该类金属是
(3)中国古代最早的指南针“司南”,其具有磁性作用是因为主要含有
您最近一年使用:0次
名校
8 . 根据元素周期表中1~18号元素的性质和递变规律,回答下列问题。
(1)原子序数为17的元素符号是___________ ;
(2)二氧化碳中所含两种元素的原子半径大小:C___________ O(填“>”或“<”);
(3)硫和氯均为第三周期元素,则两种元素的气态氢化物的稳定性强弱:
___________ HCl(填“>”或“<”);
(4)氮元素的简单气态氢化物与其最高价氧化物对应的水化物相互反应的离子方程式为___________ 。
(1)原子序数为17的元素符号是
(2)二氧化碳中所含两种元素的原子半径大小:C
(3)硫和氯均为第三周期元素,则两种元素的气态氢化物的稳定性强弱:

(4)氮元素的简单气态氢化物与其最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
解题方法
9 . 化学与人类生活密切相关。请按要求回答下列问题:
(1)过氧化钠是一种淡黄色固体,在呼吸面具或潜水艇中作为氧气的来源, 所发生的主要反应的化学方程式为
所发生的主要反应的化学方程式为
_______ ;
(2)铝制易拉罐的表面有一层氧化膜,主要成分是 。它与盐酸和氢氧化钠溶液反应都生成盐和水,则
。它与盐酸和氢氧化钠溶液反应都生成盐和水,则 属于
属于_______ (填“酸性”“碱性”或“两性”)氧化物;
(3)我国古代建筑红墙碧瓦,庄严巍峨。可用作建筑外墙红色涂料的是_______ (填“ ”或“
”或“ ”)。
”)。
(1)过氧化钠是一种淡黄色固体,在呼吸面具或潜水艇中作为氧气的来源,
 所发生的主要反应的化学方程式为
所发生的主要反应的化学方程式为
(2)铝制易拉罐的表面有一层氧化膜,主要成分是
 。它与盐酸和氢氧化钠溶液反应都生成盐和水,则
。它与盐酸和氢氧化钠溶液反应都生成盐和水,则 属于
属于(3)我国古代建筑红墙碧瓦,庄严巍峨。可用作建筑外墙红色涂料的是
 ”或“
”或“ ”)。
”)。
您最近一年使用:0次
解题方法
10 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
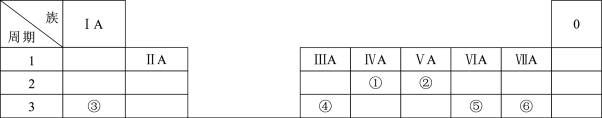
(1)②的原子结构示意图是_______ 。
(2)写出①的最高价氧化物的电子式:_______ 。
(3)⑤和⑥分别形成的最简单氢化物更稳定的是_______ (填化学式)。
(4)③对应的最高价氧化物形成的水化物与④形成的氧化物反应的离子方程式为_______ 。

(1)②的原子结构示意图是
(2)写出①的最高价氧化物的电子式:
(3)⑤和⑥分别形成的最简单氢化物更稳定的是
(4)③对应的最高价氧化物形成的水化物与④形成的氧化物反应的离子方程式为
您最近一年使用:0次



