1 . 海带中含有丰富的碘元素,某化学兴趣小组设计如下所示的流程图提取碘:
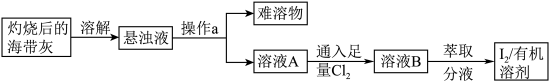
请回答下列问题:
(1)加水溶解海带灰,应采用的装置是_______ (填字母序号)
A.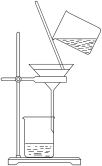 B.
B. C.
C.
(2)操作a的名称是_______ (填“过滤”或“蒸发”);
(3)溶液A中通入足量 发生的反应为:
发生的反应为: ,反应物
,反应物 表现
表现_______ (填“氧化性”或“还原性”);
(4)工业上合成氨的反应为: 。一定条件下,将2 mol
。一定条件下,将2 mol  和6 mol
和6 mol  置于1 L的密闭容器中,10 min后测得
置于1 L的密闭容器中,10 min后测得 为0.4 mol。
为0.4 mol。
①用 的浓度变化表示该反应0~10 min的平均速率为
的浓度变化表示该反应0~10 min的平均速率为_______ mol/(L·min);
②其他条件不变时,压缩容器体积,增大压强,该反应的速率将_______ (填“增大”或“减小”)。

请回答下列问题:
(1)加水溶解海带灰,应采用的装置是
A.
 B.
B. C.
C.
(2)操作a的名称是
(3)溶液A中通入足量
 发生的反应为:
发生的反应为: ,反应物
,反应物 表现
表现(4)工业上合成氨的反应为:
 。一定条件下,将2 mol
。一定条件下,将2 mol  和6 mol
和6 mol  置于1 L的密闭容器中,10 min后测得
置于1 L的密闭容器中,10 min后测得 为0.4 mol。
为0.4 mol。①用
 的浓度变化表示该反应0~10 min的平均速率为
的浓度变化表示该反应0~10 min的平均速率为②其他条件不变时,压缩容器体积,增大压强,该反应的速率将
您最近一年使用:0次
2 . 钠、铝和钙是中学化学常见的三种重要金属。请回答下列问题:
(1)常盛放在呼吸面具中作为供氧剂的物质为____________ (填“ ”或“
”或“ ”)。
”)。
(2) 能溶于酸或强碱溶液生成盐和水,则
能溶于酸或强碱溶液生成盐和水,则 是一种
是一种____________ (填“酸性”“碱性”或“两性”)氧化物。
(3)漂白粉的有效成分为____________ (填“ ”或“
”或“ ”)。
”)。
(1)常盛放在呼吸面具中作为供氧剂的物质为
 ”或“
”或“ ”)。
”)。(2)
 能溶于酸或强碱溶液生成盐和水,则
能溶于酸或强碱溶液生成盐和水,则 是一种
是一种(3)漂白粉的有效成分为
 ”或“
”或“ ”)。
”)。
您最近一年使用:0次
名校
解题方法
3 . 请根据物质在生产、生活等方面的应用填空:
(1)厨房里常使用小苏打,向其水溶液中滴加酚酞溶液后,溶液呈_______ (填“无”或“浅红”)色;
(2)检验某补铁剂中的Fe2+是否被氧化成Fe3+,可用_______ (填“KSCN”或“H2SO4”)溶液;
(3)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装_______ (填“浓硫酸”或“浓盐酸”)。
(1)厨房里常使用小苏打,向其水溶液中滴加酚酞溶液后,溶液呈
(2)检验某补铁剂中的Fe2+是否被氧化成Fe3+,可用
(3)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装
您最近一年使用:0次
2017-12-04更新
|
388次组卷
|
6卷引用:湖南省株洲市茶陵县第三中学2019-2020学年高二上学期12月月考化学试题(学考)
4 . 化学来源于生活,应用于生活。根据题意回答下列问题:
(1)钠的氧化物中,与水反应产生氧气的是___________ (填“ ”或“
”或“ ”);
”);
(2)在反应 中,
中,___________ 是氧化剂(填“ ”或“CO”);
”或“CO”);
(3) 既能与盐酸反应,也能与NaOH溶液反应,则
既能与盐酸反应,也能与NaOH溶液反应,则 属于
属于___________ (填“酸性”“碱性”或“两性”)氢氧化物。
(1)钠的氧化物中,与水反应产生氧气的是
 ”或“
”或“ ”);
”);(2)在反应
 中,
中, ”或“CO”);
”或“CO”);(3)
 既能与盐酸反应,也能与NaOH溶液反应,则
既能与盐酸反应,也能与NaOH溶液反应,则 属于
属于
您最近一年使用:0次
5 . 钠、铝和硫是中学化学常见的三种重要元素。请回答下列问题:
(1)钠在空气中燃烧生成_______ (填“ ”或“
”或“ ”);
”);
(2) 能溶于强酸或强碱溶液生成盐和水,则
能溶于强酸或强碱溶液生成盐和水,则 是一种
是一种_______ (填“酸性”、“碱性”或“两性”)氧化物;
(3)加热时,浓硫酸可与木炭反应,请配平反应的化学方程式:_______ 。

_______  (浓)
(浓)
(1)钠在空气中燃烧生成
 ”或“
”或“ ”);
”);(2)
 能溶于强酸或强碱溶液生成盐和水,则
能溶于强酸或强碱溶液生成盐和水,则 是一种
是一种(3)加热时,浓硫酸可与木炭反应,请配平反应的化学方程式:

 (浓)
(浓)
您最近一年使用:0次
解题方法
6 . 化学是一门以实验为基础的科学。请根据题意填空:
(1)受热易分解产生气体的是___________ (填“ ”或“
”或“ ”);
”);
(2)一种红棕色粉末,常用于红色油漆和涂料的是___________ (填“FeO”或“ ”);
”);
(3) 能溶于酸或强碱溶液生成盐和水,则
能溶于酸或强碱溶液生成盐和水,则 是一种
是一种___________ (填“酸性”“碱性”或“两性”)氧化物。
(1)受热易分解产生气体的是
 ”或“
”或“ ”);
”);(2)一种红棕色粉末,常用于红色油漆和涂料的是
 ”);
”);(3)
 能溶于酸或强碱溶液生成盐和水,则
能溶于酸或强碱溶液生成盐和水,则 是一种
是一种
您最近一年使用:0次
解题方法
7 . 化学与人类生活密切相关。请按要求回答下列问题:
(1)过氧化钠是一种淡黄色固体,在呼吸面具或潜水艇中作为氧气的来源, 所发生的主要反应的化学方程式为
所发生的主要反应的化学方程式为
_______ ;
(2)铝制易拉罐的表面有一层氧化膜,主要成分是 。它与盐酸和氢氧化钠溶液反应都生成盐和水,则
。它与盐酸和氢氧化钠溶液反应都生成盐和水,则 属于
属于_______ (填“酸性”“碱性”或“两性”)氧化物;
(3)我国古代建筑红墙碧瓦,庄严巍峨。可用作建筑外墙红色涂料的是_______ (填“ ”或“
”或“ ”)。
”)。
(1)过氧化钠是一种淡黄色固体,在呼吸面具或潜水艇中作为氧气的来源,
 所发生的主要反应的化学方程式为
所发生的主要反应的化学方程式为
(2)铝制易拉罐的表面有一层氧化膜,主要成分是
 。它与盐酸和氢氧化钠溶液反应都生成盐和水,则
。它与盐酸和氢氧化钠溶液反应都生成盐和水,则 属于
属于(3)我国古代建筑红墙碧瓦,庄严巍峨。可用作建筑外墙红色涂料的是
 ”或“
”或“ ”)。
”)。
您最近一年使用:0次
名校
解题方法
8 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)钠在空气中燃烧生成_______ (填“Na2O”或“Na2O2”);
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种_______ (填“酸性”“碱性”或“两性”)氧化物;
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______ 。
(1)钠在空气中燃烧生成
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
您最近一年使用:0次
9 . 单质碘有非常重要的用途,从海带燃烧后所得的海带灰中提取碘是单质碘的制备方法之一:海带燃烧后所得的海带灰中含有 ,从中获得
,从中获得 ,再由
,再由 制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:

请回答下列问题:
(1)步骤③的实验操作名称是______ (填“过滤”或“蒸发”);
(2)含碘离子溶液中加氧化剂转化为含单质碘的水溶液,能达到该目的的物质是______ (填“氯水”或“稀盐酸”);
(3)I-被氧化为I2的离子方程式为____________ ;
(4)工业上合成氨的反应为: ,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为
,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为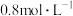
①用N2表示该反应的速率为______ ;
②其他条件不变时,升高温度,该反应的反应速率将______ (填“增大”或“减小”)。
 ,从中获得
,从中获得 ,再由
,再由 制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
请回答下列问题:
(1)步骤③的实验操作名称是
(2)含碘离子溶液中加氧化剂转化为含单质碘的水溶液,能达到该目的的物质是
(3)I-被氧化为I2的离子方程式为
(4)工业上合成氨的反应为:
 ,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为
,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为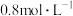
①用N2表示该反应的速率为
②其他条件不变时,升高温度,该反应的反应速率将
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)工业上常用铝土矿冶炼金属铝。
①铝土矿的主要成分为 和
和 ,其中
,其中 属于
属于____________ (填“酸性”“碱性”或“两性”)氧化物;
②冶炼过程中需要用到氨,氨溶于水所得溶液呈____________ (填“酸性”或“碱性”);
③利用金属活动性的不同,可以采用不同的冶炼方法,制取单质铝应采取_____________ (填“热还原法”或“电解法”)。
(2)工业上合成氨的反应为: ,一定条件下,将
,一定条件下,将 和
和 置于
置于 的密闭容器中,
的密闭容器中,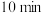 后测得
后测得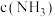 为
为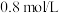 。
。
①用 表示该反应的速率为
表示该反应的速率为___________ ;
②其他条件不变时,再通入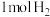 ,该反应的速率将
,该反应的速率将_____________ (填“增大”或“减小”)。
(1)工业上常用铝土矿冶炼金属铝。
①铝土矿的主要成分为
 和
和 ,其中
,其中 属于
属于②冶炼过程中需要用到氨,氨溶于水所得溶液呈
③利用金属活动性的不同,可以采用不同的冶炼方法,制取单质铝应采取
(2)工业上合成氨的反应为:
 ,一定条件下,将
,一定条件下,将 和
和 置于
置于 的密闭容器中,
的密闭容器中,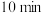 后测得
后测得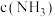 为
为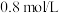 。
。①用
 表示该反应的速率为
表示该反应的速率为②其他条件不变时,再通入
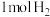 ,该反应的速率将
,该反应的速率将
您最近一年使用:0次
2020-05-12更新
|
404次组卷
|
2卷引用:湖南省2020年普通高中学业水平考试第一次模拟试卷化学试题



