名校
解题方法
1 . 84消毒液是一种常见的含氯消毒剂。如图为某品牌84消毒液的说明书中的部分内容。

(1)84消毒液的主要成分为_______ (用化学式表示)。
(2)常温,将氯气通入NaOH溶液中可制得84消毒液的主要成分。写出离子方程式:_______ 。
(3)某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。
Ⅰ.向2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.向2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
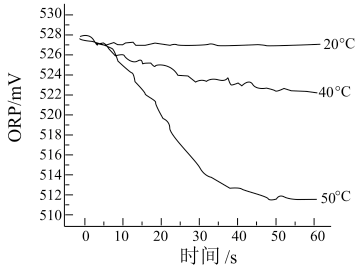
Ⅲ.测得84消毒液在不同温度时ORP随时间的变化曲线如下。
①已知白醋显酸性,不具有漂白性。实验Ⅰ、Ⅱ现象不同的原因是_______ 。
②实验表明,向84消毒液中加入较多稀硫酸时会产生氯气,生成氯气的离子方程式是_______ 。
③由实验Ⅲ可得出的结论是_______ 。ORP值不同的原因可能是_______ 。
(4)针对不同物品的消毒,84消毒液需要稀释到不同的浓度来使用。取含次氯酸钠14.9g/L的84消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为_______ mol∙L−1。

| 产品特点 本品是以次氯酸钠为主要成分的液体消毒剂。可杀灭肠道致病菌、化脓性球菌、致病性酵母菌,并能灭活病毒。 注意事项 1.本品易使有色衣脱色,禁止用于丝、毛、麻织物的消毒。 2.不得将本品与酸性产品(如洁厕类清洁产品)同时使用。 3.置于避光、阴凉处保存。 4.需稀释后使用,勿口服。 |
(2)常温,将氯气通入NaOH溶液中可制得84消毒液的主要成分。写出离子方程式:
(3)某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映水溶液中所有物质表现出来的氧化—还原性,ORP值越大,氧化性越强。
Ⅰ.向2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.向2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.测得84消毒液在不同温度时ORP随时间的变化曲线如下。

①已知白醋显酸性,不具有漂白性。实验Ⅰ、Ⅱ现象不同的原因是
②实验表明,向84消毒液中加入较多稀硫酸时会产生氯气,生成氯气的离子方程式是
③由实验Ⅲ可得出的结论是
(4)针对不同物品的消毒,84消毒液需要稀释到不同的浓度来使用。取含次氯酸钠14.9g/L的84消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为
您最近一年使用:0次
2021-01-24更新
|
568次组卷
|
4卷引用:湖南省株洲市炎陵县湘山高级中学等2校2022-2023学年高一下学期开学考试化学试题
解题方法
2 . 氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)苹果汁是人们喜欢的饮料。由于此饮料中含有Fe2+,现榨的苹果汁会由淡绿色(含Fe2+)变为棕黄色(含Fe3+)。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有_______。
(2)近年来,我国储氢碳纳米管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法除去,其反应的方程式为:C+K2Cr2O7+H2SO4→CO2↑+K2SO4+Cr2(SO4)3+H2O(未配平)。该反应中氧化产物的化学式是_______ , 被还原的元素是_______ ,氧化剂与还原剂的物质的量之比为_______ ,若反应中消耗5.88g重铬酸钾,则生成标准状况下的CO2体积为_______ 。
(3)硝化细菌可利用氧气和自身的酶,将酸性土壤中的 氧化为
氧化为 ,则该反应的离子方程式为
,则该反应的离子方程式为_______ 。
(1)苹果汁是人们喜欢的饮料。由于此饮料中含有Fe2+,现榨的苹果汁会由淡绿色(含Fe2+)变为棕黄色(含Fe3+)。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有_______。
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
(3)硝化细菌可利用氧气和自身的酶,将酸性土壤中的
 氧化为
氧化为 ,则该反应的离子方程式为
,则该反应的离子方程式为
您最近一年使用:0次
解题方法
3 . 双氧水和84消毒液是生活中常用的两种消毒剂,了解物质的性质是科学合理使用化学品的基础和前提,请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质
①从化合价上看H2O2既有氧化性又有还原性,理由是_______ ;
②上述实验能证明H2O2具有还原性的是_______ (填序号);
(2)84消毒液的有效成分为NaClO,某游泳馆的工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。化学兴趣小组的同学猜测可能是NaClO与H2O2反应产生O2促进藻类快速生长,由此推断该反应中H2O2是_______ (填“氧化剂”或“还原剂”)。
(1)某同学设计如下实验研究H2O2的性质
| 序号 | 实验 | 实验现象 |
| ⅰ | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ⅱ | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
②上述实验能证明H2O2具有还原性的是
(2)84消毒液的有效成分为NaClO,某游泳馆的工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。化学兴趣小组的同学猜测可能是NaClO与H2O2反应产生O2促进藻类快速生长,由此推断该反应中H2O2是
您最近一年使用:0次
名校
解题方法
4 . (1)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现的性质是________
A.酸性 B.氧化性 C.还原性 D.碱性
若反应生成标准状况下11.2 L NO,则被还原的HNO3为___________ mol,转移电子为___________ mol。
(2)若NA为阿伏加德罗常数,3.4g氨气中所含氢原子数为___________ ;所含质子数为________
(3)同温同压下,相同体积的氢气和气体A的质量分别是0.2g和3.4g,则气体A的摩尔质量为___________
A.酸性 B.氧化性 C.还原性 D.碱性
若反应生成标准状况下11.2 L NO,则被还原的HNO3为
(2)若NA为阿伏加德罗常数,3.4g氨气中所含氢原子数为
(3)同温同压下,相同体积的氢气和气体A的质量分别是0.2g和3.4g,则气体A的摩尔质量为
您最近一年使用:0次
名校
5 . 利用下图,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丁属于________ (“酸性”或“碱性”)氧化物;
(2)图中甲、乙、丙、戊中,属于电解质的是________________ (填化学式);根据氯元素的化合价判断,乙物质________ ;
A.只有氧化性B.只有还原性C.既有氧化性又有还原性
(3)电解甲溶液制备己的化学反应为: (未配平),则配平后参与反应的甲与H2O的物质的量之比是
(未配平),则配平后参与反应的甲与H2O的物质的量之比是________ ;
(4)庚是漂白粉的有效成分,用乙制取庚的化学方程式为________________________________ 。

(1)丁属于
(2)图中甲、乙、丙、戊中,属于电解质的是
A.只有氧化性B.只有还原性C.既有氧化性又有还原性
(3)电解甲溶液制备己的化学反应为:
 (未配平),则配平后参与反应的甲与H2O的物质的量之比是
(未配平),则配平后参与反应的甲与H2O的物质的量之比是(4)庚是漂白粉的有效成分,用乙制取庚的化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 我国科学家陈竺院士获得一项国际大奖——美国血液学会颁发的欧尼斯特博特勒奖。该奖是为表彰他利用砒霜治疗“急性早幼粒细胞白血病(APL)”研究中取得的突出成就。

已知砒霜(As2O3)与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O
(1)请用双线桥法标出电子转移的方向和数目:__ 。
(2)As2O3在上述反应中显示出来的性质是__ 。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的还原产物是__ 。
(4)若生成1分子AsH3,则转移的电子数为__ 。

已知砒霜(As2O3)与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O
(1)请用双线桥法标出电子转移的方向和数目:
(2)As2O3在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的还原产物是
(4)若生成1分子AsH3,则转移的电子数为
您最近一年使用:0次
2020-10-10更新
|
122次组卷
|
2卷引用:湖南省长沙市周南中学2020-2021学年高一上学期第一次月考化学试题
名校
7 . 我国科学家陈竺院士获得一项国际大奖——美国血液学会颁发的欧尼斯特博特勒奖。该奖是为表彰他利用砒霜治疗“急性早幼粒细胞白血病(APL)”研究中取得的突出成就。

已知砒霜(As2O3)与Zn可以发生如下反应:As2O3+6Zn+6H2SO4==2AsH3+6ZnSO4+3H2O(已知AsH3中As的化合价为-3价)
(1)请用单线桥法标出电子转移的方向和数目:____________ 。
(2)As2O3在上述反应中显示出来的性质是_________________ 。
A.氧化性B.还原性C.酸性D.碱性
(3)该反应的还原产物是_______ 。
(4)若生成1分子AsH3,则转移的电子数为________ 。

已知砒霜(As2O3)与Zn可以发生如下反应:As2O3+6Zn+6H2SO4==2AsH3+6ZnSO4+3H2O(已知AsH3中As的化合价为-3价)
(1)请用单线桥法标出电子转移的方向和数目:
(2)As2O3在上述反应中显示出来的性质是
A.氧化性B.还原性C.酸性D.碱性
(3)该反应的还原产物是
(4)若生成1分子AsH3,则转移的电子数为
您最近一年使用:0次
名校
8 . 已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4 2AsH3↑+6ZnSO4+3H2O。
2AsH3↑+6ZnSO4+3H2O。
(1)请用双线桥法标出电子转移的方向和数目____________________________________ 。
(2)As2O3在上述反应中显示出来的性质是____________ (填序号)。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化产物是__________ ,还原产物是________ 。
(4)若生成0.2 mol AsH3,则转移的电子数为___________ 。
 2AsH3↑+6ZnSO4+3H2O。
2AsH3↑+6ZnSO4+3H2O。(1)请用双线桥法标出电子转移的方向和数目
(2)As2O3在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化产物是
(4)若生成0.2 mol AsH3,则转移的电子数为
您最近一年使用:0次
2017-11-27更新
|
2991次组卷
|
13卷引用:2014-2015学年湖南省益阳市箴言中学高一12月月考化学试卷
2014-2015学年湖南省益阳市箴言中学高一12月月考化学试卷(已下线)2.3.1 氧化还原反应高中化学人教版 必修1 第二章 化学物质及其变化 3.氧化还原反应 氧化还原反应2018年高一化学(人教版)必修1综合题型练习卷:氧化还原反应人教版高中化学必修一 第二章化学物质及其变化 单元测试题河南省安阳市第二中学2018-2019学年高一上学期期中考试化学试题【校级联考】吉林省辽源市田家炳高级中学(第六十六届友好学校)2018-2019学年高一上学期期末联考化学试题(已下线)2019年10月2日《每日一题》必修1—— 氧化还原反应电子转移方向和数目的表示(已下线)第二章 化学物质及其变化(基础过关)-2020-2021学年高一化学单元测试定心卷(人教版必修1)(已下线)2.3.1 氧化还原反应(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)新疆维吾尔自治区喀什第二中学2020-2021学年高一上学期期末考试化学试题(已下线)易错专题07 氧化还原反应电子转移的表示及方程式的书写-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)广东省南阳中学、清新一中、佛冈一中、连州中学、连 山中学五校2022-2023学年高一上学期12月联考化学试题
9 . 利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2中S元素处于中间价态,既有氧化性又有还原性;
②将SO2通入酸性KMnO4溶液中,溶液由紫红色褪至无色,SO2表现出_______ 性质。
A.氧化性 B.还原性 C.既有氧化性又有还原性
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成。其中SiO2属于_______ (填“酸性”、“碱性”或“两性”,下同)氧化物,Al2O3属于_______ 氧化物。
②现取一份蛇纹石试样进行实验:
Ⅰ.先将其溶于过量的盐酸中,过滤,滤渣的主要成分是_______ ;
Ⅱ.再向滤液中加入NaOH溶液至过量,过滤,滤渣中的主要成分是_______ 。
(1)从化合价的角度可以预测物质的性质。
①SO2中S元素处于中间价态,既有氧化性又有还原性;
②将SO2通入酸性KMnO4溶液中,溶液由紫红色褪至无色,SO2表现出
A.氧化性 B.还原性 C.既有氧化性又有还原性
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成。其中SiO2属于
②现取一份蛇纹石试样进行实验:
Ⅰ.先将其溶于过量的盐酸中,过滤,滤渣的主要成分是
Ⅱ.再向滤液中加入NaOH溶液至过量,过滤,滤渣中的主要成分是
您最近一年使用:0次
名校
10 . 下图为元素周期表的一部分,请参照① ⑨在表中的位置,回答下列问题:
⑨在表中的位置,回答下列问题:
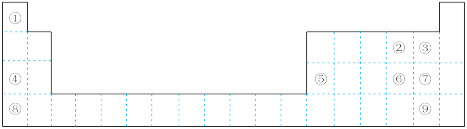
(1)最高价氧化物对应水化物碱性最强的是_______ (填化学式),氢化物热稳定性最强的是_______ (填电子式)。
(2)②③④的原子半径从大到小的顺序是_______ (填元素符号)。④⑤⑧的阳离子中氧化性最强的是_______ (填离子符号)。
(3)元素⑥的非金属性比⑦_______ (填“强”或“弱”),请从原子结构的角度解释:_______ 。
(4)现在含有元素硒( )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,硒在周期表中的位置为
个电子层,硒在周期表中的位置为_______ ,则下列叙述中正确的是_______ 。
A.原子序数为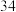
B.气态氢化物的稳定性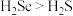
C. 不能与氢氧化钠反应
不能与氢氧化钠反应
D. 既有氧化性又有还原性
既有氧化性又有还原性
(5)①和④可形成 型离子化合物,该离子化合物的电子式为
型离子化合物,该离子化合物的电子式为_______ ,其与水反应放出气体的化学方程式为_______ 。
 ⑨在表中的位置,回答下列问题:
⑨在表中的位置,回答下列问题:
(1)最高价氧化物对应水化物碱性最强的是
(2)②③④的原子半径从大到小的顺序是
(3)元素⑥的非金属性比⑦
(4)现在含有元素硒(
 )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,硒在周期表中的位置为
个电子层,硒在周期表中的位置为A.原子序数为
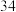
B.气态氢化物的稳定性
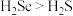
C.
 不能与氢氧化钠反应
不能与氢氧化钠反应D.
 既有氧化性又有还原性
既有氧化性又有还原性(5)①和④可形成
 型离子化合物,该离子化合物的电子式为
型离子化合物,该离子化合物的电子式为
您最近一年使用:0次
2023-02-05更新
|
278次组卷
|
2卷引用:湖南省郴州市苏仙区多校2022-2023学年高一上学期期末线上联考化学试题



