1 . 氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。___________ 。
a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2 2NaCl
2NaCl
b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为___________ 。
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为___________ 。
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)___________ 。
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和___________ 。
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO =CaCO3↓和
=CaCO3↓和___________ 。
③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和___________ 。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。

a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2
 2NaCl
2NaCl b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO
 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO
 =CaCO3↓和
=CaCO3↓和③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和
您最近一年使用:0次
2 . 化学与人类生活、生产密切相关。请根据题意填空:
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维,用于制造光导纤维的基本原料是___________ (填“SiO2”或“Si”);
(2)“84”消毒液在新冠肺炎疫情防控中发挥了很大的作用,已知“84”消毒液的制备原理为Cl2+2NaOH=NaCl+NaClO+H2O,则“84”消毒液的有效成分为___________ (填“NaCl”或“NaClO”);
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质,请完成该反应的化学方程式:2CO+2NO 2CO2+
2CO2+___________ 。
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维,用于制造光导纤维的基本原料是
(2)“84”消毒液在新冠肺炎疫情防控中发挥了很大的作用,已知“84”消毒液的制备原理为Cl2+2NaOH=NaCl+NaClO+H2O,则“84”消毒液的有效成分为
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质,请完成该反应的化学方程式:2CO+2NO
 2CO2+
2CO2+
您最近一年使用:0次
3 . 研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示置换反应的是___________ (填字母)。
①下列应用或事实与胶体的性质有关系的是___________ 。
A.在 溶液中滴加
溶液中滴加 溶液出现红褐色沉淀
溶液出现红褐色沉淀
B.在河流入海处易形成三角洲
C.用石膏或盐卤点制豆腐
②提纯明胶的水溶液和 溶液装置是下列中的
溶液装置是下列中的___________ (填序号)。___________ (填化学式),若该反应生成标准状况下的气体为8.96L,则该反应中转移电子的数目为___________ 。
(4)中国古代著作中有“银针验毒”的记录,其原理为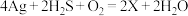 ,则X的化学式是
,则X的化学式是___________ ,其中 在该反应中
在该反应中___________ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(1)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示置换反应的是

①下列应用或事实与胶体的性质有关系的是
A.在
 溶液中滴加
溶液中滴加 溶液出现红褐色沉淀
溶液出现红褐色沉淀B.在河流入海处易形成三角洲
C.用石膏或盐卤点制豆腐
②提纯明胶的水溶液和
 溶液装置是下列中的
溶液装置是下列中的A. B.
B. 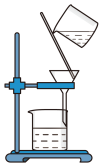 C.
C.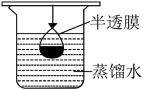
(4)中国古代著作中有“银针验毒”的记录,其原理为
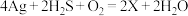 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
您最近一年使用:0次
4 . 高铁酸钾( 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 价。
(2)过程①中活细菌表现了___________ (填“氧化”或“还原”)性。
(3)净水利用了 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式___________ 。
(4)根据上述原理分析,作水处理剂时, 的作用有
的作用有___________ 和净水剂。
(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是___________ 。(填化学式)
(6)已知铁与水蒸气发生如下反应: ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:___________ ;该反应的还原产物是___________ 。
 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。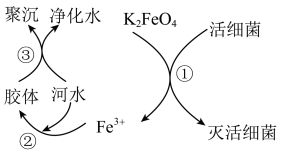
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活细菌表现了
(3)净水利用了
 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式(4)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是
(6)已知铁与水蒸气发生如下反应:
 ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:
您最近一年使用:0次
5 . 铁与空气接触时会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖与金属接触的一侧是FeO,与空气接触的一侧是 ,而中间则是
,而中间则是 。
。
(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的___________ (填化学式)。
(2) 的一种用途是
的一种用途是___________ 。(填“用作油漆、涂料 ”或“磁电机”);
(3)FeO可作化妆品中的色素,它还能进行一系列转化: 。
。
① 时应加入的试剂是
时应加入的试剂是___________ (填“H2SO4”或“Na2SO4”)。
②“速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入___________ (填“KSCN”或“K2SO4”),若出现___________ (填“红色”或“浅绿色”)现象,则证明该药物已变质。
③在 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成___________ (填“红褐色”或“黄色”),其中沉淀颜色发生变化的化学方程式为___________ 。
 ,而中间则是
,而中间则是 。
。(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的
(2)
 的一种用途是
的一种用途是(3)FeO可作化妆品中的色素,它还能进行一系列转化:
 。
。①
 时应加入的试剂是
时应加入的试剂是②“速力菲”(主要有效成分是
 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入③在
 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
您最近一年使用:0次
6 . 有以下9种熟悉的元素的单质及熟悉的化合物:氯化氢、二氧化硫、铜片、食盐、生石灰、一氧化氮、纯碱、镁片和木炭粉,结合下图中①~⑤选择适当的物质,使有连线的两物质能发生反应。
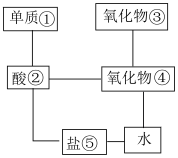
(1)请推断它们的化学式分别为①___________ ;②___________ ;③___________ ;⑤___________ 。
(2)写出下列序号之间的化学方程式
①和②:___________ ;②和④:___________ ;③和④:___________ 。

(1)请推断它们的化学式分别为①
(2)写出下列序号之间的化学方程式
①和②:
您最近一年使用:0次
7 . 准确掌握化学基本概念和研究方法是学好化学的重要手段。按要求回答问题:
(1)有以下物质:
①熔融氯化钠;②铝;③乙醇;④氨水溶液;⑤氯化氢气体;⑥NaHSO4固体
其中能导电的是___________ (填序号,下同);属于电解质的是___________ ;
属于非电解质的有___________ 。
(2)关于酸、碱、盐的下列各种说法中,正确的是___________ (填字母)。
A.化合物电离时,电离出的阳离子有氢离子的是酸
B.化合物电离时,电离出的阴离子有氢氧根离子的是碱
C.化合物电离时,电离出金属阳离子(或铵根离子)和酸根离子的是盐
(3)有些食品的包装袋中有一个小纸袋,上面标注“干燥剂”,其主要成分是生石灰。
ⅰ.下列关于生石灰的说法正确的是___________ (填字母)。
A.CaO是纯净物,属于盐类 B.CaO既是金属氧化物,也是碱性氧化物
C.CaO是纯净物,属于碱类 D.小纸袋中的物质可长期持续作干燥剂
ⅱ. 某同学将生石灰和浓硫酸、NaOH固体等物质划分为一类。该同学的分类依据为___________ (填字母)。
A.酸 B.碱 C.氧化物 D.干燥剂
iii. 生石灰可作干燥剂的理由是___________ (用化学方程式表示)。
(1)有以下物质:
①熔融氯化钠;②铝;③乙醇;④氨水溶液;⑤氯化氢气体;⑥NaHSO4固体
其中能导电的是
属于非电解质的有
(2)关于酸、碱、盐的下列各种说法中,正确的是
A.化合物电离时,电离出的阳离子有氢离子的是酸
B.化合物电离时,电离出的阴离子有氢氧根离子的是碱
C.化合物电离时,电离出金属阳离子(或铵根离子)和酸根离子的是盐
(3)有些食品的包装袋中有一个小纸袋,上面标注“干燥剂”,其主要成分是生石灰。
ⅰ.下列关于生石灰的说法正确的是
A.CaO是纯净物,属于盐类 B.CaO既是金属氧化物,也是碱性氧化物
C.CaO是纯净物,属于碱类 D.小纸袋中的物质可长期持续作干燥剂
ⅱ. 某同学将生石灰和浓硫酸、NaOH固体等物质划分为一类。该同学的分类依据为
A.酸 B.碱 C.氧化物 D.干燥剂
iii. 生石灰可作干燥剂的理由是
您最近一年使用:0次
名校
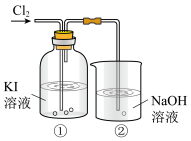
8 . 某研究小组利用下图所示装置探究卤素的性质。___________ (填“氧化性”或“还原性”)。
(2)①中溶液有I2生成,发生反应的化学方程式是___________ 。
(3)②中NaOH溶液的作用是吸收多余的氯气,发生反应的离子方程式是___________ 。
(2)①中溶液有I2生成,发生反应的化学方程式是
(3)②中NaOH溶液的作用是吸收多余的氯气,发生反应的离子方程式是
您最近一年使用:0次
名校
9 . 有下列物质:①过氧化钠、②氧化铝、③硅、④二氧化硅。请根据它们的用途填空:
(1)能作光导纤维的是___________ (填序号,下同)。
(2)可用于呼吸面具中作为氧气来源的是___________ 。
(3)能作耐火材料的金属氧化物是___________ 。
(1)能作光导纤维的是
(2)可用于呼吸面具中作为氧气来源的是
(3)能作耐火材料的金属氧化物是
您最近一年使用:0次
10 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ 中。
(2)除去碳酸钠固体中碳酸氢钠的方法是______________ 。
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”)。
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______________ 。
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于__________ (填“碱性”或“两性”)氧化物。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)除去碳酸钠固体中碳酸氢钠的方法是
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
您最近一年使用:0次



