名校
1 . 柠檬酸亚铁(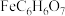 ,摩尔质量:246
,摩尔质量:246 )在食品工业中做营养增补剂,可用于乳制品等。一种用硫铁矿(成分为60%
)在食品工业中做营养增补剂,可用于乳制品等。一种用硫铁矿(成分为60%  、
、 、
、 及其他杂质)为原料来制备柠檬酸亚铁的流程如图所示:
及其他杂质)为原料来制备柠檬酸亚铁的流程如图所示:
①“焙烧”生成了铁红;
②常温下,柠檬酸(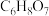 )是一种三元弱酸;
)是一种三元弱酸;
③“还原”时 发生的反应为
发生的反应为 。
。
请回答下列问题:
(1)焙烧时气体与矿料逆流而行,目的是________________ ,请写出焙烧过程中硫铁矿发生反应的化学方程式:_________________ 。
(2)滤渣1的主要成分是___________ (写化学式)。
(3)柠檬酸亚铁(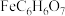 )是一种
)是一种___________ (填“正”“酸式”或“碱式”)盐。
(4)“沉铁”时需控制温度在32℃左右,温度不能过高的原因是________________ 。
(5)在制备过程中,若条件控制不当,容易生成 ,请写出检验
,请写出检验 所用试剂及现象:
所用试剂及现象:______________ 。
(6)某工厂用1kg硫铁矿经上述流程制得1.6kg柠檬酸亚铁,则柠檬酸亚铁的产率为________ (保留两位有效数字)。
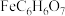 ,摩尔质量:246
,摩尔质量:246 )在食品工业中做营养增补剂,可用于乳制品等。一种用硫铁矿(成分为60%
)在食品工业中做营养增补剂,可用于乳制品等。一种用硫铁矿(成分为60%  、
、 、
、 及其他杂质)为原料来制备柠檬酸亚铁的流程如图所示:
及其他杂质)为原料来制备柠檬酸亚铁的流程如图所示:
①“焙烧”生成了铁红;
②常温下,柠檬酸(
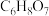 )是一种三元弱酸;
)是一种三元弱酸;③“还原”时
 发生的反应为
发生的反应为 。
。请回答下列问题:
(1)焙烧时气体与矿料逆流而行,目的是
(2)滤渣1的主要成分是
(3)柠檬酸亚铁(
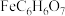 )是一种
)是一种(4)“沉铁”时需控制温度在32℃左右,温度不能过高的原因是
(5)在制备过程中,若条件控制不当,容易生成
 ,请写出检验
,请写出检验 所用试剂及现象:
所用试剂及现象:(6)某工厂用1kg硫铁矿经上述流程制得1.6kg柠檬酸亚铁,则柠檬酸亚铁的产率为
您最近一年使用:0次
名校
2 . 元素周期表是化学史上重要的里程碑之一,下表是现行长式周期表的一部分。结合下表用化学用语回答问题:
(1)上表元素①~⑦中,非金属性最强的是___________ 。
(2)元素⑦为铁元素,其在周期表中的位置为___________ ,写出其单质与⑤的单质反应的化学方程式___________ 。
(3)可以用元素③的氢化物的水溶液溶蚀玻璃生产磨砂玻璃,写出反应的化学方程式___________ 。
(4)元素②④⑥简单离子半径由大到小为___________ 。
(5)元素④与元素①形成化合物X,写出X的电子式___________ ,其化学键类型为___________ ,X在野外能做生氢剂,其与水反应生氢的反应中,氧化剂为___________ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ||||||||||||||||
| ⑥ | ⑦ | ||||||||||||||||
(2)元素⑦为铁元素,其在周期表中的位置为
(3)可以用元素③的氢化物的水溶液溶蚀玻璃生产磨砂玻璃,写出反应的化学方程式
(4)元素②④⑥简单离子半径由大到小为
(5)元素④与元素①形成化合物X,写出X的电子式
您最近一年使用:0次
3 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的 以上。工业制硅,先制得粗硅,再制得高纯硅。
以上。工业制硅,先制得粗硅,再制得高纯硅。
I.请回答:
(1)工业制粗硅反应的化学方程式为_______ ,制取的高纯硅可用于_______ (写出硅的一种用途)。
(2)工业制粗硅的中间产物 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和一种气体单质,请写出化学反应方程式
和一种气体单质,请写出化学反应方程式_______ 。
II.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
① ,
,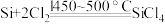
② 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。
请回答下列问题:
(3)A中装浓盐酸的仪器名称是_______ 。
(4)装置B的作用是_______ 。
(5)为了更好的收集产品,可以将试剂瓶E放在_______ 中使四氯化硅液化收集。
(6)能否将装置G改成如图装置来吸收尾气?_______ (填“能”或“不能”),原因:_______ 。
 以上。工业制硅,先制得粗硅,再制得高纯硅。
以上。工业制硅,先制得粗硅,再制得高纯硅。I.请回答:
(1)工业制粗硅反应的化学方程式为
(2)工业制粗硅的中间产物
 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和一种气体单质,请写出化学反应方程式
和一种气体单质,请写出化学反应方程式II.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。

①
 ,
,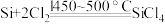
②
 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。请回答下列问题:
(3)A中装浓盐酸的仪器名称是
(4)装置B的作用是
(5)为了更好的收集产品,可以将试剂瓶E放在
(6)能否将装置G改成如图装置来吸收尾气?
您最近一年使用:0次
名校
4 . Vilsmeier试剂是化学反应中的一种重要原料,由以下反应生成。W、X、Y、Z、Q为短周期主族元素,只有X、Y、Z在同一周期,Y的单质在空气中含量最多,W元素的一种核素不含中子,该五种元素的原子在以上结构中均达到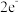 或
或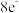 的稳定结构。
的稳定结构。
(1)写出各元素的元素符号:X_______ ;Z_______ 。
(2)Q元素在元素周期表中的位置为_______ 。
(3)Vilsmeier试剂中存在的化学键类型有_______ 和_______ 。
(4)X、Y、Z三元素分别形成的简单氢化物中,稳定性最强的是_______ (填分子式)。
(5)写出两种由W和Y形成的10电子微粒:_______ 、_______ 。
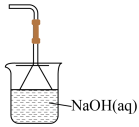
(6)某同学利用下图装置来制取X的单质,并探究该淡黄色的固体反应物是否变质。_______ 。
②测定气体体积时需要在反应停止后的操作顺序为_______ 。
A.向下移动漏斗,使漏斗中液面与量气管液面相平
B.视线与量气管中的凹液面相平进行读数
C.冷却气体至室温
③若用电子天平称取 固体反应物进行实验,反应完全后,测得标准状况下气体体积为
固体反应物进行实验,反应完全后,测得标准状况下气体体积为 ,说明该固体反应物已经
,说明该固体反应物已经_____ (填“完全”或“部分”或“没有”)变质。(忽略加入的水的体积对气体体积的影响)
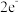 或
或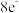 的稳定结构。
的稳定结构。
(1)写出各元素的元素符号:X
(2)Q元素在元素周期表中的位置为
(3)Vilsmeier试剂中存在的化学键类型有
(4)X、Y、Z三元素分别形成的简单氢化物中,稳定性最强的是
(5)写出两种由W和Y形成的10电子微粒:
(6)某同学利用下图装置来制取X的单质,并探究该淡黄色的固体反应物是否变质。
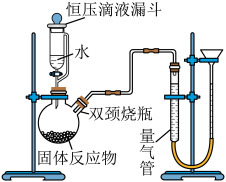
②测定气体体积时需要在反应停止后的操作顺序为
A.向下移动漏斗,使漏斗中液面与量气管液面相平
B.视线与量气管中的凹液面相平进行读数
C.冷却气体至室温
③若用电子天平称取
 固体反应物进行实验,反应完全后,测得标准状况下气体体积为
固体反应物进行实验,反应完全后,测得标准状况下气体体积为 ,说明该固体反应物已经
,说明该固体反应物已经
您最近一年使用:0次
5 . 实验室需配制 的
的 溶液,请回答下列问题:
溶液,请回答下列问题:
(1)需用托盘天平称取 固体的总质量为
固体的总质量为_______ g。
(2)在此溶液的配制过程中,有以下基本实验步骤,其中只需进行一次的操作是_______ (填序号)。
①称量(用托盘天平) ②溶解 ③转移 ④洗涤 ⑤定容 ⑥摇匀
(3)配制 的
的 溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有
溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有_______ 、_______ 。
(4)配制 的
的 溶液,配制过程中所涉及的下列相关操作正确的是
溶液,配制过程中所涉及的下列相关操作正确的是_______ 。
 的
的 溶液,请回答下列问题:
溶液,请回答下列问题:(1)需用托盘天平称取
 固体的总质量为
固体的总质量为(2)在此溶液的配制过程中,有以下基本实验步骤,其中只需进行一次的操作是
①称量(用托盘天平) ②溶解 ③转移 ④洗涤 ⑤定容 ⑥摇匀
(3)配制
 的
的 溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有
溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有(4)配制
 的
的 溶液,配制过程中所涉及的下列相关操作正确的是
溶液,配制过程中所涉及的下列相关操作正确的是a. 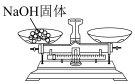 b.
b. 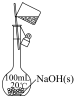 c.
c. 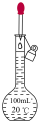 d.
d.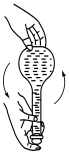
A.用蒸馏水溶解 固体后,立即转入容量瓶中 固体后,立即转入容量瓶中 |
B.称量 固体时,将药品和砝码放反了 固体时,将药品和砝码放反了 |
| C.定容时俯视刻度线 |
| D.定容后发现溶液的凹液面最低点高于刻度线,用胶头滴管将多余的液体吸出 |
您最近一年使用:0次
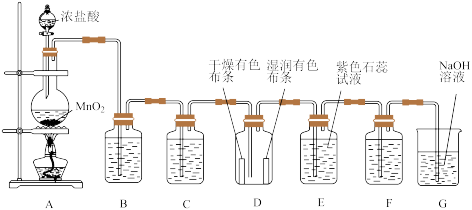
6 . 某化学兴趣小组用如图实验装置和药品制备氯气并检测氯气的相关性质,请回答问题。_______ ;该反应中氧化剂和还原剂物质的量之比为______ 。
(2)装置B中的试剂是_______ ,作用是_______ ;装置C中的试剂是_______ ,作用是_______ 。
(3)装置D中的现象是_______ ,通过这一现象能得出的结论是_______ 。
(4)若要证明氯气具有氧化性,可在装置F中盛装下列试剂中的_______ (填序号),证明氯气有氧化性的实验现象是_______ ,发生的化学方程式是_______ 。
a.酸性KMnO4溶液 b.FeCl3溶液 c.CuSO4溶液 d.淀粉碘化钾溶液
(5)装置G的作用是_______ 。
(2)装置B中的试剂是
(3)装置D中的现象是
(4)若要证明氯气具有氧化性,可在装置F中盛装下列试剂中的
a.酸性KMnO4溶液 b.FeCl3溶液 c.CuSO4溶液 d.淀粉碘化钾溶液
(5)装置G的作用是
您最近一年使用:0次
解题方法
7 . I.某校化学课外小组为了鉴别Na2CO3和NaHCO3两种白色固体,用不同的方法做了以下实验,如图所示:
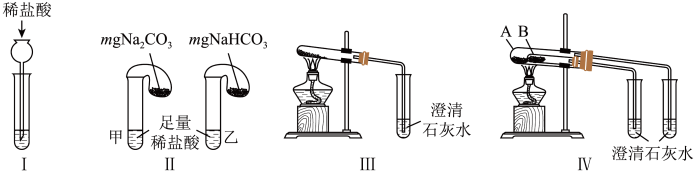
(1)方法Ⅰ,为鉴别Na2CO3和NaHCO3两种白色固体,分别取样配成溶液,再逐滴加入稀盐酸。若将稀盐酸改为Ba(OH)2溶液_______ (填“能”或“不能”)鉴别。
(2)方法Ⅱ,若固体质量相同且稀盐酸足量时,气球鼓起较小的是_______ (填“甲”或“乙”)试管。
(3)方法Ⅲ、Ⅳ均能鉴别这两种物质,加热试管发生反应的化学方程式为________ 。方法Ⅳ中NaHCO3应放在________ (填“A”或“B”)试管中。
Ⅱ.某同学欲配制450mL0.2mol/LNaOH溶液,试回答下列问题:
(4)需要称取NaOH固体的质量为_______ 。
(5)配制过程中若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?没有洗涤烧杯和玻璃棒_______ ;加蒸馏水时不慎超过了刻度线然后用胶头滴管吸掉多余的溶液至刻度线_______ ;定容时俯视刻度线_______ 。

(1)方法Ⅰ,为鉴别Na2CO3和NaHCO3两种白色固体,分别取样配成溶液,再逐滴加入稀盐酸。若将稀盐酸改为Ba(OH)2溶液
(2)方法Ⅱ,若固体质量相同且稀盐酸足量时,气球鼓起较小的是
(3)方法Ⅲ、Ⅳ均能鉴别这两种物质,加热试管发生反应的化学方程式为
Ⅱ.某同学欲配制450mL0.2mol/LNaOH溶液,试回答下列问题:
(4)需要称取NaOH固体的质量为
(5)配制过程中若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?没有洗涤烧杯和玻璃棒
您最近一年使用:0次
解题方法
8 . 已知A~P均为中学化学中的常见物质,其中A是工业生产中应用最广泛的金属单质,D,M,X均为气体单质,且X为黄绿色,F也是气体,G为淡黄色固体,H常温下为无色液体,它们有如图的转化关系(部分产物未列出)。请回答以下问题:

(1)A是_______ ,F是_______ 。(填化学式)
(2)反应②的化学方程式为________ 。
(3)反应③的离子方程式为_______ ;若要通过该反应制取16gM,理论上需要G的质量为_______ 。
(4)若C溶液中混有少量E溶液的杂质,为了除掉E溶液,可向该混合液中加入过量的________ ;该反应的离子方程式为_______ 。
(5)N在空气中转变为P的现象是_______ ;化学方程式为_______ 。

(1)A是
(2)反应②的化学方程式为
(3)反应③的离子方程式为
(4)若C溶液中混有少量E溶液的杂质,为了除掉E溶液,可向该混合液中加入过量的
(5)N在空气中转变为P的现象是
您最近一年使用:0次
解题方法
9 . 配制100mL1mol/LNaOH溶液,请完成下列填空。
(1)计算并用“托盘天平称”取_____ gNaOH。
(2)配制过程部分操作如下图所示(没有按先后排序),正确的先后顺序为_____ 。
_____→_____→_____→_____→_____→E(填写“下列字母”)。
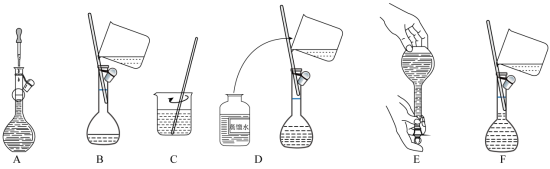
(3)判断下列操作对NaOH溶液的物质的量浓度的影响(填“偏高”“偏低”或“无影响”)。
①定容时俯视刻度线,配得溶液浓度将_____ 。
②容量瓶中原有少量蒸馏水,配得溶液浓度将_____ 。
(1)计算并用“托盘天平称”取
(2)配制过程部分操作如下图所示(没有按先后排序),正确的先后顺序为
_____→_____→_____→_____→_____→E(填写“下列字母”)。

(3)判断下列操作对NaOH溶液的物质的量浓度的影响(填“偏高”“偏低”或“无影响”)。
①定容时俯视刻度线,配得溶液浓度将
②容量瓶中原有少量蒸馏水,配得溶液浓度将
您最近一年使用:0次
解题方法
10 . 下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。
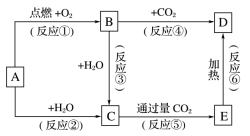
请填写下列空白:
(1)B为_____ (填“物质的颜色”)固体,D的化学式为_____ 。
(2)下列试剂不能鉴别等浓度D的水溶液和E的水溶液的是_____ (填“标号”)。
a.酚酞溶液 b.稀盐酸溶液 c.澄清石灰水 d.CaCl2溶液
(3)A→C反应的化学方程式:_____ 。
(4)B→C反应的离子方程式:_____ 。

请填写下列空白:
(1)B为
(2)下列试剂不能鉴别等浓度D的水溶液和E的水溶液的是
a.酚酞溶液 b.稀盐酸溶液 c.澄清石灰水 d.CaCl2溶液
(3)A→C反应的化学方程式:
(4)B→C反应的离子方程式:
您最近一年使用:0次



