解题方法
1 . 煤的化学活性是评价煤气化或燃烧性能的一项重要指标,可用与焦炭(由煤样制得)反应的CO2的转化率 来表示。研究小组设计模拟实验探究煤燃烧产物的转化率装置如下:
来表示。研究小组设计模拟实验探究煤燃烧产物的转化率装置如下:___________ 。
(2)装置Ⅰ中,仪器a的名称是___________ ;b的作用是___________ 。
(3)装置Ⅱ中,CO2从下口通入的原因是___________ 。气体X的成分有:___________ 。
(4)装置Ⅲ中,d中的现象是___________ 。e中生成的固体为Ag,则反应的离子方程式为___________ 。
 来表示。研究小组设计模拟实验探究煤燃烧产物的转化率装置如下:
来表示。研究小组设计模拟实验探究煤燃烧产物的转化率装置如下:
(2)装置Ⅰ中,仪器a的名称是
(3)装置Ⅱ中,CO2从下口通入的原因是
(4)装置Ⅲ中,d中的现象是
您最近一年使用:0次
解题方法
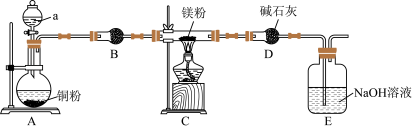
2 . 镁及其化合物是实验设计的热点载体。某学习小组设计实验探究镁与二氧化氮反应的产物,实验装置如图所示。 能与水反应;②反应完后E中有
能与水反应;②反应完后E中有 。
。
回答下列问题:
(1)仪器a的名称为___________ ;a中试剂是___________ 。
(2)实验时,为了防止Mg与空气中氧气等反应,操作为___________ 。
(3)实验测得Mg与 反应生成MgO、
反应生成MgO、 和
和 ,其中
,其中 和
和 的物质的量相等,则C中反应的化学方程式为
的物质的量相等,则C中反应的化学方程式为___________ 。装置D的作用是___________ 。
(4)E装置中发生反应的离子方程式为___________ 。
(5)写出氮化镁与水反应的化学方程式___________ 。
(6)已知浓硝酸分解反应为: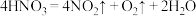 ,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出
,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出 气体能支持燃烧的说法,你认为该说法正确吗?并说明理由
气体能支持燃烧的说法,你认为该说法正确吗?并说明理由___________ 。
 能与水反应;②反应完后E中有
能与水反应;②反应完后E中有 。
。回答下列问题:
(1)仪器a的名称为
(2)实验时,为了防止Mg与空气中氧气等反应,操作为
(3)实验测得Mg与
 反应生成MgO、
反应生成MgO、 和
和 ,其中
,其中 和
和 的物质的量相等,则C中反应的化学方程式为
的物质的量相等,则C中反应的化学方程式为(4)E装置中发生反应的离子方程式为
(5)写出氮化镁与水反应的化学方程式
(6)已知浓硝酸分解反应为:
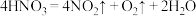 ,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出
,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出 气体能支持燃烧的说法,你认为该说法正确吗?并说明理由
气体能支持燃烧的说法,你认为该说法正确吗?并说明理由
您最近一年使用:0次
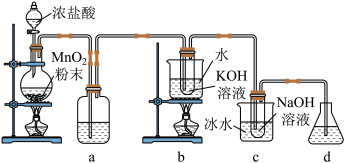
3 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
(1)盛放浓盐酸的仪器名称是___________ ,a的作用为___________ 。
(2)d中可选用试剂___________(填字母)。
(3)浓盐酸与二氧化锰反应的离子方程式是___________ 。
(4)b中采用的加热方式是___________ ,化学反应的离子方程式是___________ 。
(5)c中采用冰水浴冷却的目的是___________ 。
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显___________ 色。可知该条件下KClO3的氧化能力___________ (填“大于”或“小于”)NaClO。
(1)盛放浓盐酸的仪器名称是
(2)d中可选用试剂___________(填字母)。
| A.Na2S | B.NaCl | C.Ca(OH)2 | D.H2SO4 |
(3)浓盐酸与二氧化锰反应的离子方程式是
(4)b中采用的加热方式是
(5)c中采用冰水浴冷却的目的是
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显
您最近一年使用:0次
解题方法
4 . 以硫铁矿(主要成分为 ,含有少量
,含有少量 )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体( )的工艺流程如下:
)的工艺流程如下:
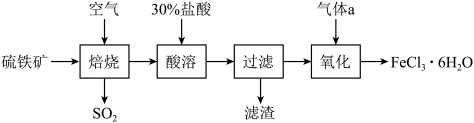
已知:氯化铁晶体受热会生成 ,最后得到
,最后得到 。回答下列问题:
。回答下列问题:
(1)“焙烧”时为加快反应速率可采取的方法有___________ (答出1点即可)。
(2)“焙烧”时反应的化学方程式为 ,则X的化学式为
,则X的化学式为___________ 。“酸溶”时反应的化学方程式为___________ 。
(3)氧化时通入的气体a为___________ (填化学式),反应的离子方程式为___________ 。
(4)焙烧排出的尾气中主要含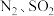 ,可用于尾气处理的试剂有
,可用于尾气处理的试剂有___________ (填标号)。
a.浓硫酸 b. 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液
(5)制取 晶体的操作包括蒸发浓缩、冷却结晶、过滤、洗涤、烘干。烘干时晶体需要减压,原因是
晶体的操作包括蒸发浓缩、冷却结晶、过滤、洗涤、烘干。烘干时晶体需要减压,原因是___________ 。
 ,含有少量
,含有少量 )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体( )的工艺流程如下:
)的工艺流程如下:
已知:氯化铁晶体受热会生成
 ,最后得到
,最后得到 。回答下列问题:
。回答下列问题:(1)“焙烧”时为加快反应速率可采取的方法有
(2)“焙烧”时反应的化学方程式为
 ,则X的化学式为
,则X的化学式为(3)氧化时通入的气体a为
(4)焙烧排出的尾气中主要含
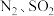 ,可用于尾气处理的试剂有
,可用于尾气处理的试剂有a.浓硫酸 b.
 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液(5)制取
 晶体的操作包括蒸发浓缩、冷却结晶、过滤、洗涤、烘干。烘干时晶体需要减压,原因是
晶体的操作包括蒸发浓缩、冷却结晶、过滤、洗涤、烘干。烘干时晶体需要减压,原因是
您最近一年使用:0次
解题方法
5 . ClO2是一种优良的消毒剂,浓度过高时易发生分解,常将其制成NaClO2固体,以便运输和贮存,过氧化氢法制备NaClO2固体的实验装置如图所示。
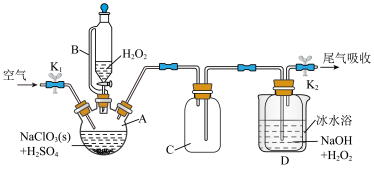
已知:①2NaClO3+ H2O2 + H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O;
②ClO2熔点-59℃、沸点11℃;H2O2沸点150℃。
请回答:
(1)仪器A的名称_______ ,仪器B支管的作用为_______ 。
(2)仪器C的作用是防倒吸,则冰水浴冷却的目的是_______ (任写一条)。
(3)空气流速过快或过慢,均降低NaClO2产率,试解释其原因_______ 。
(4)装置D中发生反应的化学方程式为_______ 。
(5)Cl-存在时会催化ClO2的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气。该过程可能经两步完成,请将其补充完整:
①_______ (用离子方程式表示);
②H2O2+Cl2=2Cl- +O2 + 2H+。

已知:①2NaClO3+ H2O2 + H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O;
②ClO2熔点-59℃、沸点11℃;H2O2沸点150℃。
请回答:
(1)仪器A的名称
(2)仪器C的作用是防倒吸,则冰水浴冷却的目的是
(3)空气流速过快或过慢,均降低NaClO2产率,试解释其原因
(4)装置D中发生反应的化学方程式为
(5)Cl-存在时会催化ClO2的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气。该过程可能经两步完成,请将其补充完整:
①
②H2O2+Cl2=2Cl- +O2 + 2H+。
您最近一年使用:0次
6 . 某无色稀溶液X中,可能含有下表所列离子中的一种或几种。
现取适量该溶液于锥形瓶中,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。

回答下列问题:
(1)仅通过观察颜色,可以判断溶液X中一定不存在的离子是_______ (用化学用语表示)。
(2)若Y是盐酸,则Oa段生成的沉淀为_______ (填化学式);ab段发生反应的离子为_______ (用化学用语表示),bc段发生反应的离子方程式为_______ ;取少量d点对应的上层清液于试管中,加入几滴硝酸银溶液,有白色沉淀生成,不能证明溶液X中含有 ,原因是
,原因是_______ 。
(3)若Y是NaOH溶液,则X中一定含有的离子是_______ ;ab段反应的离子方程式为_______ 。
| 阴离子 |  、 、 、 、 、 、 |
| 阳离子 |  、 、 、 、 、 、 、 、 |

回答下列问题:
(1)仅通过观察颜色,可以判断溶液X中一定不存在的离子是
(2)若Y是盐酸,则Oa段生成的沉淀为
 ,原因是
,原因是(3)若Y是NaOH溶液,则X中一定含有的离子是
您最近一年使用:0次
名校
解题方法
7 . 现用如图装置制取氯气,并用氯气制备 。回答下列问题:
。回答下列问题:
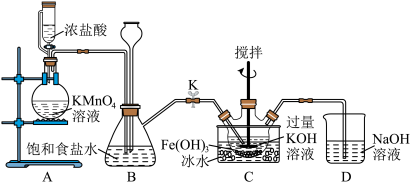
(1)盛浓盐酸的仪器名称为___________ ; 中铁元素的化合价为
中铁元素的化合价为___________ 。
(2)装置B有安全瓶作用,同时也可收集少量氯气,若关闭弹簧夹K,则B中的现象为___________ 。
(3)装置A中可产生 ,相应的离子方程式为
,相应的离子方程式为___________ 。
(4)装置C中制备 的化学反应方程式为
的化学反应方程式为___________ 。
(5)实验室可用间接碘量法测定所得 样品的纯度:称取
样品的纯度:称取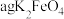 样品溶于淀粉
样品溶于淀粉 溶液中,调节
溶液中,调节 使混合液充分反应。用
使混合液充分反应。用 的
的 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗 标准溶液
标准溶液 (已知:
(已知: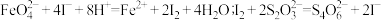 )。
)。
①滴定终点的现象为___________ 。
② 样品的纯度为
样品的纯度为___________ %(保留三位有效数字)。
 。回答下列问题:
。回答下列问题:
(1)盛浓盐酸的仪器名称为
 中铁元素的化合价为
中铁元素的化合价为(2)装置B有安全瓶作用,同时也可收集少量氯气,若关闭弹簧夹K,则B中的现象为
(3)装置A中可产生
 ,相应的离子方程式为
,相应的离子方程式为(4)装置C中制备
 的化学反应方程式为
的化学反应方程式为(5)实验室可用间接碘量法测定所得
 样品的纯度:称取
样品的纯度:称取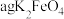 样品溶于淀粉
样品溶于淀粉 溶液中,调节
溶液中,调节 使混合液充分反应。用
使混合液充分反应。用 的
的 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗 标准溶液
标准溶液 (已知:
(已知: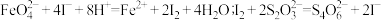 )。
)。①滴定终点的现象为
②
 样品的纯度为
样品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
|
解题方法
8 . 某化学兴趣小组在实验室配制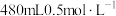 硫酸溶液。回答下列问题:
硫酸溶液。回答下列问题:
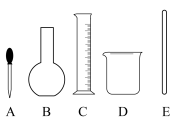
(1)在配制溶液时不需要用到的下图仪器是______ (填字母),配制上述溶液还缺少的玻璃仪器是______ (填仪器名称)。
(2)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
本实验中正确的操作顺序为______ →④(填序号,用箭头连接)。
(3)在配制过程中,以下操作会导致所配溶液浓度偏高的是______(填字母)。
(4)若定容时,加蒸馏水超过刻度线,接下来应采取的措施为______ 。
(5)用配制好的 的硫酸溶液测定
的硫酸溶液测定 溶液中
溶液中 的物质的量浓度。取
的物质的量浓度。取 该
该 溶液,逐滴滴加
溶液,逐滴滴加 的硫酸溶液,当加入硫酸的体积为
的硫酸溶液,当加入硫酸的体积为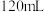 时
时 恰好完全沉淀,则该
恰好完全沉淀,则该 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为______ 。
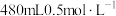 硫酸溶液。回答下列问题:
硫酸溶液。回答下列问题:(1)在配制溶液时不需要用到的下图仪器是

(2)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
本实验中正确的操作顺序为
(3)在配制过程中,以下操作会导致所配溶液浓度偏高的是______(填字母)。
| A.量取浓硫酸时,仰视刻度线 |
| B.转移前,容量瓶中含有少量蒸馏水 |
| C.转移时,有少量液体溅出 |
| D.未等溶液恢复至室温就转移到容量瓶中 |
(4)若定容时,加蒸馏水超过刻度线,接下来应采取的措施为
(5)用配制好的
 的硫酸溶液测定
的硫酸溶液测定 溶液中
溶液中 的物质的量浓度。取
的物质的量浓度。取 该
该 溶液,逐滴滴加
溶液,逐滴滴加 的硫酸溶液,当加入硫酸的体积为
的硫酸溶液,当加入硫酸的体积为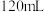 时
时 恰好完全沉淀,则该
恰好完全沉淀,则该 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
2023-12-16更新
|
33次组卷
|
2卷引用:贵州省部分中学2023-2024学年高三上学期第四次月考化学试题
名校
9 . 钠及其化合物在生产、生活中有着重要的用途,根据所学知识,回答下列问题。
Ⅰ.某汽车安全气囊的产气药剂主要含有 等物质。 当汽车发生碰撞时,NaN3迅速分解产生N2和 Na,同时放出大量的热,
等物质。 当汽车发生碰撞时,NaN3迅速分解产生N2和 Na,同时放出大量的热, 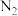 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。
(1)KClO4 可处理产生的Na,KClO4中氯元素的化合价为_______ 。
(2) 是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为
是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为_______ 。
Ⅱ.某实验小组设计如下实验方案测定 与
与 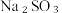 混合物中各组分的含量。
混合物中各组分的含量。
(3)方案一:称取30g样品,置于坩埚中加热至恒重,冷却、称量,剩余固体质量为31.6g,计算。
①实验中加热至恒重的目的是_______ 。
②样品中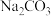 的质量分数为
的质量分数为_______ 。
(4)方案二:用如图所示装置(铁架台、铁夹等仪器未在图中画出)进行实验。

①装置C的作用是_______ ;装置F的作用是_______
②实验过程中,当装置A内的固体反应完全后,需打开活塞K,向 A 中通入大量的氮气。这样做的目的是_______ 。
(5)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量。 溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是
溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是_______ 。
Ⅰ.某汽车安全气囊的产气药剂主要含有
 等物质。 当汽车发生碰撞时,NaN3迅速分解产生N2和 Na,同时放出大量的热,
等物质。 当汽车发生碰撞时,NaN3迅速分解产生N2和 Na,同时放出大量的热, 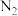 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。(1)KClO4 可处理产生的Na,KClO4中氯元素的化合价为
(2)
 是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为
是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为Ⅱ.某实验小组设计如下实验方案测定
 与
与 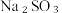 混合物中各组分的含量。
混合物中各组分的含量。(3)方案一:称取30g样品,置于坩埚中加热至恒重,冷却、称量,剩余固体质量为31.6g,计算。
①实验中加热至恒重的目的是
②样品中
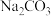 的质量分数为
的质量分数为(4)方案二:用如图所示装置(铁架台、铁夹等仪器未在图中画出)进行实验。

①装置C的作用是
②实验过程中,当装置A内的固体反应完全后,需打开活塞K,向 A 中通入大量的氮气。这样做的目的是
(5)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量。
 溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是
溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是
您最近一年使用:0次
2023-10-31更新
|
135次组卷
|
3卷引用:贵州省部分名校2023-2024学年高三上学期10月大联考化学试题
10 . A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期主族元素组成,在一定条件下有如图转化关系,请完成下列问题:

(1)若常温下A为有色气体。
①若F是一种金属单质,请写出一定浓度的B溶液和适量 F反应生成C与气体E的离子方程式:_______ 。
②若C为直线形分子,E具有漂白性,物质F的焰色试验火焰呈黄色,则C的电子式为_______ ;D中所含化学键的类型为_______ 。
(2)若A为淡黄色固体,D为白色、难溶于水的物质,且A和D的相对分子质量相等,D的化学式为_______ ,请用离子方程式表示 F的水溶液呈酸性的原因:_______ 。
(3)若A中一种元素原子的最外层电子数为内层电子总数的 F为气体单质,且F中的元素在地壳中的含量最多,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液。请写出B的一种用途:
F为气体单质,且F中的元素在地壳中的含量最多,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液。请写出B的一种用途:_______ ;B转化为C的化学方程式为_______ 。

(1)若常温下A为有色气体。
①若F是一种金属单质,请写出一定浓度的B溶液和适量 F反应生成C与气体E的离子方程式:
②若C为直线形分子,E具有漂白性,物质F的焰色试验火焰呈黄色,则C的电子式为
(2)若A为淡黄色固体,D为白色、难溶于水的物质,且A和D的相对分子质量相等,D的化学式为
(3)若A中一种元素原子的最外层电子数为内层电子总数的
 F为气体单质,且F中的元素在地壳中的含量最多,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液。请写出B的一种用途:
F为气体单质,且F中的元素在地壳中的含量最多,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液。请写出B的一种用途:
您最近一年使用:0次
2023-10-31更新
|
132次组卷
|
2卷引用:贵州省部分名校2023-2024学年高三上学期10月大联考化学试题



