解题方法
1 . 设NA为阿伏加德罗常数的值,下列有关叙述不正确的是
| A.标准状况下,11.2L的庚烷所含的分子数为0.5NA |
| B.1 mol甲基(-CH3)所含的电子总数为9NA |
| C.0.5 mol 1,3-丁二烯分子中含有碳碳双键数为NA |
| D.1 mol乙烷含共价键数目为7NA |
您最近一年使用:0次
2 . 如表是同一短周期元素W、X、Y、Z的相关信息,下列说法不正确的是
| 元素代号 | W | X | Y | Z |
| 原子半径/nm | 0.186 | 0.117 | 0.110 | 0.099 |
| 最高正(最低负)化合价 | +1 | +7、-1 | ||
| 一种新化合物 |  | |||
| A.简单离子半径:Z->W+ |
| B.Y的最高价氧化物对应的水化物是强酸 |
| C.该新化合物中含有离子键和极性共价键 |
| D.该新化合物中所有原子均满足8电子稳定结构 |
您最近一年使用:0次
解题方法
3 . 下列各组物质全部是强电解质的是
A. 、 、 、 、 | B. 、 、 、 、 |
C. 、 、 、 、 | D. 、 、 、 、 |
您最近一年使用:0次
4 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1 L   溶液中含有的 溶液中含有的 数目为 数目为 |
B.标准状况下,2.24 L  中含有的分子数为 中含有的分子数为 |
C.0.5 mol  与1.5 mol 与1.5 mol  在密闭容器中充分反应,生成的 在密闭容器中充分反应,生成的 分子数为 分子数为 |
D.常温下,1 L  的 的 溶液中含有的 溶液中含有的 数目为 数目为 |
您最近一年使用:0次
名校
5 . 工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如图:

已知:1.NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
2.高氯酸是至今为止人们已知酸中的最强酸,沸点90℃。
请回答下列问题:
(1)反应器I中发生反应的化学方程式为_______ ,冷却的目的是_______ ,能用蒸馏法分离出高氯酸的原因是_______ 。
(2)反应器Ⅱ中发生反应的离子方程式为_______ 。
(3)通入反应器Ⅱ中的SO2用另一物质H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是_______ 。
(4)Ca(ClO)2、ClO2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有_______ ,请写出工业上用氯气和NaOH溶液生产另一种消毒剂NaClO的离子方程式_______ 。

已知:1.NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
2.高氯酸是至今为止人们已知酸中的最强酸,沸点90℃。
请回答下列问题:
(1)反应器I中发生反应的化学方程式为
(2)反应器Ⅱ中发生反应的离子方程式为
(3)通入反应器Ⅱ中的SO2用另一物质H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是
(4)Ca(ClO)2、ClO2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有
您最近一年使用:0次
6 . 下列现象或事实可用同一化学原理加以说明的是
| A.氯化铵和碘都可以用加热法进行提纯 |
| B.铜和氯化钠溶液均能导电 |
| C.硫酸亚铁溶液和氢氧化钠溶液在空气中久置后均会变质 |
| D.铁片和铝片置于冷的浓硫酸中均无明显现象 |
您最近一年使用:0次
名校
7 . 下列离子反应方程式正确的是
| A.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
| B.钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
C.Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++  =BaSO4↓+H2O =BaSO4↓+H2O |
| D.FeCl3溶液刻蚀铜制的印刷电路板:Cu+Fe3+=Cu2++Fe2+ |
您最近一年使用:0次
名校
8 . 下列归类完全正确的是
| A | B | C | D | |
| 强电解质 | Fe | NaCl | CaCO3 | HNO3 |
| 弱电解质 | CH3COOH | NH3 | H2SO3 | Fe(OH)3 |
| 非电解质 | 蔗糖 | BaSO4 | 乙醇 | H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-07更新
|
526次组卷
|
2卷引用:广东实验中学附属江门学校2022-2023学年高二上学期期中考试化学试题
9 . 2021年10月16日,神舟十三号载人飞船与“天和”核心舱成功径向交会对接。化学助力我国航天事业发展,借助元素周期表可以认识各种材料的组成、结构和性质。a~h8种元素在元素周期表中的位置如下:
(1)液态a单质和液态d单质可用作火箭推进剂,二者反应的化学方程式为___________ 。常温下,与a单质更容易反应的是___________ (填“c”或“d”或“e”)单质。
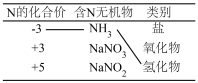
(2)空间站再生式生活保障系统能将尿液处理得到再生水,再生水后处理需除去残留的有机物和含N无机物。按示例,在答题卡相应位置补齐连线。_________
(3)我国科学家自主研发了用于航空航天的f合金材料。f原子的核外电子排布为___________ ;h最高价氧化物对应的水化物的稀溶液,与f的最高价氧化物反应的离子方程式为___________ 。
(4)g单质在太阳能电池和芯片制造等领域有着重要应用。g最高价氧化物的化学式为___________ ;b和g组成的化合物可作为新型陶瓷材料,其化学式为___________ 。上述g的两种化合物含有的化学键类型均为___________ 。
| 周期 | ⅠA | 0 | |||||||
| 1 | a | ⅡA | … | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | b | c | d | e | |||||
| 3 | f | g | h | ||||||
(2)空间站再生式生活保障系统能将尿液处理得到再生水,再生水后处理需除去残留的有机物和含N无机物。按示例,在答题卡相应位置补齐连线。

(3)我国科学家自主研发了用于航空航天的f合金材料。f原子的核外电子排布为
(4)g单质在太阳能电池和芯片制造等领域有着重要应用。g最高价氧化物的化学式为
您最近一年使用:0次
解题方法
10 . 对实验现象及其内涵的建构能发展学生的宏观辨识和微观探析素养。下列实验对应的离子方程式书写正确的是
| 选项 | 实验与现象 | 离子方程式 |
| A | 铝片插入CuSO4溶液,析出红色物质 |  |
| B | 稀H2SO4中滴加Ba(OH)2溶液,产生白色沉淀 | 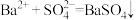 |
| C | 在大理石上滴稀盐酸,产生气泡 |  |
| D | Fe2(SO4)3溶液中滴加氨水,产生红褐色沉淀 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-02更新
|
207次组卷
|
2卷引用:2022年广东省高中学业平合格考试(新课标)化学试题



