21-22高一上·福建漳州·期中
名校
解题方法
1 . 某溶液中只含有Na+、Al3+、Cl-、 四种离子,前三种离子的个数比为3:2:1,则溶液中Al3+和
四种离子,前三种离子的个数比为3:2:1,则溶液中Al3+和 的离子个数比为
的离子个数比为
 四种离子,前三种离子的个数比为3:2:1,则溶液中Al3+和
四种离子,前三种离子的个数比为3:2:1,则溶液中Al3+和 的离子个数比为
的离子个数比为| A.1:2 | B.1:4 | C.3:4 | D.3:2 |
您最近一年使用:0次
2024-01-30更新
|
78次组卷
|
15卷引用:四川省南江中学2022-2023学年高二上学期10月诊断月考化学试题
(已下线)四川省南江中学2022-2023学年高二上学期10月诊断月考化学试题山东省新泰市第一中学2022—2023学年高一上学期期中考试化学试题天津大学附属中学2022-2023学年高一上学期期末考试化学试题四川省眉山市彭山区第一中学2023-2024学年高一上学期9月月考化学试题四川省泸县第一中学2023-2024学年高一上学期10月月考化学试题福建省漳州市正兴学校2021-2022学年高一上学期期中考试化学试题新疆维吾尔自治区喀什第二中学2021-2022学年高三上学期10月月考化学试题天津市红桥区2020-2021学年高一上学期期末考试化学试题山东省济南市天桥区黄河双语实验学校2021-2022学年高一上学期期中考试化学试题天津市新华中学2022-2023学年高一上学期期末考试化学试题云南省丽江市第一高级中学2022-2023学年高一下学期期末考试化学试题甘肃省兰州市教育局第四片区联考2023-2024学年高一上学期期中考试化学试题15-2023新东方高一上期中考化学江西省宜春市丰城市东煌学校2023-2024学年高一上学期11月期中化学试题天津北京师范大学静海附属学校2023-2024学年高一上学期第三次月考化学试题
名校
解题方法
2 . 春节期间,王亚平在太空绘制奥运五环,环中的试剂涉及X、Y、Z、W四种元素,已知X、Y、Z、W分布于前三个周期且原子序数依次增大,W在短周期主族元素中原子半径最大,X与W同一主族,Z元素的最外层电子数是电子层数的3倍,也是其它三种元素的最外层电子数之和,下列说法正确的是
| A.工业上常采用电解饱和盐溶液的方法制备单质W |
| B.氢化物的沸点:Z>Y |
| C.简单离子半径:W>Z |
| D.空间站可采用W2Z2提供用于呼吸的气体并净化空气 |
您最近一年使用:0次
名校
解题方法
3 . 高铁酸钾( )是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓KOH溶液,能溶于水,且能与水反应放出氧气,并生成
)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓KOH溶液,能溶于水,且能与水反应放出氧气,并生成 胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于
胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于 、
、 等。工业上湿法制备
等。工业上湿法制备 的流程如下:
的流程如下:
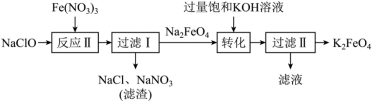
下列关于 的说法错误的是
的说法错误的是
 )是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓KOH溶液,能溶于水,且能与水反应放出氧气,并生成
)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾微溶于浓KOH溶液,能溶于水,且能与水反应放出氧气,并生成 胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于
胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下,其氧化性强于 、
、 等。工业上湿法制备
等。工业上湿法制备 的流程如下:
的流程如下:
下列关于
 的说法错误的是
的说法错误的是A.可用丁达尔效应鉴别 和 和 两种紫红色溶液 两种紫红色溶液 |
B.与水反应,每消耗1mol 转移3mol电子 转移3mol电子 |
C.将 与盐酸混合使用,可增强其杀菌消毒效果 与盐酸混合使用,可增强其杀菌消毒效果 |
| D.“反应Ⅱ”中,氧化剂和还原剂的个数之比为3∶2 |
您最近一年使用:0次
名校
4 . 高铁酸盐是优良的多功能水处理剂。K2FeO4为紫色固体,可溶于水,微溶于浓KOH溶液,难溶于有机物;在0~5℃、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2。某实验小组制备高铁酸钾(K2FeO4)。回答下列问题:
制备K2FeO4:装置如图所示,夹持、加热等装置略。

(1)仪器a的名称是___________ ,装置B中除杂质所用试剂名称是_____________ 。
(2)A中发生反应的离子方程式为_____________ (填序号)
A.MnO2+4H+ +2 Cl- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
B. MnO2+4H++4 Cl- MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
C.Mn2++ 4H++ 4 Cl- MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
D装置的作用为_____________ (填序号)。
A.吸收多余的HCl B.吸收多余的Cl2 C.防止外界二氧化碳进入 D.防倒吸
(3)C中反应为放热反应,而反应温度须控制在0~5℃,采用的控温方法为______ (选填“热水浴”或者“冰水浴”),反应中KOH必须过量的原因是主要考虑K2 FeO4的_______ 。(选填“强氧化性”,“溶解性”或者“稳定性”)
(4)选出C中总反应的离子方程式: (填序号)。C中混合物经分离提纯得到高铁酸钾。
制备K2FeO4:装置如图所示,夹持、加热等装置略。

(1)仪器a的名称是
(2)A中发生反应的离子方程式为
A.MnO2+4H+ +2 Cl-
 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O B. MnO2+4H++4 Cl-
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O C.Mn2++ 4H++ 4 Cl-
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O D装置的作用为
A.吸收多余的HCl B.吸收多余的Cl2 C.防止外界二氧化碳进入 D.防倒吸
(3)C中反应为放热反应,而反应温度须控制在0~5℃,采用的控温方法为
(4)选出C中总反应的离子方程式: (填序号)。C中混合物经分离提纯得到高铁酸钾。
A.2Cl2+2Fe3++16OH- =2 +4Cl- + 8H2O +4Cl- + 8H2O |
B.3Cl2 + Fe3+ + 8OH- = + 6Cl- + 4H2O + 6Cl- + 4H2O |
C.3Cl2+ 2Fe3+ + 16OH- = 2 + 6Cl- + 8H2O + 6Cl- + 8H2O |
| D.3Cl2+2Fe3++4K+ + 16OH- =2K2 FeO4 + 6Cl- + 8H2O |
您最近一年使用:0次
名校
解题方法
5 . 下列说法中,正确的一组是
①两种元素组成的共价化合物的分子中的化学键都是极性键
②两种不同非金属元素的原子之间形成的化学键都是极性键
③2p能级上有两个未成对电子的简单氢化物属于非极性分子
④氯化铵和五水硫酸铜都属于配合物
⑤离子化合物中一定含有离子键
⑥分子内可能没有共价键
⑦非金属单质都是非极性分子
⑧σ键和π键可以都单独存在
①两种元素组成的共价化合物的分子中的化学键都是极性键
②两种不同非金属元素的原子之间形成的化学键都是极性键
③2p能级上有两个未成对电子的简单氢化物属于非极性分子
④氯化铵和五水硫酸铜都属于配合物
⑤离子化合物中一定含有离子键
⑥分子内可能没有共价键
⑦非金属单质都是非极性分子
⑧σ键和π键可以都单独存在
| A.②⑤⑥⑦ | B.②⑤⑥ | C.①②③⑤⑥⑧ | D.②③⑤⑥⑦ |
您最近一年使用:0次
名校
6 .  、
、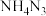 均是
均是 (叠氮酸,一元弱酸)的盐。设
(叠氮酸,一元弱酸)的盐。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 、
、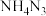 均是
均是 (叠氮酸,一元弱酸)的盐。设
(叠氮酸,一元弱酸)的盐。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.6.5g 含有的中子总数为3.6 含有的中子总数为3.6 |
B.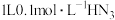 溶液中含 溶液中含 数为0.1 数为0.1 |
C.反应  中,每生成 中,每生成 ,转移的电子数为6 ,转移的电子数为6 |
D.1mol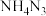 中含有的阳离子、阴离子数目均为 中含有的阳离子、阴离子数目均为 |
您最近一年使用:0次
名校
7 . 某种化合物(如右下图)由W、X、Y、Z四种前20号元素组成,分别位于四个不同周期。 的L层M层电子数相等,
的L层M层电子数相等,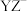 有10个电子,下列说法不正确的是
有10个电子,下列说法不正确的是
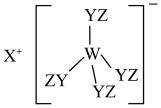
 的L层M层电子数相等,
的L层M层电子数相等,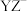 有10个电子,下列说法不正确的是
有10个电子,下列说法不正确的是
| A.原子半径:Z<Y<W<X |
| B.简单离子的氧化性:W>X |
| C.W与Y形成的化合物常用作光导纤维 |
| D.Y与X、Z均可形成多种化合物 |
您最近一年使用:0次
解题方法
8 . 某化学兴趣小组采用控制变量法探究影响硫代硫酸钠溶液与稀硫酸反应速率的因素,设计如表系列实验:
请回答下列问题:
(1)写出Na2S2O3与稀硫酸反应的离子方程式______ ;Na2S2O3长期放置在空气中易变质,需要密封保存,设计实验验证一袋密封不严的Na2S2O3固体已经变质______ 。(已知:Na2S2O3可被空气氧化,酸性条件下不稳定易分解;BaS2O3极微溶于水。)
(2)该实验①、②可探究_______ 对反应速率的影响,因此V3=______ ;实验①、③可探究______ 对反应速率的影响,因此V5=______ 。
| 实验序号 | 反应温度/℃ | Na2S2O3溶液 | H2SO4溶液 | H2O | ||
| V/mL | c(mol/L) | V/mL | c(mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(1)写出Na2S2O3与稀硫酸反应的离子方程式
(2)该实验①、②可探究
您最近一年使用:0次
解题方法
9 . 有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族:X+与M2-具有相同的电子层结构:离子半径:Z2->W-,Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
| A.元素Y、Z、W的单质晶体属于同种类型的晶体 |
| B.由于W、Z、M元素的简单氢化物相对分子质量依次减小,所以其沸点依次降低 |
| C.元素W和M的某些单质可作为水处理中的消毒剂 |
| D.X和M形成的化合物只可能有离子键 |
您最近一年使用:0次
名校
10 . 按要求填空。
(1) 的电离方程式(第一步):
的电离方程式(第一步):_______ ;
(2) 与
与 完全反应生成
完全反应生成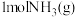 放热量46kJ,热化学方程
放热量46kJ,热化学方程_______ ;
(3)用稀硫酸酸化的KI淀粉溶液在空气中久置变蓝的离子方程式:_______ ;
(4)用 制备
制备 的反应方程式:
的反应方程式:_______ ;
(5)明矾可以净水,用离子方程式表示明矾净水的原理:_______ 。
(1)
 的电离方程式(第一步):
的电离方程式(第一步):(2)
 与
与 完全反应生成
完全反应生成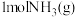 放热量46kJ,热化学方程
放热量46kJ,热化学方程(3)用稀硫酸酸化的KI淀粉溶液在空气中久置变蓝的离子方程式:
(4)用
 制备
制备 的反应方程式:
的反应方程式:(5)明矾可以净水,用离子方程式表示明矾净水的原理:
您最近一年使用:0次



