1 . 下列电离方程式中,正确的是
A.Na2SO4=2Na++ | B.Ba(OH)2=Ba2++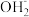 |
C.Al2(SO4)3=2Al3++3 | D.Ca(NO3)2=Ca2++2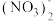 |
您最近一年使用:0次
名校
解题方法
2 . 下列物质中,其水溶液能够导电且属于非电解质的是
| A.Na | B. | C. | D. |
您最近一年使用:0次
2023-01-11更新
|
122次组卷
|
2卷引用:甘肃省庆阳市2022-2023学年高二上学期期末考试化学试题
解题方法
3 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1molP4含有P-P键的个数为4NA |
| B.1mol晶体硅中含有Si-Si键的个数为1.5NA |
| C.1molSiO2中含Si-O键的个数为2NA |
| D.含C为1mol的金刚石中含有C-C键的个数为2NA |
您最近一年使用:0次
4 . 回答下列问题
(1)在 、
、 、
、 、
、 微粒中既有氧化性又有还原性的是
微粒中既有氧化性又有还原性的是___________ 。
(2)实验室制取氯气有下列反应: 浓
浓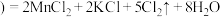
①该反应中氧化剂是___________ ;被氧化的元素是___________ 。
②用双线桥法表示: 浓
浓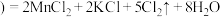
___________
(1)在
 、
、 、
、 、
、 微粒中既有氧化性又有还原性的是
微粒中既有氧化性又有还原性的是(2)实验室制取氯气有下列反应:
 浓
浓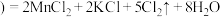
①该反应中氧化剂是
②用双线桥法表示:
 浓
浓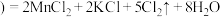
您最近一年使用:0次
解题方法
5 . 某混合物的无色溶液中,可能含有以下离子中的若干种:K+、Ca2+、Fe3+、NH 、Cl-、CO
、Cl-、CO 和SO
和SO 。现每次取10.00mL进行实验:
。现每次取10.00mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO )=
)=___________ mol·L−1;
(2)某同学认为该溶液中一定存在K+,浓度是___________ ;
(3)根据以上实验,氯离子可能存在。检验该离子是否存在的方法是:___________ ;
(4)写出③中固体加入足量盐酸洗涤的离子方程式为___________ 。
 、Cl-、CO
、Cl-、CO 和SO
和SO 。现每次取10.00mL进行实验:
。现每次取10.00mL进行实验:①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO
 )=
)=(2)某同学认为该溶液中一定存在K+,浓度是
(3)根据以上实验,氯离子可能存在。检验该离子是否存在的方法是:
(4)写出③中固体加入足量盐酸洗涤的离子方程式为
您最近一年使用:0次
6 . 现有14.4gCO和CO2的混合气体,在标准状况下所占的体积约为8.96L。回答下列问题:
(1)该混合气体的平均摩尔质量:___________ 。
(2)混合气体中碳原子的个数:___________ 。(用NA表示阿伏加德罗常数的值)
(3)将混合气体依次通过如图装置,最后收集在气球中。
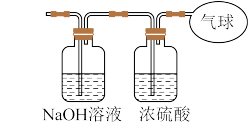
①气球中收集到的气体摩尔质量:___________ ;
②标准状况下气球中收集到的气体的体积为___________ ;
③气球中收集到的气体的电子总数___________ 。(用NA表示阿伏加德罗常数的值)
(1)该混合气体的平均摩尔质量:
(2)混合气体中碳原子的个数:
(3)将混合气体依次通过如图装置,最后收集在气球中。

①气球中收集到的气体摩尔质量:
②标准状况下气球中收集到的气体的体积为
③气球中收集到的气体的电子总数
您最近一年使用:0次
7 . 根据氧化还原反应及其规律,下列判断正确的是
A. ,反应中氧化产物和还原产物质量比为1:1 ,反应中氧化产物和还原产物质量比为1:1 |
B.根据反应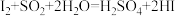 ,说明还原性: ,说明还原性: |
C.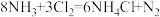 中,氧化剂和还原剂物质的量之比为3:8 中,氧化剂和还原剂物质的量之比为3:8 |
D.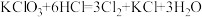 ,每生成 ,每生成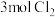 ,转移电子6mol ,转移电子6mol |
您最近一年使用:0次
解题方法
8 . 某无色溶液可能大量存在Na+、Mg2+、Al3+、Cu2+、Ag+、Cl-、OH-、C 、N
、N 中的几种离子,现进行如下实验:①取少量溶液于试管,向其中加入过量稀盐酸,有白色沉淀生成,再加入稀硝酸,沉淀不消失;②过滤,向滤液中加入过量NaOH溶液,又出现白色沉淀。下列有关说法正确的是
中的几种离子,现进行如下实验:①取少量溶液于试管,向其中加入过量稀盐酸,有白色沉淀生成,再加入稀硝酸,沉淀不消失;②过滤,向滤液中加入过量NaOH溶液,又出现白色沉淀。下列有关说法正确的是
 、N
、N 中的几种离子,现进行如下实验:①取少量溶液于试管,向其中加入过量稀盐酸,有白色沉淀生成,再加入稀硝酸,沉淀不消失;②过滤,向滤液中加入过量NaOH溶液,又出现白色沉淀。下列有关说法正确的是
中的几种离子,现进行如下实验:①取少量溶液于试管,向其中加入过量稀盐酸,有白色沉淀生成,再加入稀硝酸,沉淀不消失;②过滤,向滤液中加入过量NaOH溶液,又出现白色沉淀。下列有关说法正确的是| A.②中白色沉淀是Mg(OH)2或Al(OH)3 |
B.无色溶液中一定不存在Na+、Cu2+、Cl-、OH-和C |
C.无色溶液中一定存在Ag+、Mg2+和N |
| D.该实验无法确定Na+、Al3+和OH-是否大量存在 |
您最近一年使用:0次
2022-10-22更新
|
111次组卷
|
2卷引用:甘肃省武威第十八中学2021-2022学年高二下学期期末考试化学试卷
名校
解题方法
9 . 将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是
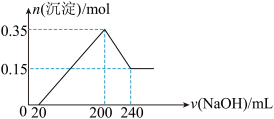

| A.Mg和Al的总质量为8g |
| B.硫酸的物质的量浓度为5mol·L-1 |
| C.NaOH溶液的物质的量浓度为5mol·L-1 |
| D.生成的H2在标准状况下的体积为11.2L |
您最近一年使用:0次
2022-10-22更新
|
231次组卷
|
7卷引用:甘肃省武威第十八中学2021-2022学年高二下学期期末考试化学试卷
10 . 填空。
(1)FeCl3的水溶液呈_______ (填“酸性”、“中性”、“碱性”),原因是(用离子方程式表示):_______ ;实验室在配制FeCl3溶液时,常将FeCl3固体先溶于盐酸中,再用蒸馏水稀释,以_______ 其水解。将FeCl3溶液加热蒸干并灼烧,最后得到的固体物质是_______ 。
(2)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的________ 。
(3)请用适当的离子方程式解释下列现象:
①NaHSO3溶液呈酸性_______ ;
②NaAlO2溶液呈碱性_______ ;
③明矾可用于净水:_______ ;
④泡沫灭火器里盛有Al2(SO4)3溶液和NaHCO3溶液,当倒置灭火器时,两种溶液混合立即喷出大量泡沫_______ 。
(1)FeCl3的水溶液呈
(2)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的
(3)请用适当的离子方程式解释下列现象:
①NaHSO3溶液呈酸性
②NaAlO2溶液呈碱性
③明矾可用于净水:
④泡沫灭火器里盛有Al2(SO4)3溶液和NaHCO3溶液,当倒置灭火器时,两种溶液混合立即喷出大量泡沫
您最近一年使用:0次



