名校
1 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.25℃, 下, 下,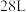 氢气中质子的数目为2.5NA 氢气中质子的数目为2.5NA |
B. 溶液中, 溶液中, 的数目为2.0NA 的数目为2.0NA |
C. 甲苯完全燃烧,生成 甲苯完全燃烧,生成 的数目为1.4NA 的数目为1.4NA |
D.电解熔融 ,阴极增重 ,阴极增重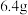 ,外电路中通过电子的数目为0.1NA ,外电路中通过电子的数目为0.1NA |
您最近一年使用:0次
2 . 设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,11.2L CH2Cl2含有的氢原子数是NA |
| B.1molSO2与足量的O2反应,转移的电子数为2NA |
C.1mol CH 中含有电子数为8 NA 中含有电子数为8 NA |
| D.0.5mol/LBa(OH)2溶液中含有的OH-的数目为NA |
您最近一年使用:0次
3 . 某学习小组拟研究FeSO4的分解实验探究,请你利用所学知识帮该小组完成以下实验方案。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2;假设2:FeO、SO3、SO2;假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
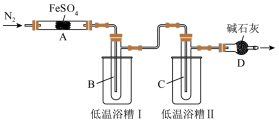
回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是_______ 。
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是_______ ,(只填操作),当A处固体完全分解后通入N2的目的是_______ 。
(3)低温浴槽I收集的物质是_______ (填化学式),低温浴槽II控制的温度范围为_______ 。
(4)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
甲组实验中A装置得到固体产物是_______ (填化学式)。
(5)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是_______ 。
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(6)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案_______ (填“1”或“2”)可行。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2;假设2:FeO、SO3、SO2;假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
| 物质 | SO3 | SO2 | O2 | N2 |
| 熔点/℃ | 16.8 | -72.4 | -218.4 | -209.9 |
| 沸点/℃ | 44.8 | -10 | -182.9 | -195.8 |

回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是
(3)低温浴槽I收集的物质是
(4)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
| 实验 | A处温度/℃ | FeSO4质量/g | 低温浴槽I净增质量/g | 低温浴槽II净增质量/g |
| 甲 | T1 | 3.04 | 0.80 | 0.64 |
| 乙 | T2 | 4.56 | 1.60 | 0.64 |
(5)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(6)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案
您最近一年使用:0次
名校
4 . 硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠NaBO2为主要原料制备NaBH4,其流程如图:

已知:NaBH4常温下能与水反应,可溶于异丙酸(沸点:13℃)
(1)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是___ 。
(2)请配平第①步反应的化学方程式:_______ 。
_____NaBO2+______SiO2+______Na+_____H2=_______NaBH4+_______Na2SiO3
(3)第②步分离采用的方法是____ ;第③步分离NaBH4并回收溶剂,采用的方法是_____ 。
(4)NaBH4与水反应生成NaBO2和一种单质气体,该反应的化学方程式是_______ ,消耗3.8克NaBH4时转移的电子数为_______ 。

已知:NaBH4常温下能与水反应,可溶于异丙酸(沸点:13℃)
(1)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是
(2)请配平第①步反应的化学方程式:
_____NaBO2+______SiO2+______Na+_____H2=_______NaBH4+_______Na2SiO3
(3)第②步分离采用的方法是
(4)NaBH4与水反应生成NaBO2和一种单质气体,该反应的化学方程式是
您最近一年使用:0次
2022-08-08更新
|
143次组卷
|
3卷引用:江西省丰城市第九中学2021-2022学年高二下学期期末检测化学试题
5 . 氯酸钾和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯(ClO2),ClO2是一种优良消毒剂。
(1)请补充空白并配平化学方程式_______ 。
_____KClO3+_____HCl(浓)→______KCl+_____ClO2↑+_____Cl2↑+_______
(2)若反应中生成标准状况下13.44L气体,则消耗还原剂的物质的量为_______ 。
(3)过氧化钙也是一种优良消毒剂,供氧剂。通常情况下用CaCl2在稀氨水条件下与H2O2反应得到CaO2·8H2O沉淀,请写出该反应的化学方程式_______ 。取2.76gCaO2·8H2O样品受热脱水过程的热重曲线(140℃时完全脱水,杂质受热不分解)如图所示。

①试确定60℃时CaO2·xH2O中x=_______ 。
②该样品中CaO2的质量分数为_______ (精确到0.1%)。
(1)请补充空白并配平化学方程式
_____KClO3+_____HCl(浓)→______KCl+_____ClO2↑+_____Cl2↑+_______
(2)若反应中生成标准状况下13.44L气体,则消耗还原剂的物质的量为
(3)过氧化钙也是一种优良消毒剂,供氧剂。通常情况下用CaCl2在稀氨水条件下与H2O2反应得到CaO2·8H2O沉淀,请写出该反应的化学方程式

①试确定60℃时CaO2·xH2O中x=
②该样品中CaO2的质量分数为
您最近一年使用:0次
6 . 填空
(1)从1L 溶液中取出100mL,向其中加入200mL
溶液中取出100mL,向其中加入200mL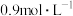 的
的 溶液恰好使
溶液恰好使 完全沉淀,则原溶液中
完全沉淀,则原溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是_______ 。
(3)标况下,1体积水中溶解了V体积HCl气体,所得溶液的密度为 ,所得溶液的物质的量浓度为
,所得溶液的物质的量浓度为_______ 。
(1)从1L
 溶液中取出100mL,向其中加入200mL
溶液中取出100mL,向其中加入200mL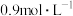 的
的 溶液恰好使
溶液恰好使 完全沉淀,则原溶液中
完全沉淀,则原溶液中 的物质的量浓度为
的物质的量浓度为(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是
(3)标况下,1体积水中溶解了V体积HCl气体,所得溶液的密度为
 ,所得溶液的物质的量浓度为
,所得溶液的物质的量浓度为
您最近一年使用:0次
7 . 一种用于合成治疗免疫疾病药物的物质,其结构如图所示,其中X、Y、Z、Q、W为1~20号元素且原子序数依次增大,Z与Q同主族,Q和W的简单离子具有相同的电子层结构。下列叙述正确的是


| A.该物质中所有原子都满足最外层8e-结构 | B.最高价氧化物对应的水化物的酸性:Q<Y |
| C.原子半径:W>Z>Y | D.Z和X、Y、W、Q均形成至少两种二元化合物 |
您最近一年使用:0次
名校
解题方法
8 . Cl2、SO2均能使品红溶液褪色。后者因为品红分子结构中的发色团遇到亚硫酸后结构发生改变,生成不稳定的无色化合物,其漂白原理可用下面的反应方程式表示:
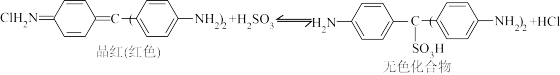
| A.品红溶液中同时通入Cl2、SO2漂白效果会更好 |
| B.加热不能判断品红褪色是通入SO2还是通入Cl2引起的 |
| C.“无色化合物”分子中,19个碳原子都可能在同一平面上 |
| D.SO2不能使品红乙醇溶液褪色 |
您最近一年使用:0次
2022-07-12更新
|
92次组卷
|
2卷引用:江西省抚州市2021-2022学年高二下学期期末考化学试题
9 . 化学和生活、生产密切相关。下列说法错误的是
| A.“碳中和”是指一定时期内,二氧化碳排放量与吸收量相平衡的状态,植树造林捕获和储存大气中的CO2的过程中涉及了氧化还原反应 |
| B.冬奥会火炬名称为“飞扬”,其外壳含碳纤维,碳纤维为新型无机非金属材料 |
| C.石墨晶体中存在范德华力,常用作润滑剂 |
| D.75%的医用酒精和84消毒液均可将新冠病毒氧化而达到消毒的目的 |
您最近一年使用:0次
10 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.在一定条件下,1 mol  和0.5 mol 和0.5 mol  充分反应后,容器中的分子总数小于 充分反应后,容器中的分子总数小于 |
B.已知反应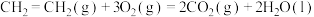 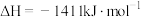 ,当反应中放出的热量为2822 kJ时,形成C=O键的数目为8 ,当反应中放出的热量为2822 kJ时,形成C=O键的数目为8 |
C.标准状况下,1.12 L 戊烷(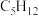 )中所含有的氢原子数为0.6 )中所含有的氢原子数为0.6 |
D.28 g  和 和 的混合物中,所含氢原子总数为6 的混合物中,所含氢原子总数为6 |
您最近一年使用:0次



