解题方法
1 . 某小组想通过实验探究 三种金属元素性质的递变规律。
三种金属元素性质的递变规律。
1.下表是元素周期表的一部分,将 三种元素填入相应位置
三种元素填入相应位置_______ 。
I.探究 分别与水反应的情况。
分别与水反应的情况。
实验①切一小块绿豆大小的金属 ,用滤纸吸干其表面的煤油,将其投入盛有
,用滤纸吸干其表面的煤油,将其投入盛有 水(含酚酞)的烧杯中。观察到
水(含酚酞)的烧杯中。观察到 与冷水发生剧烈反应,烧杯内溶液变红。
与冷水发生剧烈反应,烧杯内溶液变红。
2. 与
与 反应生成
反应生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ 。该反应中作还原剂的是_______ 。
A. B.
B. C.
C.
3. 溶液中使酚酞试液变红的微粒是
溶液中使酚酞试液变红的微粒是_______ 。
A. B.
B. C.
C.
实验②分别取一小段镁条和铝条,放入两支试管中,向试管中各加入 水,再滴入2滴酚酞试液,观察到试管中均无明显现象。
水,再滴入2滴酚酞试液,观察到试管中均无明显现象。
有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后 与水反应现象仍不明显。
与水反应现象仍不明显。
4.实验②的设计中未考虑到的因素是_______ 。
5.通过上述实验,得出 的金属性由强到弱顺序
的金属性由强到弱顺序_______ 。
A. B.
B.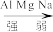
6.除反应物自身性质外,上述实验还验证了化学反应速率与_______ 有关。
Ⅱ.比较 碱性的强弱。
碱性的强弱。
实验④在试管中加入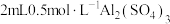 溶液,然后逐滴滴加
溶液,然后逐滴滴加 溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
实验⑤在试管中加入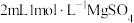 溶液,然后逐滴滴加
溶液,然后逐滴滴加 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
7.写出由实验④、⑤的实验现象可推导得出的结论。
8.综上实验可知, 的碱性由强到弱顺序:
的碱性由强到弱顺序:_______ 。
A.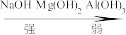 B.
B.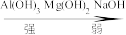
 三种金属元素性质的递变规律。
三种金属元素性质的递变规律。1.下表是元素周期表的一部分,将
 三种元素填入相应位置
三种元素填入相应位置H | |||
C | |||
I.探究
 分别与水反应的情况。
分别与水反应的情况。实验①切一小块绿豆大小的金属
 ,用滤纸吸干其表面的煤油,将其投入盛有
,用滤纸吸干其表面的煤油,将其投入盛有 水(含酚酞)的烧杯中。观察到
水(含酚酞)的烧杯中。观察到 与冷水发生剧烈反应,烧杯内溶液变红。
与冷水发生剧烈反应,烧杯内溶液变红。2.
 与
与 反应生成
反应生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式A.
 B.
B. C.
C.
3.
 溶液中使酚酞试液变红的微粒是
溶液中使酚酞试液变红的微粒是A.
 B.
B. C.
C.
实验②分别取一小段镁条和铝条,放入两支试管中,向试管中各加入
 水,再滴入2滴酚酞试液,观察到试管中均无明显现象。
水,再滴入2滴酚酞试液,观察到试管中均无明显现象。有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后
 与水反应现象仍不明显。
与水反应现象仍不明显。4.实验②的设计中未考虑到的因素是
5.通过上述实验,得出
 的金属性由强到弱顺序
的金属性由强到弱顺序A.
 B.
B.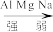
6.除反应物自身性质外,上述实验还验证了化学反应速率与
Ⅱ.比较
 碱性的强弱。
碱性的强弱。实验④在试管中加入
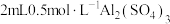 溶液,然后逐滴滴加
溶液,然后逐滴滴加 溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。实验⑤在试管中加入
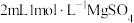 溶液,然后逐滴滴加
溶液,然后逐滴滴加 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。7.写出由实验④、⑤的实验现象可推导得出的结论。
实验序号 | 现象 | 结论 |
④ | 出现白色沉淀 |
|
沉淀全部溶解 | ||
⑤ | 出现白色沉淀 | |
沉淀不溶解 |
|
 的碱性由强到弱顺序:
的碱性由强到弱顺序:A.
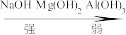 B.
B.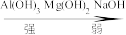
您最近一年使用:0次
2 . (1) 由液态转变为气态的过程中
由液态转变为气态的过程中_______ ;
A.放出热量 B.吸收热量 C.发生化学变化
(2)上述转变过程中,微粒间的距离_______ 。
A.变大 B.变小 C.不变
 由液态转变为气态的过程中
由液态转变为气态的过程中A.放出热量 B.吸收热量 C.发生化学变化
(2)上述转变过程中,微粒间的距离
A.变大 B.变小 C.不变
您最近一年使用:0次
3 . C和 是同主族元素,下列事实能说明两者非金属性相对强弱的是
是同主族元素,下列事实能说明两者非金属性相对强弱的是_______ 。
A.沸点: B.相对原子质量:
B.相对原子质量: C.酸性:
C.酸性: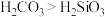
 是同主族元素,下列事实能说明两者非金属性相对强弱的是
是同主族元素,下列事实能说明两者非金属性相对强弱的是A.沸点:
 B.相对原子质量:
B.相对原子质量: C.酸性:
C.酸性: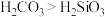
您最近一年使用:0次
解题方法
4 .  分子中化学键类型为
分子中化学键类型为_______ ; 分子的空间填充模型为
分子的空间填充模型为_______ 。
 分子中化学键类型为
分子中化学键类型为 分子的空间填充模型为
分子的空间填充模型为A. B.
B.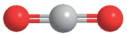
您最近一年使用:0次
解题方法
5 . 碳元素有三种核素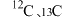 和
和 。
。 中的“14”是指
中的“14”是指_______ 。
A. 的中子数 B.
的中子数 B. 的质量数 C.碳元素的相对原子质量
的质量数 C.碳元素的相对原子质量
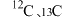 和
和 。
。 中的“14”是指
中的“14”是指A.
 的中子数 B.
的中子数 B. 的质量数 C.碳元素的相对原子质量
的质量数 C.碳元素的相对原子质量
您最近一年使用:0次
名校
6 . 数字化实验是化学研究的重要手段。实验小组将电导率传感器插入20.00mL 0.1mol·L-1 H2SO4溶液中,向溶液中匀速滴入等浓度的BaCl2溶液,电导率与溶液体积图像如图所示。 (已知溶液导电性越强,电导率值越大),请回答下列问题。
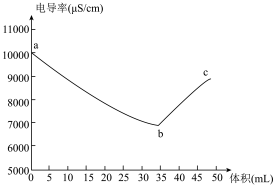
(1)按物质分类,BaCl2属于_______ (选填“强电解质”或“弱电解质”)。
(2)其它条件相同的情况下,溶的导电性由_______ 决定。
(3)用离子方程式解释图中 a→b段曲线变化的原因_______ 。
(4)对 b、c 两处溶液的c(H+)进行比较,b_______ c(选填“>”或“=”或“<”), 说明原因_______ 。
(5)用等浓度的Ba(OH)2溶液替换BaCl2溶液,则电导率最低点与图中 b 点的位置关系为
(6)向 0.1 mol·L-1氨水中,匀速滴入等浓度的醋酸溶液,下列图像正确的是
(7)在无色溶液中能大量共存的一组离子是
(8)下列物质的溶液不能将Al(OH)3溶解的是

(1)按物质分类,BaCl2属于
(2)其它条件相同的情况下,溶的导电性由
(3)用离子方程式解释图中 a→b段曲线变化的原因
(4)对 b、c 两处溶液的c(H+)进行比较,b
(5)用等浓度的Ba(OH)2溶液替换BaCl2溶液,则电导率最低点与图中 b 点的位置关系为
| A.在 b 上方 | B.与 b 重合 | C.在 b 下方 | D.无法确定 |
A.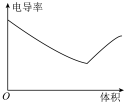 | B.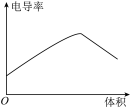 |
C.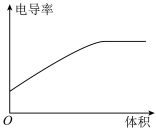 | D.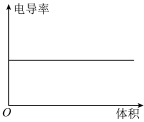 |
A.NO 、Cl-、Na+、Ca2+ 、Cl-、Na+、Ca2+ | B.Ag+、NO 、OH-、Na+ 、OH-、Na+ |
C.Mg2+、MnO 、K+、I- 、K+、I- | D.HCO 、OH-、Ca2+、Na+ 、OH-、Ca2+、Na+ |
| A.NaOH | B.NaCl | C.H2SO4 | D.HCl |
您最近一年使用:0次
名校
7 . 如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题。
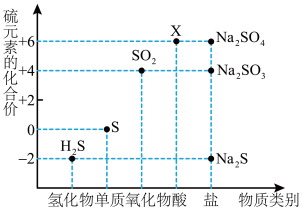
(1)X 的浓溶液与碳在一定条件下可以发生反应,体现了 X 的_______ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有_______ (填化学式)。
(3)将 H2S 与 SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为_______ 。
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目______ 。
Na2S+_______Na2SO3+_______H2SO4=_______Na2SO4+_______S↓+_______H2O
(5)下列关于硫及其化合物的叙述正确的是
(6)设 NA为阿伏加德罗常数的值。下列说法正确的是
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:
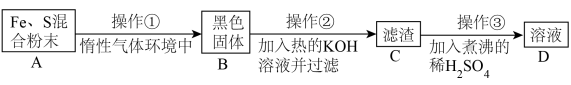
请回答以下问题:
(7)操作②的作用是_______ ,也可改用_______ 。
(8)混合粉末 A 中硫粉过量的原因是_______ 。
(9)下列溶液中通入SO2一定不会产生沉淀的是
(10)区别浓H2SO4和稀H2SO4,既简单又可靠的方法是

(1)X 的浓溶液与碳在一定条件下可以发生反应,体现了 X 的
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将 H2S 与 SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目
Na2S+_______Na2SO3+_______H2SO4=_______Na2SO4+_______S↓+_______H2O
(5)下列关于硫及其化合物的叙述正确的是
| A.试管内壁残留的硫可用酒精洗涤 | B.SO2的水溶液长期放置,酸性会增强 |
| C.SO2有毒,不可以做食品添加剂 | D.浓硫酸在空气中敞口放置,质量会减小 |
| A.1mol 铁单质与足量的硫单质充分反应,转移电子的数目为3NA |
| B.常温下,22.4LSO2与足量的O2反应,生成的SO3分子数为NA |
| C.常温下,将5.6g铁片投入足量的浓硫酸中,铁失去的电子数为0.3NA |
| D.1 molNa2O2与足量H2O反应,转移的电子数为NA |
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:

请回答以下问题:
(7)操作②的作用是
(8)混合粉末 A 中硫粉过量的原因是
(9)下列溶液中通入SO2一定不会产生沉淀的是
| A.Ba(OH)2 | B.澄清石灰水 | C.Na2S | D.BaCl2 |
| A.各取少许溶液分别放入铜片 | B.分别与石蕊试液作用 |
| C.用玻璃棒各蘸少许液涂在纸上 | D.观察溶液的颜色 |
您最近一年使用:0次
名校
8 . 元素周期表是研究化学的重要工具。下表为元素周期表的一部分,请根据元素①~⑧所处的位置回答下列问题。

(1)元素④⑤⑧的离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)元素⑦的原子结构示意图为_______ ;元素④⑦的最简单氢化物的稳定性关系为_______ (用化学式表示)。
(3)由元素④⑤组成原子个数比为1:1的化合物中含_______ (填“离子键”、“共价键” 或“离子键和共价键”);将78g该化合物投入98g水中,所得溶液的质量分数为_______ 。
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是_______ (填化学式);该酸与元素⑥的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(5)由元素①③组成的含10e-和18e-的分子的电子式分别是_______ 、_______ 。
(6)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是
(7)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是
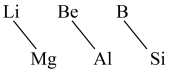

(1)元素④⑤⑧的离子半径由大到小的顺序为
(2)元素⑦的原子结构示意图为
(3)由元素④⑤组成原子个数比为1:1的化合物中含
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是
(5)由元素①③组成的含10e-和18e-的分子的电子式分别是
(6)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是
| A.在周期表中金属与非金属的分界处可以找到催化剂材料 |
| B.对氟、氯、硫、磷、砷等元素的研究,有助于制造出新品种的农药 |
| C.在过渡元素中可寻找制造半导体的元素 |
| D.可在第ⅠA、ⅡA族元素中寻找制造耐高温、耐腐蚀合金的元素 |

| A.Li在空气中燃烧生成Li2O、Li3N | B.硼酸是弱酸 |
| C.BeCl2是离子化合物 | D.Be(OH)2是两性氢氧化物 |
您最近一年使用:0次

 的碱性比
的碱性比 无酸性
无酸性

