解题方法
1 . 电子工业常用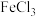 溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含
溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含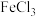 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得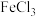 溶液,处理流程如下:
溶液,处理流程如下:
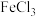 溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含
溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含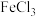 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得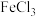 溶液,处理流程如下:
溶液,处理流程如下: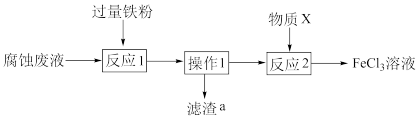
A. 溶液腐蚀铜箔的原理为 溶液腐蚀铜箔的原理为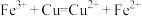 |
| B.反应1和反应2都发生了氧化还原反应 |
| C.实验室中进行操作1时,用到的主要玻璃仪器有漏斗、烧杯和玻璃棒 |
| D.滤渣a的主要成分是Cu和Fe,物质X可以选用氯气 |
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式书写正确的是
A.铁与稀盐酸反应: |
B.氯气与氯化亚铁溶液反应: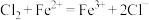 |
C.过量二氧化硫溶于氢氧化钠溶液: |
D.氯化铁溶液与硫化氢反应: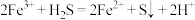 |
您最近一年使用:0次
3 . 室温下,下列各组离子在指定溶液中能大量共存的是
A.在新制饱和氯水中: 、 、 、 、 、 、 |
B.使酚酞变红色的溶液: 、 、 、 、 、 、 |
C.使紫色石蕊试液变红色的溶液: 、 、 、 、 、 、 |
D.在 小于7的溶液: 小于7的溶液: 、 、 |
您最近一年使用:0次
解题方法
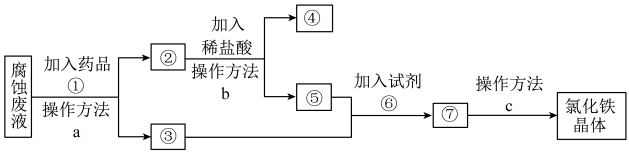
4 . 一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如下。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)__________________ 。
(2)④所代表的物质是______ (用化学式表示)。
(3)操作方法a、b、c中是过滤的是______ (填序号)。
(4)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,______ (补全实验现象),此过程涉及氧化还原反应的化学方程式是_________________ 。
(5)试剂⑥是 时,发生反应的化学方程式是
时,发生反应的化学方程式是__________________ 。
(2)④所代表的物质是
(3)操作方法a、b、c中是过滤的是
(4)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(5)试剂⑥是
 时,发生反应的化学方程式是
时,发生反应的化学方程式是
您最近一年使用:0次
解题方法
5 . 部分含铁微粒所带的电荷数与其中铁元素化合价的关系如图所示。下列推断不合理的是

| A.含R的合金是用量最大、用途最广的合金 |
B.高温条件下,红热的 与水蒸气反应生成 与水蒸气反应生成 |
C.可用 溶液检验溶液中 溶液检验溶液中 是否被氧化 是否被氧化 |
D.根据 中铁元素的价态,可判断 中铁元素的价态,可判断 具有氧化性 具有氧化性 |
您最近一年使用:0次
名校
6 . 能正确表示下列反应的离子方程式的是
| A.氯化铁溶液腐蚀铜箔:Fe3++Cu=Fe2++Cu2+ |
| B.向FeBr2溶液中通入过量Cl2:2Fe2++Cl2=2Fe3++2Cl﹣ |
C.向Na2CO3溶液中滴入少量盐酸:CO +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| D.用“胃舒平”治疗胃酸过多:Al(OH)3+3H+=Al3++3H2O |
您最近一年使用:0次
7 . 已知A、B、C均为含铁化合物,请根据以下四种物质的转化过程回答相关问题:
Fe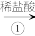 A
A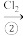 B
B C
C
(1)反应①、②、③中属于氧化还原反应的是 。
(2)关于B的溶液,说法正确的是 。
(3)选择合适的试剂也可以实现B转化为A,且考虑不能引入杂质,能实现该转化的方程式 。
Fe
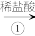 A
A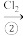 B
B C
C(1)反应①、②、③中属于氧化还原反应的是 。
| A.①② | B.①③ | C.②③ | D.①②③ |
| A.滴入几滴KSCN溶液后,可观察到溶液变血红色 |
| B.可与Fe反应,不能与Cu反应 |
| C.若加入NaOH溶液有红褐色沉淀生成 |
| D.Cl2 是氧化剂,可用双氧水替换 |
| A.2FeCl3+Fe=3FeCl2 | B.2FeCl3+Zn=2FeCl2+ZnCl2 |
| C.4Fe(OH)2+2H2O+O2=4Fe(OH)3 | D.2KI+2FeCl3=2KCl+2FeCl2+I2 |
您最近一年使用:0次
名校
8 . 下列实验方案不可行的是
| A.用碱石灰干燥氨气 | B.用蓝色石蕊试液检验酸性溶液 |
| C.通入Cl2除去FeCl3溶液中的FeCl2 | D.加入Fe粉除去Al3+溶液中的杂质Cu2+ |
您最近一年使用:0次
名校
9 . 下列物质的应用中,利用了氧化还原反应原理的是
A. 补血剂与维生素C配合使用效果 补血剂与维生素C配合使用效果 |
| B.二氧化碳灭火 |
| C.小苏打中和胃酸 |
| D.稀硫酸除铁锈更佳 |
您最近一年使用:0次
解题方法
10 . 工业上用FeCl3溶液做印刷电路铜板的腐蚀液。化学小组设计如下流程对腐蚀废液(阳离子主要有H+、Fe3+、Fe2+和Cu2+)进行处理,实现FeCl3溶液再生并回收Cu。
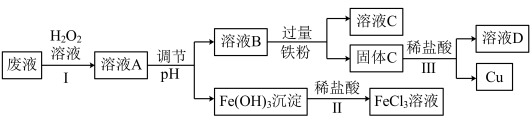
(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:_____________ ;
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为__________ ;
(3)步骤Ⅱ中发生反应的化学方程式为_____________ ;
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?_____________ ;
(5)固体C中的成分为________________ (填化学式);
(6)步骤Ⅲ中发生反应的离子方程式为___________ ,分离的操作名称为_______ 。

(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为
(3)步骤Ⅱ中发生反应的化学方程式为
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?
(5)固体C中的成分为
(6)步骤Ⅲ中发生反应的离子方程式为
您最近一年使用:0次



