名校
解题方法
1 . 已知还原性: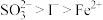 。某无色溶液中只可能含有
。某无色溶液中只可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的部分离子,取该溶液进行下列实验:
中的部分离子,取该溶液进行下列实验:
通过实验得出的结论正确的是
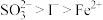 。某无色溶液中只可能含有
。某无色溶液中只可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的部分离子,取该溶液进行下列实验:
中的部分离子,取该溶液进行下列实验:| 实验编号 | 操作 | 现象 |
| ① | 取 溶液,先加入稍过量的氯水,后加入苯并充分振荡、静置 溶液,先加入稍过量的氯水,后加入苯并充分振荡、静置 | 生成无色气体、上层为紫色 |
| ② | 向实验①的水溶液中加入足量 和 和 溶液 溶液 | 可得到白色沉淀 |
| ③ | 取 原溶液,加入过量的 原溶液,加入过量的 溶液并加热 溶液并加热 | 产生 气体(标准状况) 气体(标准状况) |
A.实验①中若通入过量的 ,则可能先后氧化了 ,则可能先后氧化了 、 、 |
B.上述3个实验不能确定是否一定含有 ,判断方法:在溶液中加硝酸银,再加硝酸,若有沉淀生成,则证明有 ,判断方法:在溶液中加硝酸银,再加硝酸,若有沉淀生成,则证明有 |
| C.判断溶液中是否含有钾离子,需要通过焰色反应来检验 |
D.实验②能够确定溶液中不含有 |
您最近一年使用:0次
2021-09-10更新
|
485次组卷
|
4卷引用:第二单元 化学物质及其变化(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)
(已下线)第二单元 化学物质及其变化(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)山西省运城市2022届高三上学期入学摸底测试化学试题天津市滨海新区塘沽第一中学2022届高三第一次月考化学试卷江西省新余市第一中学2021-2022学年高三上学期第二次模拟考试化学试题
名校
解题方法
2 . 下列方案设计、现象和结论有正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 鉴定 与溴蒸气 与溴蒸气 | 两气体分别通入淀粉KI溶液中 | 变蓝色的是通入溴蒸气 |
| B | 检验固体混合物是否存在铵盐 | 将固体溶于水,加入足量浓NaOH溶液,加热,用红色湿润石蕊试纸检验产生的气体 | 若试纸不变蓝,说明固体中不存在铵盐 |
| C | 检验 的氧化性 的氧化性 | 在 溶液中加入 溶液中加入 溶液 溶液 | 若溶液出现淡黄色沉淀,则说明 具有氧化性 具有氧化性 |
| D | 检验火柴头中的氯元素 | 取用火柴头浸泡过的溶液,加 溶液、稀硝酸和 溶液、稀硝酸和 溶液 溶液 | 若出现白色沉淀,说明有氯元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-21更新
|
537次组卷
|
4卷引用:第28讲 物质的分离、提纯和检验(练)-2023年高考化学一轮复习讲练测(全国通用)
(已下线)第28讲 物质的分离、提纯和检验(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题05 突破化学实验基础(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)天津市第二十一中学2023-2024学年高三上学期期中质量检测化学试题浙江省精诚联盟2022届高三下学期适应性考试化学试题
3 . 含SO2的工业烟气脱硫往往使用较为廉价的碱性物质如生石灰、浓氨水等吸收。近年来一些近海的煤电厂,利用海水的微碱性(8.0≤pH≤8.3)开发海水脱硫新工艺。主要原理是:SO2与海水生成H2SO3,H2SO3电离得到HSO 和SO
和SO 进一步氧化得到SO
进一步氧化得到SO 。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO
。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO 和CO
和CO )发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。在指定条件下,下列选项所示的物质间转化能实现的是
)发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。在指定条件下,下列选项所示的物质间转化能实现的是
 和SO
和SO 进一步氧化得到SO
进一步氧化得到SO 。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO
。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO 和CO
和CO )发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。在指定条件下,下列选项所示的物质间转化能实现的是
)发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。在指定条件下,下列选项所示的物质间转化能实现的是A.FeS2(s) 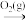 SO3(g) SO3(g) |
B.HSO (aq) (aq) 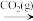 SO2 (g) SO2 (g) |
C.SO2(g)  CaSO3(s) CaSO3(s) |
D.SO2(g) NH4HSO4(aq) NH4HSO4(aq) |
您最近一年使用:0次
名校
4 . 某研究小组同学为探究锌与硫酸反应生成 SO2、H2的临界浓度(浓硫酸能与锌反应生成 SO2的最低浓度)设计了如图实验 (加热和夹持装置已省略)。
已知:锌与浓硫酸开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。
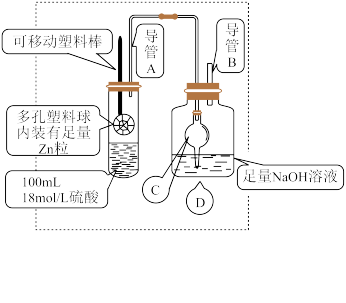
(1)请写出锌与硫酸反应产生 SO2的化学方程式_______ 。
(2)在组装仪器之后,加入试剂之前必须进行的操作是_______ 。
(3)装置中干燥管C的作用是_______ 。
(4)移动塑料棒,使锌浸没到硫酸中充分反应,反应结束后向D 装置中加入足量的 H2O2溶液,再加入足量的BaCl2溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a克。
①加入 H2O2溶液发生反应的离子方程式是_______ 。
②浓硫酸与锌反应的临界浓度为:_______ mol/L。(用含a的计算式表示,忽略溶液体积变化)
(5)导管A竖直部分较长,其作用是_______ 。
(6)另甲同学提出测定方案:将D中的溶液酸化后,利用标准酸性KMnO4溶液测定原溶液中的SO ,从而计算临界浓度。乙同学认为相对于(4)中的测定方法,此方案会使测定结果偏高,你认为乙同学的理由是
,从而计算临界浓度。乙同学认为相对于(4)中的测定方法,此方案会使测定结果偏高,你认为乙同学的理由是_______ 。
已知:锌与浓硫酸开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。

(1)请写出锌与硫酸反应产生 SO2的化学方程式
(2)在组装仪器之后,加入试剂之前必须进行的操作是
(3)装置中干燥管C的作用是
(4)移动塑料棒,使锌浸没到硫酸中充分反应,反应结束后向D 装置中加入足量的 H2O2溶液,再加入足量的BaCl2溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a克。
①加入 H2O2溶液发生反应的离子方程式是
②浓硫酸与锌反应的临界浓度为:
(5)导管A竖直部分较长,其作用是
(6)另甲同学提出测定方案:将D中的溶液酸化后,利用标准酸性KMnO4溶液测定原溶液中的SO
 ,从而计算临界浓度。乙同学认为相对于(4)中的测定方法,此方案会使测定结果偏高,你认为乙同学的理由是
,从而计算临界浓度。乙同学认为相对于(4)中的测定方法,此方案会使测定结果偏高,你认为乙同学的理由是
您最近一年使用:0次
5 . 为了测定实验室长期存放的Na2SO3固体的纯度,准确称取W g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案Ⅰ:取25.00 mL上述溶液,加入足量的用过量盐酸酸化的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1 g。
方案Ⅱ:取25.00 mL上述溶液,加入过量的盐酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2 g。
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻璃棒、胶头滴管、药匙、________________ 、________ 。
(2)写出Na2SO3固体氧化变质的化学方程式_____________ 。
(3)方案Ⅰ加入过量的盐酸酸化的BaCl2溶液,目的是__________________________ ,
在过滤前,需要检验是否沉淀完全,其操作是______________ 。
(4)方案Ⅰ中,若滤液浑浊,将导致测定结果________ (填“偏高”或“偏低”)。
(5)若操作正确,则m1________ m2(填“>”、“<”或“=”),原因是_______________ 。
(6)取25.00 mL上述溶液,用酸性KMnO4溶液滴定的方法测定Na2SO3的纯度。已知酸性条件下,KMnO4通常被还原为Mn2+,则Na2SO3固体的纯度可表示为_____________ (注明表达式中所用的有关符号的含义和单位)。
方案Ⅰ:取25.00 mL上述溶液,加入足量的用过量盐酸酸化的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1 g。
方案Ⅱ:取25.00 mL上述溶液,加入过量的盐酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2 g。
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻璃棒、胶头滴管、药匙、
(2)写出Na2SO3固体氧化变质的化学方程式
(3)方案Ⅰ加入过量的盐酸酸化的BaCl2溶液,目的是
在过滤前,需要检验是否沉淀完全,其操作是
(4)方案Ⅰ中,若滤液浑浊,将导致测定结果
(5)若操作正确,则m1
(6)取25.00 mL上述溶液,用酸性KMnO4溶液滴定的方法测定Na2SO3的纯度。已知酸性条件下,KMnO4通常被还原为Mn2+,则Na2SO3固体的纯度可表示为
您最近一年使用:0次
2017-06-26更新
|
263次组卷
|
3卷引用:苏教版2017届高三单元精练检测一化学试题
名校
解题方法
6 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将过量铁粉加入稀硝酸中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 将铜粉加入1.0mol/LFe2(SO4)3溶液中 | 溶液由黄色变为蓝绿(青)色 | 金属铁比铜活泼 |
| C | 向久置的FeCl2溶液中加入酸性KMnO4溶液 | KMnO4溶液紫色褪去 | FeCl2溶液没有完全被氧化 |
| D | 将少量Na2SO3样品溶于足量稀盐酸中,静置,取上层溶液于试管中,滴加BaCl2溶液 | 产生白色沉淀 | 该Na2SO3样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-19更新
|
361次组卷
|
4卷引用:考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)黑龙江省哈尔滨市第九中学2020-2021学年高二下学期6月月考化学试题(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)湖南省衡阳师范学院祁东附属中学2021-2022学年高三上学期12月月考化学试题



