解题方法
1 . 元素化合物在日常生活、化工生产和环境科学中有着重要的用途。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是______________ 。
(2)自然界中Cr主要以+3价和+6价形式存在。Cr2O 中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O
中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O 还原。写出反应的离子方程式:
还原。写出反应的离子方程式:___________________________________________ 。
(3)当皮肤划破时可用FeCl3溶液应急止血,其主要作用是__________________ 。
(4)高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式Fe(OH)3+ C1O-+ OH-→ FeO + C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:
+ C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:__________ ,每生成1mol K2FeO4,转移的电子数是_________ 。
(5)合成氨及其相关工业中,部分物质间的转化关系如下:
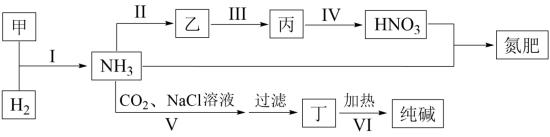
反应IV属于___________ 反应类型,氮肥主要成分的化学式为_______________ ,V的化学反应方程式为_________________ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是
(2)自然界中Cr主要以+3价和+6价形式存在。Cr2O
 中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O
中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O 还原。写出反应的离子方程式:
还原。写出反应的离子方程式:(3)当皮肤划破时可用FeCl3溶液应急止血,其主要作用是
(4)高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式Fe(OH)3+ C1O-+ OH-→ FeO
 + C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:
+ C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:(5)合成氨及其相关工业中,部分物质间的转化关系如下:

反应IV属于
您最近一年使用:0次
2 . 化学与生产、生活密切相关。下列物质用途不正确的是
| A.Al2O3熔点很高,可用作耐火材料,制作耐火管和耐火坩埚 |
| B.Na2CO3能与酸反应,可制成胃药治疗胃酸过多 |
| C.铝盐和铁盐可以在水中形成胶体,因此它们可以作净水剂 |
| D.Fe2O3是红棕色固体,可用作红色油漆和涂料 |
您最近一年使用:0次
解题方法
3 . 通常电动汽车使用的是锂电池,制备锂电池正极材料的主要原料为四氧化三钴,工业上用CoCl2·6H2O制备四氧化三钴。以水钴矿(主要成分为Co2O3、CoO、CuO、Fe2O3和SiO2等)为原料制备CoCl2·6H2O的工艺流程如图所示:
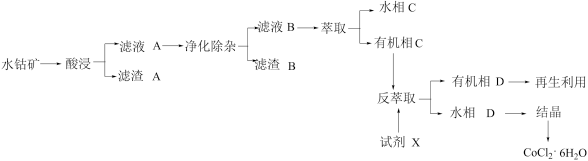
回答下列问题:
(1)“酸浸”
①写出滤渣A主要成分的一种用途________ 。钴的浸出率随酸浸时间、温度的变化关系如图所示。综合考虑,应选择的最佳工艺条件为________ 。
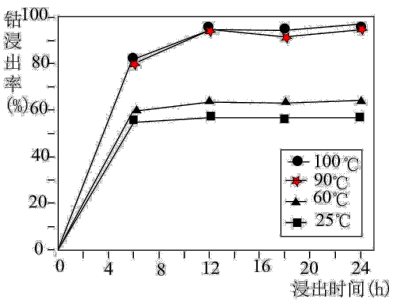
②Co2O3与浓硫酸反应除生成CoSO4和H2O外,还生成的一种物质是________ 。
(2)“净化除杂”过程包括除铁、除铜等步骤。
①除铁:加入适量Na2SO4固体,析出淡黄色晶体黄钠铁矾Na2Fe6(SO4)4(OH)12,写出反应的离子方程式____________________________________ 。
②除铜:加入适量Na2S2O3,发生反应2Cu2++2S2O +2H2O=Cu2S↓+S↓+4H++2SO
+2H2O=Cu2S↓+S↓+4H++2SO ,其中氧化产物为
,其中氧化产物为___________ 。
(3)“萃取和反萃取”
①试剂X的名称为_____________ 。
②实验室称取100 g原料(含钴11.80%),反萃取时得到浓度为0.036 mol·L-1的CoCl2溶液5 L,忽略损耗,钴的产率=_____________ 。
(4)以CoCl2·6H2O与NH4HCO3为原料,经两步经典反应合成四氧化三钴,第一步在80℃条件下二者生成Co2(OH)2CO3;第二步在600~820℃下Co2(OH)2CO3在空气中转化生成四氧化三钴,写出第二步反应的化学方程式_______________ 。

回答下列问题:
(1)“酸浸”
①写出滤渣A主要成分的一种用途

②Co2O3与浓硫酸反应除生成CoSO4和H2O外,还生成的一种物质是
(2)“净化除杂”过程包括除铁、除铜等步骤。
①除铁:加入适量Na2SO4固体,析出淡黄色晶体黄钠铁矾Na2Fe6(SO4)4(OH)12,写出反应的离子方程式
②除铜:加入适量Na2S2O3,发生反应2Cu2++2S2O
 +2H2O=Cu2S↓+S↓+4H++2SO
+2H2O=Cu2S↓+S↓+4H++2SO ,其中氧化产物为
,其中氧化产物为(3)“萃取和反萃取”
①试剂X的名称为
②实验室称取100 g原料(含钴11.80%),反萃取时得到浓度为0.036 mol·L-1的CoCl2溶液5 L,忽略损耗,钴的产率=
(4)以CoCl2·6H2O与NH4HCO3为原料,经两步经典反应合成四氧化三钴,第一步在80℃条件下二者生成Co2(OH)2CO3;第二步在600~820℃下Co2(OH)2CO3在空气中转化生成四氧化三钴,写出第二步反应的化学方程式
您最近一年使用:0次



