1 . 草酸亚铁晶体( ,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。
,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。

(1)按照气流从左到右的方向,上述装置的接口顺序为A→_______ →尾气处理装置(仪器可重复使用)。
(2)实验证明了气体产物中含有 ,依据的实验现象为
,依据的实验现象为_______ 。
(3)实验证明了气体产物中含有CO,依据的实验现象为_______ 。
(4)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为_______ 。
(5)工业制得的草酸亚铁晶体中常含有 杂质,测定其纯度的步骤如下:
杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品溶于稀 中,配成250 mL溶液;
中,配成250 mL溶液;
步骤2:取上述溶液25.00 mL,用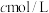
 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 ;
;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀 ,再用
,再用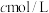
 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 。
。
①步骤2中滴定终点的现象为_______ 。
②该样品中草酸亚铁晶体的质量分数的表达式为_______ 。
③若步骤1配制溶液时部分 被氧化变质,则测定结果将
被氧化变质,则测定结果将_______ (填“偏高”“偏低”或“不变”)。
 ,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。
,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。
(1)按照气流从左到右的方向,上述装置的接口顺序为A→
(2)实验证明了气体产物中含有
 ,依据的实验现象为
,依据的实验现象为(3)实验证明了气体产物中含有CO,依据的实验现象为
(4)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(5)工业制得的草酸亚铁晶体中常含有
 杂质,测定其纯度的步骤如下:
杂质,测定其纯度的步骤如下:步骤1:称取m g草酸亚铁晶体样品溶于稀
 中,配成250 mL溶液;
中,配成250 mL溶液;步骤2:取上述溶液25.00 mL,用
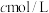
 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 ;
;步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀
 ,再用
,再用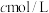
 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 。
。①步骤2中滴定终点的现象为
②该样品中草酸亚铁晶体的质量分数的表达式为
③若步骤1配制溶液时部分
 被氧化变质,则测定结果将
被氧化变质,则测定结果将
您最近一年使用:0次
2022-12-16更新
|
190次组卷
|
2卷引用:黑龙江省海伦市第一中学2022-2023学年高三上学期1月期末考试化学试题
名校
2 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 取久置的 粉末,向其中滴加过量的盐酸,产生无色气体 粉末,向其中滴加过量的盐酸,产生无色气体 |  粉末没有变质 粉末没有变质 |
| B | 将 样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 |  样品已变质 样品已变质 |
| C | 将 气体通入棕黄色 气体通入棕黄色 溶液,溶液变为浅绿色 溶液,溶液变为浅绿色 |  具有还原性 具有还原性 |
| D | 把 和气体X一起通入到 和气体X一起通入到 溶液中,有白色沉淀产生 溶液中,有白色沉淀产生 | X气体具有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-09更新
|
353次组卷
|
2卷引用:黑龙江省哈尔滨市第三中学校2023-2024学年 高一下学期第一次验收考试化学试题
名校
解题方法
3 . 氯化亚铜(CuCl)广泛用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。学习小组开展了与CuCl相关的系列实验。回答下列问题:
Ⅰ.利用废铜屑制备 ,实验装置如图所示。
,实验装置如图所示。_______ 。
(2)三颈烧瓶中制备 的化学方程式为
的化学方程式为____ ,将浓盐酸加入三颈烧瓶的操作为:____ ,再将分液漏斗下面的活塞打开。
Ⅱ.制备氯化亚铜,制备流程如图所示:
(3)反应①中氧化剂与还原剂的物质的量之比为_______ ,操作②为_______ 。
(4)析出的CuCl粗产品不用盐酸而用水、乙醇分别洗涤的目的依次是_____ 、_______ 。
(5)测定产品中CuCl的质量分数。准确称取制备的CuCl产品0.40g,加入足量的氯化铁溶液,待样品全部溶解后,加入适量稀硫酸,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液24.00mL,反应中
溶液24.00mL,反应中 被还原为
被还原为 ,产品中CuCl的质量分数为
,产品中CuCl的质量分数为_____ (保留四位有效数字)。
Ⅰ.利用废铜屑制备
 ,实验装置如图所示。
,实验装置如图所示。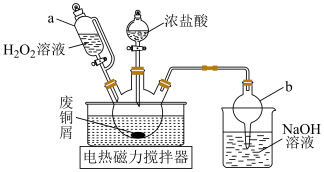
(2)三颈烧瓶中制备
 的化学方程式为
的化学方程式为Ⅱ.制备氯化亚铜,制备流程如图所示:


(3)反应①中氧化剂与还原剂的物质的量之比为
(4)析出的CuCl粗产品不用盐酸而用水、乙醇分别洗涤的目的依次是
(5)测定产品中CuCl的质量分数。准确称取制备的CuCl产品0.40g,加入足量的氯化铁溶液,待样品全部溶解后,加入适量稀硫酸,用
 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液24.00mL,反应中
溶液24.00mL,反应中 被还原为
被还原为 ,产品中CuCl的质量分数为
,产品中CuCl的质量分数为
您最近一年使用:0次
名校
4 . 下列实验的实验操作、现象及所得到的结论均正确的是
选项 | 实验操作 | 现象和结论 |
A | 取少量硫代硫酸钠样品溶于水,先加入过量稀盐酸,再滴加 溶液 溶液 | 有沉淀生成,则硫代硫酸钠已变质生成了硫酸钠 |
B | 向 溶液中加入醋酸,将产生的气体通入苯酚钠水溶液中 溶液中加入醋酸,将产生的气体通入苯酚钠水溶液中 | 观察到苯酚钠溶液变浑浊,则碳酸的酸性强于苯酚 |
C | 常温下,测定 溶液酸碱性 溶液酸碱性 | 若溶液呈碱性,则 为弱酸 为弱酸 |
D | 相同温度下,向含有NaCl、NaBr的混合溶液中逐滴加入 溶液 溶液 | 先出现淡黄色沉淀,则 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-29更新
|
473次组卷
|
2卷引用:黑龙江省哈尔滨市第三中学校2023-2024学年高三一模化学试题
5 . 下列有关实验、现象及结论等叙述正确的个数有
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
2024-04-19更新
|
297次组卷
|
2卷引用:黑龙江省大庆铁人中学2023-2024学年高一下学期开学考试化学试题
名校
解题方法
6 . 氨基甲酸铵是一种白色固体,易水解,是工业上生产尿素的副产物,可以用于药物合成。实验室向四氯化碳中通入干燥的二氧化碳和氨气制取氨基甲酸铵固体,实验装置如下图,反应的化学方程式为 。
。
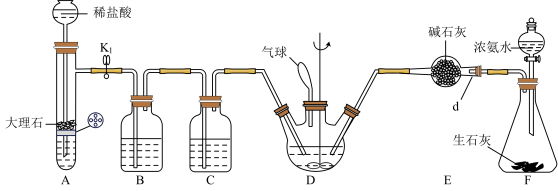
回答下列问题:
(1)仪器d的名称为
___________ ;装置F中发生反应的化学方程式为
___________ 。
(2)装置B中盛放的试剂为
___________ 。
(3)装置D中气球的作用是
___________ 。
(4)反应过程中需要将装置D放入冰水浴中,原因是
___________ 。
(5)氨基甲酸铵易水解,在潮湿的空气中发生水解反应生成碳酸氢铵的化学方程式为
________ 。
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品
 ,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得其质量为
,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得其质量为
 。则样品中氨基甲酸铵的物质的量分数为
。则样品中氨基甲酸铵的物质的量分数为
___________ 。(碳酸氢铵和氨基甲酸铵的相对分子质量分别为79和78)。
 。
。
回答下列问题:
(1)仪器d的名称为
(2)装置B中盛放的试剂为
(3)装置D中气球的作用是
(4)反应过程中需要将装置D放入冰水浴中,原因是
(5)氨基甲酸铵易水解,在潮湿的空气中发生水解反应生成碳酸氢铵的化学方程式为
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品
 ,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得其质量为
,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得其质量为 。则样品中氨基甲酸铵的物质的量分数为
。则样品中氨基甲酸铵的物质的量分数为
您最近一年使用:0次
7 . 以硫铁矿(主要成分为FeS2,还有少量CuS、SiO2等杂质)为原料制备绿矾晶体(FeSO4·7H2O)的工艺流程如下:

(1)“酸浸”过程,矿渣中的Fe2O3与稀H2SO4反应的离子方程式为_______ 。
(2)滤液中金属阳离子的检验方法_______ 。
(3)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.F)对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如下图所示:
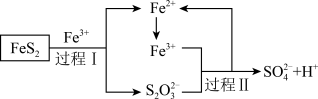
过程Ⅱ反应的离子方程式为_______ 。
(4)FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na2FeO4),其氧化性比Cl2、O2、ClO2、KMnO4更强,工业上有多种制备高铁酸钠方法。
①干法制备:主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中的氧化剂是_______ ,还原剂是_______ 。
②湿法制备:在碱性条件下,用NaClO溶液和Fe2(SO4)3溶液反应制备。该反应的离子方程式为_______ 。
③在Na2FeO4溶液中加入稀硫酸,溶液很快变为棕黄色,并有无色气体产生。该反应的离子方程式为_______ 。
(5)绿矾晶体在空气中易被氧化变质。取x g样品,加水完全溶解,滴加硫酸酸化的a mol/L K2Cr2O7溶液至恰好完全反应,消耗K2Cr2O7溶液b mL。
反应原理:6Fe2++Cr2O +14H+ = 6Fe3++2Cr3++7H2O。
+14H+ = 6Fe3++2Cr3++7H2O。
则绿矾晶体纯度的计算式为_______ 。

(1)“酸浸”过程,矿渣中的Fe2O3与稀H2SO4反应的离子方程式为
(2)滤液中金属阳离子的检验方法
(3)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.F)对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如下图所示:

过程Ⅱ反应的离子方程式为
(4)FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na2FeO4),其氧化性比Cl2、O2、ClO2、KMnO4更强,工业上有多种制备高铁酸钠方法。
①干法制备:主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中的氧化剂是
②湿法制备:在碱性条件下,用NaClO溶液和Fe2(SO4)3溶液反应制备。该反应的离子方程式为
③在Na2FeO4溶液中加入稀硫酸,溶液很快变为棕黄色,并有无色气体产生。该反应的离子方程式为
(5)绿矾晶体在空气中易被氧化变质。取x g样品,加水完全溶解,滴加硫酸酸化的a mol/L K2Cr2O7溶液至恰好完全反应,消耗K2Cr2O7溶液b mL。
反应原理:6Fe2++Cr2O
 +14H+ = 6Fe3++2Cr3++7H2O。
+14H+ = 6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为
您最近一年使用:0次
名校
8 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究金属钠在氧气中受热所剩固体的成分 | 取少量固体粉末,加入 蒸馏水 蒸馏水 | 若无气体生成,则固体粉末为 ;若有气体生成,则固体粉末为 ;若有气体生成,则固体粉末为 |
| B | 探究 与 与 反应的限度 反应的限度 | 取 溶液于试管中,加入 溶液于试管中,加入 溶液,充分反应后滴入几滴 溶液,充分反应后滴入几滴 溶液 溶液 | 若溶液变红,则 与 与 的反应有一定限度 的反应有一定限度 |
| C | 检验某无色溶液中是否含有 | 取少量该溶液于试管中,滴加稀氢氧化钠溶液,用湿润的红色石蕊试纸放试管口 | 试纸不变蓝,证明溶液中无铵根离子 |
| D | 探究 固体样品是否变质 固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液 溶液 | 若有白色沉淀产生,则样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-13更新
|
233次组卷
|
4卷引用:黑龙江省佳木斯市第十二中学2022-2023学年高二上学期开学考试化学试题
解题方法
9 . 有一Na2SO3固体因部分被氧化而变质。为测定样品纯度,甲、乙两位同学分别设计了如下实验方案:
甲同学:称取mg样品溶于水,加入过量的BaCl2溶液。过滤,向沉淀中加入过量盐酸,再过滤,将残留固体洗涤后进行烘干,冷却后称得质量为m1g。
(1)BaCl2溶液必须过量的原因是_______ 。在滤液中滴加_______ 溶液,若没有白色沉淀生成,则证明BaCl2溶液不足,还需继续在滤液中加入BaCl2溶液后进行过滤。
(2)洗涤残留固体的方法是_______ ;在洗出液中滴加_______ 溶液,可以判断残留固体是否洗涤干净。
乙同学:称取mg样品溶于水,配成溶液,用滴定管取VmL于锥形瓶中,用浓度为cmol/L的标准酸性高锰酸钾溶液滴定至终点。反应关系为:SO +MnO
+MnO SO
SO +Mn2+(未配平)
+Mn2+(未配平)
(3)配制样品溶液时,不一定 需要的实验仪器是_______(选填答案编号)。
(4)滴定终点的判断依据是_______ 。
(5)上述滴定中,滴定管在注入酸性高锰酸钾溶液之前,先用蒸馏水洗净,再用_______ 。滴定管液面变化如图所示,从图Ⅰ图Ⅱ显示消耗的高锰酸钾溶液体积为_______ 。

甲同学:称取mg样品溶于水,加入过量的BaCl2溶液。过滤,向沉淀中加入过量盐酸,再过滤,将残留固体洗涤后进行烘干,冷却后称得质量为m1g。
(1)BaCl2溶液必须过量的原因是
(2)洗涤残留固体的方法是
乙同学:称取mg样品溶于水,配成溶液,用滴定管取VmL于锥形瓶中,用浓度为cmol/L的标准酸性高锰酸钾溶液滴定至终点。反应关系为:SO
 +MnO
+MnO SO
SO +Mn2+(未配平)
+Mn2+(未配平)(3)配制样品溶液时,
| A.容量瓶 | B.玻璃棒 | C.滴定管 | D.烧杯 |
(5)上述滴定中,滴定管在注入酸性高锰酸钾溶液之前,先用蒸馏水洗净,再用

您最近一年使用:0次
名校
10 . 下列有关实验、现象、及结论等叙述正确的有( )
①向溶有 的
的 溶液中通入气体X,出现白色沉淀,X具有强氧化性
溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向某溶液加入稀硫酸有白色沉淀产生,该溶液中一定含有钡离子
④向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有
⑤向饱和 溶液中滴加硼酸,无气泡产生,非金属性:硼<碳
溶液中滴加硼酸,无气泡产生,非金属性:硼<碳
⑥取少量 样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
①向溶有
 的
的 溶液中通入气体X,出现白色沉淀,X具有强氧化性
溶液中通入气体X,出现白色沉淀,X具有强氧化性②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向某溶液加入稀硫酸有白色沉淀产生,该溶液中一定含有钡离子
④向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有

⑤向饱和
 溶液中滴加硼酸,无气泡产生,非金属性:硼<碳
溶液中滴加硼酸,无气泡产生,非金属性:硼<碳⑥取少量
 样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质| A.1条 | B.0条 | C.3条 | D.4条 |
您最近一年使用:0次
2022-12-15更新
|
1148次组卷
|
4卷引用:黑龙江省鹤岗市第一中学2022-2023学年高一下学期5月期中考试化学试题



