1 . 回答下列问题。
(1)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为_______ 。
(2)基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
(3) 位于元素周期表中第四周期第
位于元素周期表中第四周期第_______ 族。
(4)基态 原子价电子的电子排布图(轨道表达式)为
原子价电子的电子排布图(轨道表达式)为_______ 。
(5) 原子核外电子排布式为
原子核外电子排布式为_______ 。
(6)氮原子价层电子的轨道表达式(电子排布图)为_______ 。
(7) 基态原子核外电子排布式为
基态原子核外电子排布式为_______ 。
(1)基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(2)基态
 原子的核外电子排布式为
原子的核外电子排布式为(3)
 位于元素周期表中第四周期第
位于元素周期表中第四周期第(4)基态
 原子价电子的电子排布图(轨道表达式)为
原子价电子的电子排布图(轨道表达式)为(5)
 原子核外电子排布式为
原子核外电子排布式为(6)氮原子价层电子的轨道表达式(电子排布图)为
(7)
 基态原子核外电子排布式为
基态原子核外电子排布式为
您最近一年使用:0次
名校
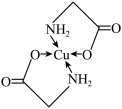
2 . 太阳能的开发利用在新能源研究中占据重要地位,单品硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物的结构如图所示。请回答下列问题:_______ 区,最外层原子轨道呈_______ 形。
(2)基态二价铜离子的电子排布式为_______ ,已知高温下 比CuO更稳定,试从核外电子排布角度解释
比CuO更稳定,试从核外电子排布角度解释_______ 。
(3)在基态硼原子中,核外存在_______ 个运动状态不同的电子。
(4) 的价层电子排布图为
的价层电子排布图为_______ 。
(5)根据元素周期律,电负性O_______ Se(填“大于”“小于”或“等于”),N、O、Se三种元素中的第一电离能最大的为_______ 。
(2)基态二价铜离子的电子排布式为
 比CuO更稳定,试从核外电子排布角度解释
比CuO更稳定,试从核外电子排布角度解释(3)在基态硼原子中,核外存在
(4)
 的价层电子排布图为
的价层电子排布图为(5)根据元素周期律,电负性O
您最近一年使用:0次
名校
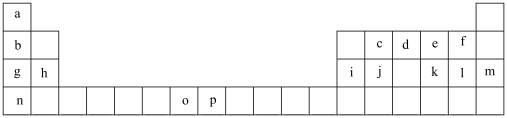
3 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题。_______ (用元素符号表示),1和n的离子半径较大的是_______ (填离子符号)。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是_______ (填字母)。
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p两元素的部分电离能数据如下表所示。
比较两元素的 、
、 可知,气态
可知,气态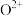 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是_______ 。
(4)第三周期8种元素其中电负性最大的是_______ (填图中的序号)。
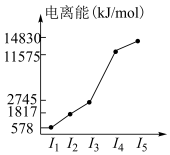
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式:_______ 。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p两元素的部分电离能数据如下表所示。
电离能/ |  |  |  |
| o | 717 | 1509 | 3248 |
| p | 759 | 1561 | 2957 |
 、
、 可知,气态
可知,气态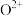 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是(4)第三周期8种元素其中电负性最大的是
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次
名校
4 . 已知五种短周期元素的原子半径及主要化合价(最高正价、最低负价)如下表:
下列叙述正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A.T与氢元素形成的化合物中一定只含极性键 |
| B.L-M-稀硫酸原电池、L-M-NaOH溶液原电池中,负极均是L |
| C.Q的一种氧化物是能使品红溶液褪色的气体,该气体通入BaCl2溶液可观察到有白色沉淀产生 |
| D.M的最高价氧化物既能与NaOH溶液反应,又能与稀盐酸反应 |
您最近一年使用:0次
名校
5 . 某基态原子核外共有6个电子,分布在K与L能层上,在下列L层分布中正确的是
A. | B. |
C. | D. |
您最近一年使用:0次
名校
6 . 电子在原子核外排布时,下列说法正确的是
①电子排布在同一能级时,总是优先单独占据不同轨道,且自旋平行
②电子排布在不同能级时,总是优先占据能量低的轨道,然后再占据能量高的轨道
③电子排布在同一轨道时,最多只能排2个,且自旋相反
④电子的排布总是同时遵循“能量最低原理”“泡利原理”和“洪特规则”
①电子排布在同一能级时,总是优先单独占据不同轨道,且自旋平行
②电子排布在不同能级时,总是优先占据能量低的轨道,然后再占据能量高的轨道
③电子排布在同一轨道时,最多只能排2个,且自旋相反
④电子的排布总是同时遵循“能量最低原理”“泡利原理”和“洪特规则”
| A.①② | B.②④ | C.①③ | D.②③④ |
您最近一年使用:0次
解题方法
7 . 乙烯基乙炔(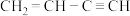 )在工业上主要用于制备合成橡胶的原料2-氯-1,3-丁二烯(结构简式为
)在工业上主要用于制备合成橡胶的原料2-氯-1,3-丁二烯(结构简式为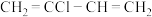 )。请回答下列问题:
)。请回答下列问题:
(1)乙烯基乙炔中的官能团是___________ (写名称)。
(2)乙烯基乙炔生成2-氯-1,3-丁二烯的反应方程式是___________ 。
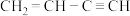 )在工业上主要用于制备合成橡胶的原料2-氯-1,3-丁二烯(结构简式为
)在工业上主要用于制备合成橡胶的原料2-氯-1,3-丁二烯(结构简式为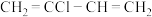 )。请回答下列问题:
)。请回答下列问题:(1)乙烯基乙炔中的官能团是
(2)乙烯基乙炔生成2-氯-1,3-丁二烯的反应方程式是
您最近一年使用:0次
8 . A、B、C、D四种烃分子中均含有8个氢原子,其中A、B常温下呈气态,C、D呈液态。
(1)A是符合上述条件中相对分子质量最小的,则A的分子式为___________ ;
(2)B属于链状单烯烃,且与HBr加成的产物只有一种,试写出B与HBr反应的化学方程式___________ 。
(3)C属于芳香烃,1molC最多能和3molH2加成,试写出C的结构简式___________ 。
(1)A是符合上述条件中相对分子质量最小的,则A的分子式为
(2)B属于链状单烯烃,且与HBr加成的产物只有一种,试写出B与HBr反应的化学方程式
(3)C属于芳香烃,1molC最多能和3molH2加成,试写出C的结构简式
您最近一年使用:0次
9 . 根据所学知识回答下列问题:
(1)甲基电子式:___________ 。
(2)用系统命名法命名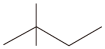 为
为___________ 。
(1)甲基电子式:
(2)用系统命名法命名
 为
为
您最近一年使用:0次
10 . 在卤代烃R—CH2—CH2—X中化学键如下图所示,则下列说法正确的是
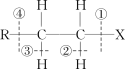
| A.当该卤代烃发生水解反应时,被破坏的键是①和③ |
| B.当该卤代烃发生消去反应时,被破坏的键是①和④ |
| C.当该卤代烃发生水解反应时,被破坏的键是① |
| D.当该卤代烃发生消去反应时,被破坏的键是①和② |
您最近一年使用:0次



