1 . 下图是A、B两种重要的有机合成原料。下列有关说法中正确的是


| A.A与B互为同系物 |
| B.A与B都能与溴的四氯化碳溶液发生加成反应 |
| C.在一定条件下,A与B均能发生取代反应 |
| D.A与B都能与碳酸氢钠反应产生氢气 |
您最近一年使用:0次
2016-12-09更新
|
377次组卷
|
3卷引用:2016届江西省红色七校高三上学期第一次联考化学试卷
2 . A、B、C、D、E是五种短周期主族元素,它们的原子序数依次增大,其中A的最高正价与最低负价的代数和等于0,B、E是同一主族元素,C元素的原子半径大于所在同周期中其它主族元素的原子半径,D元素的最外层电子数等于其电子层数,E元素的最外层电子数是次外层电子数的0.75倍,则下列说法正确的是
| A.B、C、D形成的简单离子,半径最小的是B |
| B.E形成最简单氢化物稳定性比B的强 |
| C.A、C、D形成的最高价氧化物的水化物两两间可相互反应 |
| D.A、B形成的化合物与B、E形成的化合物化学键类型相同 |
您最近一年使用:0次
2016-12-09更新
|
160次组卷
|
3卷引用:2016届江西省红色七校高三上学期第一次联考化学试卷
3 . 下列图像表达正确的是
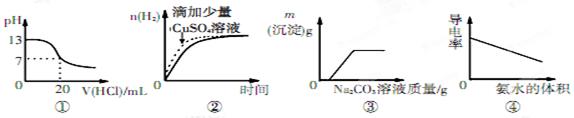

| A.图①表示25℃时, 用0.1mol·L-1盐酸滴定20mL 0.1mol·L-1NaOH溶液 |
| B.图②表示常温下,两份足量、等浓度的盐酸与等量锌粉反应时,其中一份滴加了少量硫酸铜溶液 |
| C.图③表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 |
| D.图④表示向醋酸溶液中滴入氨水 |
您最近一年使用:0次
2016-12-09更新
|
204次组卷
|
2卷引用:2016届江西省红色七校高三上学期第一次联考化学试卷
4 . 检验某溶液中是否含有 K+、Fe3+、Cl- 、Mg2+、I- 、CO32- 、SO42-,限用的试剂有:盐酸、硫酸、硝酸银溶液、硝酸钡溶液。设计如下实验步骤,并记录相关现象。下列叙述不正确的是
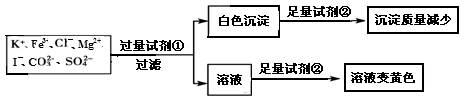

| A.该溶液中一定有 I- 、CO32- 、SO42- 、K+ |
| B.试剂①为硝酸钡 |
| C.通过在黄色溶液中加入硝酸银可以检验原溶液中是否存在Cl- |
| D.试剂②一定为盐酸 |
您最近一年使用:0次
2016-12-09更新
|
248次组卷
|
3卷引用:2016届江西省红色七校高三上学期第一次联考化学试卷
名校
5 . 将一定质量的镁、铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物全部是NO)。向反应后的溶液中加入3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加7.65g,则下列叙述中正确的是
| A.当生成沉淀达到最大量时,消耗NaOH溶液的体积为150mL |
| B.当金属全部溶解时收集到NO气体的体积为0.336L(标准状况下) |
| C.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.6mol |
| D.参加反应的金属的总质量一定是9.9g |
您最近一年使用:0次
2016-12-09更新
|
1632次组卷
|
5卷引用:2016届江西省红色七校高三上学期第一次联考化学试卷
6 . 纯过氧化氢是淡蓝色的黏稠液体,可任意比例与水混合,是一种强氧化剂,水溶液俗称双氧水,为无色透明液体。其水溶液适用于医用伤口消毒及环境消毒和食品消毒。
(1)请写出H2O2的电子式____________ 。
(2)往硫酸中加入一定浓度的双氧水可将溶解铜,写出该反应的离子方程式_________________ 。
(3)Fe3+催化H2O2分解的机理可分两步反应进行,第一步反应为:2Fe3++H2O2=2Fe2++O2↑+2H+,
请完成第二步反应的离子方程式:
___ Fe2++ ___ H2O2 + ___ _________ == ___ _________ + ___ _________
(4)下图是一种用电解原理来制备过氧化氢并用产生的H2O2处理废氨水的装置
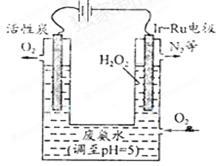
①为了不影响H2O2的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+)_______________ c(NO3-)(填“>”、“<”或“=”)。
②Ir-Ru惰性电极有吸附O2作用,该电极上的反应为______________________ 。
③理论上电路中每转移3mol电子,最多可以处理NH3·H2O的物质的量为_______________ 。
(1)请写出H2O2的电子式
(2)往硫酸中加入一定浓度的双氧水可将溶解铜,写出该反应的离子方程式
(3)Fe3+催化H2O2分解的机理可分两步反应进行,第一步反应为:2Fe3++H2O2=2Fe2++O2↑+2H+,
请完成第二步反应的离子方程式:
(4)下图是一种用电解原理来制备过氧化氢并用产生的H2O2处理废氨水的装置

①为了不影响H2O2的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+)
②Ir-Ru惰性电极有吸附O2作用,该电极上的反应为
③理论上电路中每转移3mol电子,最多可以处理NH3·H2O的物质的量为
您最近一年使用:0次
7 . 设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.32g甲醇中含有C—H键的数目为4NA |
| B.60g熔融的NaHSO4中含有的离子数目为1.5NA |
| C.Na2O2与足量H2O反应产生0.2molO2,转移电子的数目为0.4NA |
| D.惰性电极电解食盐水,当线路中通过电子数为NA时,阳极产生气体11.2L |
您最近一年使用:0次
2016-07-07更新
|
161次组卷
|
4卷引用:2016届江西省红色七校高三上学期第一次联考化学试卷
2016届江西省红色七校高三上学期第一次联考化学试卷2015-2016学年河北省定兴三中高二6月月考化学试卷2015-2016学年辽宁省实验中学分校高二下学期6月月考化学试卷(已下线)2022年浙江1月高考真题变式题(11-20)
名校
解题方法
8 . 在催化剂、400℃时可实现氯的循环利用,下图是其能量关系图下列分析正确的是
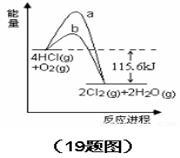

| A.曲线a是使用了催化剂的能量变化曲线 |
| B.反应物的总键能高于生成物的总键能 |
| C.反应的热化学方程式为:4HCl(g)+O2(g) = 2Cl2+2H2O(g)△H=-115.6 kJ |
| D.若反应生成2mol液态水,放出的热量高于115.6kJ |
您最近一年使用:0次
2016-05-25更新
|
240次组卷
|
10卷引用:2016届江西省红色七校高三上学期第一次联考化学试卷



