23-24高一下·全国·课前预习
解题方法
1 . 葡萄糖、果糖
(1)二者分子式相同,但结构_____ ,互为同分异构体。均属于多羟基醛,官能团有_____ ,既有_____ 的性质,又有_____ 的性质。
(2)葡萄糖中醛基的检验
(1)二者分子式相同,但结构
(2)葡萄糖中醛基的检验
| 实验内容 | 实验操作 | 实验现象 | 解释或结论 |
| 用银氨溶液检验醛基 |  | ||
| 用新制氢氧化铜悬浊液检验醛基 | 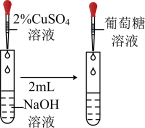 |
您最近一年使用:0次
23-24高一下·全国·课前预习
2 . 二氧化硫
(1)物理性质:二氧化硫是一种___________ 色有___________ 气味的有___________ 气体,密度比空气的___________ ,___________ 溶于水,通常情况下,1体积的水可以溶解___________ 体积的二氧化硫。
(2)化学性质
①与水反应:___________ 。
②与碱(NaOH溶液、澄清石灰水)反应:___________ 、___________ 。
③还原性(与H2O2反应):___________ 。
④氧化性(与H2S反应):___________ 。
⑤漂白性:使某些有色物质(如品红溶液)生成___________ 的无色物质,若加热,___________ 的颜色。
(1)物理性质:二氧化硫是一种
(2)化学性质
①与水反应:
②与碱(NaOH溶液、澄清石灰水)反应:
③还原性(与H2O2反应):
④氧化性(与H2S反应):
⑤漂白性:使某些有色物质(如品红溶液)生成
您最近一年使用:0次
23-24高一下·全国·课前预习
3 . 以下实验中分别利用了硫酸的哪些性质?请将答案的序号分别填在横线上。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)在胆矾晶体中滴加浓硫酸,晶体由蓝变白;______ 。
(2)浓硫酸滴在纸屑、棉花上变黑;______ 。
(3)亚硫酸钠中加入硫酸,产生二氧化硫;______ 。
(4)适量浓硫酸与蔗糖混合后,体积膨胀颜色变黑;______ 。
(5)浓硫酸与活泼金属反应无氢气生成;______ 。
(6)浓硫酸与铜反应,溶液变蓝,且生成刺激性气体;______ 。
(7)可以用铁制容器装运浓硫酸;______ 。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)在胆矾晶体中滴加浓硫酸,晶体由蓝变白;
(2)浓硫酸滴在纸屑、棉花上变黑;
(3)亚硫酸钠中加入硫酸,产生二氧化硫;
(4)适量浓硫酸与蔗糖混合后,体积膨胀颜色变黑;
(5)浓硫酸与活泼金属反应无氢气生成;
(6)浓硫酸与铜反应,溶液变蓝,且生成刺激性气体;
(7)可以用铁制容器装运浓硫酸;
您最近一年使用:0次
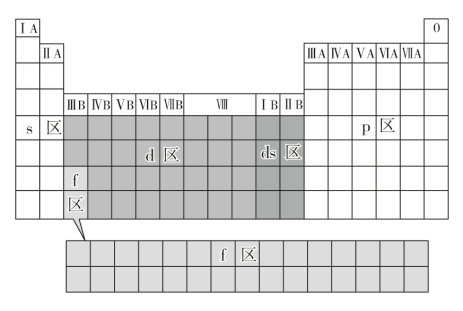
4 . 核外电子排布与元素周期系的基本结构
①根据构造原理得出的核外电子排布可以解释元素周期系中每个周期的元素数。第一周期从1s1开始,以1s2结束,只有_______ 种元素。其余各周期总是从ns能级开始,以np结束,而从ns能级开始以np结束递增的核电荷数(或电子数)就_______ 每个周期里的元素数。
②周期、能级组、元素种类的对应关系
①根据构造原理得出的核外电子排布可以解释元素周期系中每个周期的元素数。第一周期从1s1开始,以1s2结束,只有
②周期、能级组、元素种类的对应关系
| 周期 | 对应能级组 | 对应能级组最多所能容纳的电子数 | 周期中所含元素种类 |
| 1 | 1s | 2 | 2 |
| 2 | 8 | ||
| 3 | 3s、3p | 8 | 8 |
| 4 | 18 | ||
| 5 | 5s、4d、5p | 18 | 18 |
| 6 | 32 | ||
| 7 | 7s、5f、6d、7p | 32 | 32 |
您最近一年使用:0次
5 . 原子轨道
(1)定义
_____ 称为原子轨道。
(2)原子轨道的形状
s电子原子轨道是_____ 形的,p电子原子轨道是_____ 形的。
(1)定义
(2)原子轨道的形状
s电子原子轨道是
您最近一年使用:0次
23-24高一下·全国·课前预习
6 . 电子云
电子云是处于一定空间运动状态的电子在原子核外空间的_____ 分布的形象化描述,小黑点越密,表示概率密度越大。由于核外电子的_____ 分布看起来像是一片云雾,因而被形象地称作电子云。
电子云是处于一定空间运动状态的电子在原子核外空间的
您最近一年使用:0次
7 . 电子运动的特点
现代量子力学指出,无法确定核外电子在某个时刻处于原子核外空间何处,只能确定在原子核外各处出现的_____ 。用P表示电子在某处出现的_____ ,V表示该处的体积,则P/V称为_____ ,用ρ表示。
现代量子力学指出,无法确定核外电子在某个时刻处于原子核外空间何处,只能确定在原子核外各处出现的
您最近一年使用:0次
23-24高一下·全国·课前预习
8 . 构造原理
随着原子_____ 的递增,绝大多数元素的原子核外电子将遵循以下顺序填充到各能级中:1s、2s、2p、3s、3p、4s、_____ 、4p、5s、_____ 、5p、6s、_____ 、_____ 、6p、7s……这个排列顺序被称为构造原理。(见教材P6构造原理示意图)
随着原子
您最近一年使用:0次
9 . 元素在周期表中的位置与元素原子的结构、性质间的关系
(1)在元素周期表中,同族元素价层电子数_______ ,是同族元素性质_______ 的结构基础。
(2)长周期比短周期多出的元素,其原子的最外层电子数_______ 2(Pd除外),所以它们全部是_______ 。
(1)在元素周期表中,同族元素价层电子数
(2)长周期比短周期多出的元素,其原子的最外层电子数
您最近一年使用:0次