1 . S8与NH3在无水条件下反应,得到一种二元化合物A,元素分析可知,A中含S元素69.60%。A进行如下反应:
(1)A、B、C、D的化学式分别为___________ 、___________ 、___________ 、___________ 。
(2)A与SnCl2的乙醇溶液反应除生成B外,还生成一种含Sn(IV)化合物,试写出A→B的化学方程式___________ 。
(3)D与一种无色液体(该液体是由常见的红棕色气体在加压下形成的)互为等电子体,但D与无色液体的几何构型完全不同,为环状结构,试画出D的最稳定的Lewis结构式___________ ,理由是___________ ,该Lewis结构式中,S原子的电子构型是___________ 。

(1)A、B、C、D的化学式分别为
(2)A与SnCl2的乙醇溶液反应除生成B外,还生成一种含Sn(IV)化合物,试写出A→B的化学方程式
(3)D与一种无色液体(该液体是由常见的红棕色气体在加压下形成的)互为等电子体,但D与无色液体的几何构型完全不同,为环状结构,试画出D的最稳定的Lewis结构式
您最近一年使用:0次
名校
2 . 亚硫酸钠和硫代硫酸钠(Na2S2O3)都是重要的含硫化合物。某化学兴趣小组进行以下有关实验,填写下列空白。
实验Ⅰ:证明Na2SO3中硫元素的价态能发生+4→+6转化
(1)实验中,不需要用到的试剂有___________ (填标号)。
a.稀硫酸 b.H2O2溶液 c.稀盐酸 d.淀粉碘化钾溶液 e.BaCl2溶液
观察到的现象是___________ 。
实验Ⅱ:制取硫代硫酸钠
利用如图所示装置进行实验___________ 。
(3)装置D的作用是___________ 。
(4)实验中,为使 缓慢通入烧瓶C,采取的操作是
缓慢通入烧瓶C,采取的操作是___________ 。
实验Ⅲ:测定某硫代硫酸钠样品的纯度(设样品中只含Na2SO3杂质)
设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品7.9g,配制成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用0.1mol·L-1I2标准溶液滴定(发生反应:2S2O +I2=S4O
+I2=S4O +2I-),至滴定终点共消耗标准溶液23.60mL。
+2I-),至滴定终点共消耗标准溶液23.60mL。
(5)样品中Na2S2O3的百分含量为___________ (保留三位有效数字)。
实验Ⅰ:证明Na2SO3中硫元素的价态能发生+4→+6转化
(1)实验中,不需要用到的试剂有
a.稀硫酸 b.H2O2溶液 c.稀盐酸 d.淀粉碘化钾溶液 e.BaCl2溶液
观察到的现象是
实验Ⅱ:制取硫代硫酸钠
利用如图所示装置进行实验
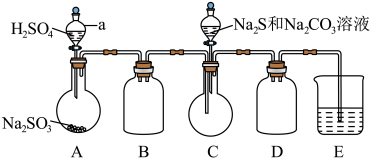
(3)装置D的作用是
(4)实验中,为使
 缓慢通入烧瓶C,采取的操作是
缓慢通入烧瓶C,采取的操作是实验Ⅲ:测定某硫代硫酸钠样品的纯度(设样品中只含Na2SO3杂质)
设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品7.9g,配制成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用0.1mol·L-1I2标准溶液滴定(发生反应:2S2O
 +I2=S4O
+I2=S4O +2I-),至滴定终点共消耗标准溶液23.60mL。
+2I-),至滴定终点共消耗标准溶液23.60mL。(5)样品中Na2S2O3的百分含量为
您最近一年使用:0次
3 . 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
(1)K2FeO4中铁元素在周期表中的位置第___________ 周期第___________ 列。
(2)在溶液I中加入KOH固体的目的是___________(填字母)。
(3)“纯化”时需加入饱和的KOH溶液,其作用是___________ 。
(4)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为___________ 。每制得59.4 g K2FeO4,理论上消耗氧化剂的物质的量为___________ mol。
(5)工业上用异丙醇对湿产品进行洗涤,目的是___________ 。
(6)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,写出该反应的离子方程式:___________ 。
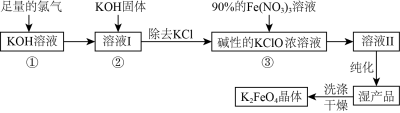
(1)K2FeO4中铁元素在周期表中的位置第
(2)在溶液I中加入KOH固体的目的是___________(填字母)。
| A.为下一步反应提供碱性的环境 |
| B.使KClO3转化为KClO |
| C.与溶液I中过量的Cl2继续反应,生成更多的KClO |
| D.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
(3)“纯化”时需加入饱和的KOH溶液,其作用是
(4)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为
(5)工业上用异丙醇对湿产品进行洗涤,目的是
(6)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
4 . 通过测定混合气中O2含可计算已变质的Na2O2(含Na2CO3)纯度的实验装置如图(Q为弹性良好的气囊)。下列分析正确的是
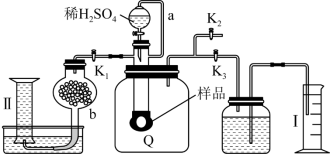
| A.b球形干燥管中装有氯化钙,用于除去气体中的水蒸气 |
| B.测定气体总体积必须关闭K1、K2,打开K3 |
| C.量筒Ⅰ用于测二氧化碳的量,干燥管b中装入碱石灰,量筒Ⅱ用于测氧气的量 |
| D.读完气体总体积后,关闭K3,缓缓打开K1、K2;可观察到Q气球慢慢变大 |
您最近一年使用:0次
名校
解题方法
5 . 将等物质的量的铁和铜的混合物24 g与600 mL稀硝酸恰好完全反应,生成NO 6.72 L(标准状况 ,向反应后的溶液中加入1mol/LNaOH溶液使金属离子恰好沉淀,过滤。下列有关说法正确的是
,向反应后的溶液中加入1mol/LNaOH溶液使金属离子恰好沉淀,过滤。下列有关说法正确的是
 ,向反应后的溶液中加入1mol/LNaOH溶液使金属离子恰好沉淀,过滤。下列有关说法正确的是
,向反应后的溶液中加入1mol/LNaOH溶液使金属离子恰好沉淀,过滤。下列有关说法正确的是| A.混合物溶解后的溶液中c(Fe3+):c(Fe2+) = 1:2 |
| B.需加入NaOH溶液600 mL |
| C.最后所得沉淀在空气中充分加热可得固体32 g |
| D.稀硝酸的物质的量浓度是1 mol/L |
您最近一年使用:0次
名校
6 . 微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以 溶液作模拟海水,采用惰性电极,用下图装置处理有机废水(以含CH3COO- 的溶液为例)。下列说法正确的是
溶液作模拟海水,采用惰性电极,用下图装置处理有机废水(以含CH3COO- 的溶液为例)。下列说法正确的是
 溶液作模拟海水,采用惰性电极,用下图装置处理有机废水(以含CH3COO- 的溶液为例)。下列说法正确的是
溶液作模拟海水,采用惰性电极,用下图装置处理有机废水(以含CH3COO- 的溶液为例)。下列说法正确的是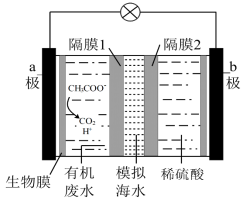
| A.负极反应为CH3COO-+2H2O-8e-=2CO2+7H+ |
| B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜 |
| C.b极每生成1 molH2,模拟海水理论上除盐58.5g |
| D.电池工作一段时间后,正、负极产生气体的物质的量之比为1:2 |
您最近一年使用:0次
7 . 下图的每一方格中表示有关的一种反应物或生成物,其中A、C、D、E为无色气体,F为红棕色气体。下列说法错误的是
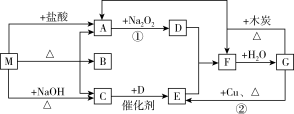
| A.D在一定条件下可以与C发生置换反应 |
| B.用蘸有浓盐酸的玻璃棒靠近瓶口可以检验C气体是否收集满 |
| C.M可能是纯净物或混合物 |
| D.F与水的反应中氧化剂与还原剂的物质的量之比为2∶1 |
您最近一年使用:0次
名校
解题方法
8 . 将15.6gNa2O2和5.4gAl 同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,下列说法错误的是
| A.最终溶液:c(Na+)= 2 mol·L-1 | B.标准状况下,反应过程中得到6.72L气体 |
| C.最终溶液:c(Na+) >c(Cl-) | D.最终得到7.8 g沉淀 |
您最近一年使用:0次
名校
解题方法
9 . M、W、X、Y、Z是同周期主族元素,X原子的最外层电子数是W原子次外层电子数的3倍,R元素是无机非金属材料的主角。M、W、X、Y、Z形成的化合物的结构如图所示。下列说法正确的是
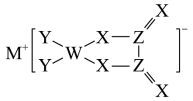
| A.M的单质通常保存在煤油中 | B.R的氧化物能溶于Y的氢化物的水溶液 |
| C.图中W原子不满足8电子稳定结构 | D.X、Y、Z的最简单氢化物的沸点:Y>X>Z |
您最近一年使用:0次
名校
10 . 设NA为阿伏加德罗常数的值,下列叙述中一定正确的是
| A.—定条件下,向0.1L容器内通入4.6 g NO2气体,NO2的物质的量浓度为1mol/L |
| B.标准状况下,2.24 L HF中含有的极性键数目为0.1NA |
| C.50mL0.1mol/LCH3COOH溶液和 10mL0.5mol/LCH3COOH溶液中所含CH3COOH分子数不相等 |
| D.1molFe与高温水蒸气反应,转移电子的数目为3NA |
您最近一年使用:0次



