1 . 设 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是
 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是A.16g  所含分子数为 所含分子数为 |
B.22.4L  与足量的铁反应,转移的电子数为 与足量的铁反应,转移的电子数为 |
C.1mol/L的NaCl溶液中含 的数目为 的数目为 |
D.1mol  中含有的离子数目为 中含有的离子数目为 |
您最近一年使用:0次
2024-07-12更新
|
268次组卷
|
2卷引用:2024年天津市河东区普通高中学业水平合格性考试模拟考试化学试卷
2 . 我国空间站“天和”核心舱太阳翼电池采用自主研发的砷化镓器件,能量转化效率大大提高。
已知:砷(As)与镓(Ga)同位于第四周期;Ga与Al同主族,As与P同主族。
(1)铝元素的原子结构示意图为___________ 。
(2)P在元素周期表中的位置是___________ 。
(3)P的非金属性弱于S的,用原子结构解释原因:P和S在同一周期,原子核外电子层数相同,___________ ,得电子能力P弱于S。
(4)下列关于Ga的推断正确的是___________ (填字母)。
a.最外层电子数为5
b.原子半径:
c.元素的金属性:
(5)氮的简单氢化物的电子式___________ , ,
, ,
, 的酸性由强到弱的关系是
的酸性由强到弱的关系是___________ 。
(6)三价砷有剧毒,五价砷毒性减弱。含 的污水可被次氯酸钠碱性溶液转化为
的污水可被次氯酸钠碱性溶液转化为 而降低毒性。该反应的离子方程式是
而降低毒性。该反应的离子方程式是___________ 。
已知:砷(As)与镓(Ga)同位于第四周期;Ga与Al同主族,As与P同主族。
(1)铝元素的原子结构示意图为
(2)P在元素周期表中的位置是
(3)P的非金属性弱于S的,用原子结构解释原因:P和S在同一周期,原子核外电子层数相同,
(4)下列关于Ga的推断正确的是
a.最外层电子数为5
b.原子半径:

c.元素的金属性:

(5)氮的简单氢化物的电子式
 ,
, ,
, 的酸性由强到弱的关系是
的酸性由强到弱的关系是(6)三价砷有剧毒,五价砷毒性减弱。含
 的污水可被次氯酸钠碱性溶液转化为
的污水可被次氯酸钠碱性溶液转化为 而降低毒性。该反应的离子方程式是
而降低毒性。该反应的离子方程式是
您最近一年使用:0次
2024-07-12更新
|
66次组卷
|
2卷引用:2024年天津市河东区普通高中学业水平合格性考试模拟考试化学试卷
3 . 下列说法正确的是
| A.氯化铁溶液具有氧化性,所以可用于制作印刷电路板 |
| B.植物油中含碳碳双键,所以可用于生产甘油 |
| C.硬铝强度高、密度大,所以是制造飞机的理想材料 |
| D.重金属盐能使蛋白质变性,所以吞服“钡餐”会引起中毒 |
您最近一年使用:0次
名校
解题方法
4 . 某地区已探明有着丰富的赤铁矿(主要成分为 ,还含有
,还含有 等杂质)、煤、石灰石和黏土。现拟在该地区建设大型炼铁厂,同时需要在该地区相应建立焦化厂、发电厂、水泥厂等,以形成一定规模的工业体系。下列说法
等杂质)、煤、石灰石和黏土。现拟在该地区建设大型炼铁厂,同时需要在该地区相应建立焦化厂、发电厂、水泥厂等,以形成一定规模的工业体系。下列说法不正确 的是
 ,还含有
,还含有 等杂质)、煤、石灰石和黏土。现拟在该地区建设大型炼铁厂,同时需要在该地区相应建立焦化厂、发电厂、水泥厂等,以形成一定规模的工业体系。下列说法
等杂质)、煤、石灰石和黏土。现拟在该地区建设大型炼铁厂,同时需要在该地区相应建立焦化厂、发电厂、水泥厂等,以形成一定规模的工业体系。下列说法
| A.甲、乙、丙、丁对应的工厂依次为发电厂、焦化厂、炼铁厂和水泥厂 |
| B.炼铁厂的炉渣可作为水泥厂的原料 |
| C.焦化厂对煤进行脱硫脱硝等处理后,可有效减少温室气体排放 |
| D.可配套建设化肥厂以充分利用焦化厂中煤干馏时的出炉煤气 |
您最近一年使用:0次
5 . 请回答:
(1)①氮气的电子式是_______ ,②乙醛的结构简式是_______ 。
(2)过氧化钠与水反应的化学方程式是_______ 。
(3)乙烯在空气中燃烧,可观察到的现象是_______ 。
(1)①氮气的电子式是
(2)过氧化钠与水反应的化学方程式是
(3)乙烯在空气中燃烧,可观察到的现象是
您最近一年使用:0次
名校
6 . 氨是一种重要的化工产品和化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
(1)物质A是_______ 。
(2)加热条件下氨能使黑色的氧化铜变红,体现了氨具有_______ 性。
(3)硝酸工业中的尾气 可用纯碱溶液吸收,生成
可用纯碱溶液吸收,生成 、
、 和一种气体,写出该反应的化学方程式
和一种气体,写出该反应的化学方程式_______ 。
(4)下列说法不正确 的是_______。
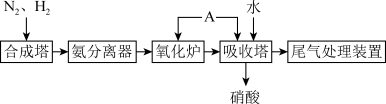
(1)物质A是
(2)加热条件下氨能使黑色的氧化铜变红,体现了氨具有
(3)硝酸工业中的尾气
 可用纯碱溶液吸收,生成
可用纯碱溶液吸收,生成 、
、 和一种气体,写出该反应的化学方程式
和一种气体,写出该反应的化学方程式(4)下列说法
A. 能使湿润的蓝色石蕊试纸变红 能使湿润的蓝色石蕊试纸变红 |
| B.合成氨反应中,使用催化剂能提高单位时间内氨的产量 |
| C.工业生产中贮存浓硝酸,可选用金属铝做罐体材料 |
D.在一定条件下 与 与 转化为氮肥的过程,属于人工固氮 转化为氮肥的过程,属于人工固氮 |
您最近一年使用:0次
名校
7 . 某电池以 和Zn为电极材料,KOH溶液为电解质溶液。该电池总反应:
和Zn为电极材料,KOH溶液为电解质溶液。该电池总反应: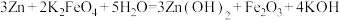 。下列说法正确的是
。下列说法正确的是
 和Zn为电极材料,KOH溶液为电解质溶液。该电池总反应:
和Zn为电极材料,KOH溶液为电解质溶液。该电池总反应: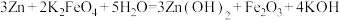 。下列说法正确的是
。下列说法正确的是A.电池工作时 向负极迁移 向负极迁移 |
B.正极反应式为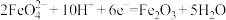 |
| C.该电池放电过程中电解质溶液浓度不变 |
| D.电子由Zn电极流出,经KOH溶液流向正极 |
您最近一年使用:0次
名校
解题方法
8 . 海带中含有碘元素,从海带中提取碘的实验过程如下图所示:不正确 的是

| A.步骤①会用到酒精灯、泥三角、三脚架、坩埚和坩埚钳等仪器 |
| B.步骤③和⑥中的操作均为过滤 |
C.步骤④中发生的离子方程式为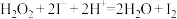 |
| D.海带灰中含有的硫酸盐,可在步骤⑤中实现与碘分离 |
您最近一年使用:0次
名校
9 . 将盛有 粉末的小烧杯放入盛有少量液态醋酸的大烧杯中,然后向小烧杯中加入盐酸。可观察到
粉末的小烧杯放入盛有少量液态醋酸的大烧杯中,然后向小烧杯中加入盐酸。可观察到 与盐酸剧烈反应,醋酸逐渐凝固。下列说法
与盐酸剧烈反应,醋酸逐渐凝固。下列说法不正确 的是
 粉末的小烧杯放入盛有少量液态醋酸的大烧杯中,然后向小烧杯中加入盐酸。可观察到
粉末的小烧杯放入盛有少量液态醋酸的大烧杯中,然后向小烧杯中加入盐酸。可观察到 与盐酸剧烈反应,醋酸逐渐凝固。下列说法
与盐酸剧烈反应,醋酸逐渐凝固。下列说法| A.醋酸由液态转化为固态时放出热量 |
B. 与盐酸的反应中,热能转化为产物内部的能量 与盐酸的反应中,热能转化为产物内部的能量 |
C. 与盐酸的反应中,反应物的总能量高于生成物的总能量 与盐酸的反应中,反应物的总能量高于生成物的总能量 |
D. 和盐酸的反应中,涉及离子键、共价键的断裂 和盐酸的反应中,涉及离子键、共价键的断裂 |
您最近一年使用:0次
名校
解题方法
10 . 下表中的科学家、其主要贡献及意义的对应关系不正确 的是
| 选项 | 科学家 | 主要贡献及意义 |
| A | 拉瓦锡 | 提出元素的概念,标志着近代化学的诞生 |
| B | 道尔顿 | 提出原子学说,为近代化学的发展奠定了坚实的基础 |
| C | 门捷列夫 | 发现元素周期律,使化学的研究变得有规律可循 |
| D | 侯德榜 | 发明联合制碱法,为我国的化工发展和技术创新做出了重要贡献 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



