23-24高一下·全国·课前预习
解题方法
1 . 化学能
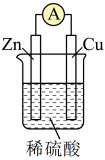
(1)如图所示,请写出锌与稀硫酸反应的化学方程式___________ 。
(2)装置中锌片上发生___________ (“氧化”或“还原”)反应,能证明化学能转化为电能的实验现象为___________ 。装置中锌片表面如何变化___________ ?电流表是否偏转___________ ?
(3)Cu的作用是___________ 。
a.离子导体 b.电子导体

(1)如图所示,请写出锌与稀硫酸反应的化学方程式
(2)装置中锌片上发生
(3)Cu的作用是
a.离子导体 b.电子导体
您最近一年使用:0次
解题方法
2 . 钢铁的电化学腐蚀
(1)实验探究——钢铁的电化学腐蚀原理
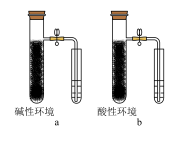
①向铁粉中加入碳粉的目的是___________ ;
②实验现象:a装置右边的小试管中液面________ ;b装置中右边小试管中液面_________ 。
(2)钢铁的电化学腐蚀
根据钢铁表面水溶液薄膜的酸碱性不同,钢铁的电化学腐蚀分为析氢腐蚀和吸氧腐蚀,如下图所示:
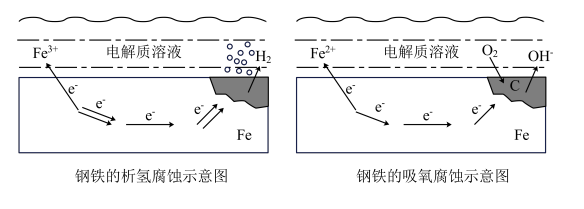
①钢铁的吸氧腐蚀:
通常情况下,在潮湿的空气中,钢铁表面凝结了一层溶有氧气的水膜,将会发生___________ 腐蚀。
负极反应式:_________ ;正极反应式:________ 。
总反应式:___________ 。
Fe(OH)2被进一步氧化成Fe(OH)3:___________ ,Fe(OH)3部分脱水生成Fe2O3·nH2O,是铁锈的主要成分。
②钢铁的析氢腐蚀:
当钢铁表面的电解质溶液_______ 较强时,腐蚀过程中有________ 放出。其中,Fe是_________ 极,C是__________ 极。
负极反应式:___________ ;正极反应式:__________ 。
总反应式:___________ 。
随着了氢气的析出,溶液的pH上升,最终形成铁锈。
(1)实验探究——钢铁的电化学腐蚀原理

①向铁粉中加入碳粉的目的是
②实验现象:a装置右边的小试管中液面
(2)钢铁的电化学腐蚀
根据钢铁表面水溶液薄膜的酸碱性不同,钢铁的电化学腐蚀分为析氢腐蚀和吸氧腐蚀,如下图所示:

①钢铁的吸氧腐蚀:
通常情况下,在潮湿的空气中,钢铁表面凝结了一层溶有氧气的水膜,将会发生
负极反应式:
总反应式:
Fe(OH)2被进一步氧化成Fe(OH)3:
②钢铁的析氢腐蚀:
当钢铁表面的电解质溶液
负极反应式:
总反应式:
随着了氢气的析出,溶液的pH上升,最终形成铁锈。
您最近一年使用:0次
3 . 配合物的制备和应用
【活动探究】结合课本完成探究实验,完成下表
【活动探究】结合课本完成探究实验,完成下表
| 实验任务 | 实验过程与现象 | 结论 |
| 1.探究氯化铜固体在溶解并稀释过程中所发生的变化 | ———— | |
| 2.分别以氯化铁和硝酸铁为原料,探究Fe3+溶液显色的原因 | ||
| 3.制备[Ag(NH3)2]+并用于与葡萄糖反应得到银镜 | ||
| 4.对比Cu2+与氨水和OH-反应的差异 |
您最近一年使用:0次
4 . 炔烃的结构和性质
(1)炔烃
炔烃的官能团是___________ ,一般只含有一个官能团时通式为___________ (n≥2)。炔烃的物理性质的递变规律与烷烃和烯烃的___________ ,沸点随分子中碳原子数的递增而___________ ,常温下,碳原子数不大于___________ 的炔烃为气态。
(2)乙炔的物理性质
乙炔(俗称___________ )是最简单的炔烃。乙炔是___________ 色、___________ 的气体,___________ 溶于水,___________ 溶于有机溶剂。
(3)乙炔的表示方法及结构特点
分子式:___________ ,电子式:___________ ,结构式:___________ ,结构简式:___________ ,键线式:___________ 。
乙炔分子为___________ 形结构,相邻两个键之间的夹角为___________ ,碳原子采取___________ 杂化。
(4)乙炔的化学性质
(i)实验探究(课本P35)
为减小电石与水反应的速率,可用___________ 代替水作反应试剂。
(ii)化学性质
①氧化反应
a.乙炔的燃烧:___________ 。
b.可使酸性KMnO4溶液___________ 。
②加成反应
a.乙炔与溴的反应:___________ (1,2-二溴乙烯);___________ (1,1,2,2-四溴乙烷)。
b.乙炔与氢气的反应(1:1):___________ 。
c.乙炔与HCl的反应(1:1):___________ 。
d.乙炔与H2O的反应:___________ 。
③加聚反应:___________ ,聚乙炔可用于制备___________ 材料。
(1)炔烃
炔烃的官能团是
(2)乙炔的物理性质
乙炔(俗称
(3)乙炔的表示方法及结构特点
分子式:
乙炔分子为
(4)乙炔的化学性质
(i)实验探究(课本P35)
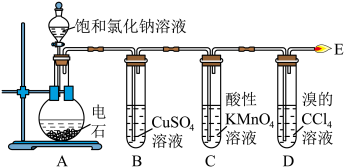
| 实验现象 | 结论或化学方程式 | |
| A | 反应 | |
| B | 有 | 乙炔中的杂质气体 |
| C | 溶液紫红色褪去 | |
| D | 溶液橙红色褪去 | |
| E | 火焰 | CH≡CH |
(ii)化学性质
①氧化反应
a.乙炔的燃烧:
b.可使酸性KMnO4溶液
②加成反应
a.乙炔与溴的反应:
b.乙炔与氢气的反应(1:1):
c.乙炔与HCl的反应(1:1):
d.乙炔与H2O的反应:
③加聚反应:
您最近一年使用:0次
5 . 苯的卤代反应
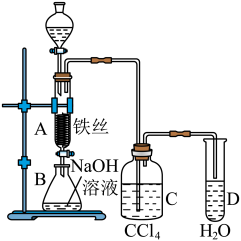
【溴苯制备实验总结】
(1)实验现象:
①反应迅速进行,溶液几乎“沸腾”。
②反应结束后,三颈烧瓶底部出现红褐色油状液体(溴苯)。
③锥形瓶内有白雾,向锥形瓶中加入AgNO3溶液,出现浅黄色沉淀。
④向三颈烧瓶中加入NaOH溶液,产生红褐色沉淀[Fe(OH)3]。
(2)注意事项:
①此处反应物为_________ 。而溴水与苯不能发生取代反应,而是萃取,分层后,水在下层,溶溴的苯在上层。
②苯与液溴反应________ 才能进行。虽然加入铁粉,但实际起催化作用的是:2Fe+3Br2=2FeBr3,上述实验中加入NaOH溶液,即可验证有Fe3+的存在。
③直形冷凝管的作用——________ (HBr和少量溴蒸气能通过)。
④导管不可插入液面下,以防_______ ,管口附近出现的________ ,是________ 遇水蒸气所形成的。
⑤生成物纯净的溴苯是一种无色的液体,密度比水大,难溶于水。烧瓶中生成的溴苯因溶入溴而显褐色,其提纯的方法是将溶有溴的溴苯倒入盛有________ 的烧杯中,振荡,溴苯比水重,沉在下层,用________ 分离出溴苯。反应的化学方程式为:________ 。

【溴苯制备实验总结】
(1)实验现象:
①反应迅速进行,溶液几乎“沸腾”。
②反应结束后,三颈烧瓶底部出现红褐色油状液体(溴苯)。
③锥形瓶内有白雾,向锥形瓶中加入AgNO3溶液,出现浅黄色沉淀。
④向三颈烧瓶中加入NaOH溶液,产生红褐色沉淀[Fe(OH)3]。
(2)注意事项:
①此处反应物为
②苯与液溴反应
③直形冷凝管的作用——
④导管不可插入液面下,以防
⑤生成物纯净的溴苯是一种无色的液体,密度比水大,难溶于水。烧瓶中生成的溴苯因溶入溴而显褐色,其提纯的方法是将溶有溴的溴苯倒入盛有
您最近一年使用:0次
6 . 烯烃、炔烃的化学性质:
(1)加成反应
①与 X2(条件:水溶液或CCl4溶液)
现象:溴水___________
溴的CCl4溶液___________
CH3CH=CH2+Br2→___________
CH≡CH+Br2→___________
CHBr=CHBr+Br2→___________
产物怎么命名呢?___________ 、___________ 、___________
【应用】上述反应可以用于烯烃与烷烃或炔烃与烷烃的鉴别。
②与 H2(条件:催化剂)
有关方程式:
乙炔+氢气:___________
乙烯+氢气:___________
③与氢卤酸:例与HCl(条件:催化剂、加热)
CH3CH=CH2+HCl
___________
CH3CH=CH2+HCl
___________
CH≡CH+HCl
___________
【应用】工业上获得卤代烃。例如,工业上利用乙炔和HCl的加成反应制备氯乙烯。
④与水:(条件催化剂、加热、加压)
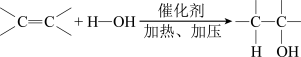
⑤加成聚合反应(简称加聚反应)条件:一定条件
nCH3CH CH2
CH2
___________
nHC CH
CH
___________
【注意】:聚乙炔在掺杂状态下具有较高的电导率。
(2)氧化反应
①可燃性:___________
②与酸性KMnO4的反应。现象:___________ 。
(1)加成反应
①与 X2(条件:水溶液或CCl4溶液)
现象:溴水
溴的CCl4溶液
CH3CH=CH2+Br2→
CH≡CH+Br2→
CHBr=CHBr+Br2→
产物怎么命名呢?
【应用】上述反应可以用于烯烃与烷烃或炔烃与烷烃的鉴别。
②与 H2(条件:催化剂)
有关方程式:
乙炔+氢气:
乙烯+氢气:
③与氢卤酸:例与HCl(条件:催化剂、加热)
CH3CH=CH2+HCl

CH3CH=CH2+HCl

CH≡CH+HCl

【应用】工业上获得卤代烃。例如,工业上利用乙炔和HCl的加成反应制备氯乙烯。
④与水:(条件催化剂、加热、加压)
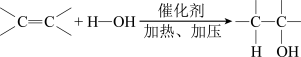
⑤加成聚合反应(简称加聚反应)条件:一定条件
nCH3CH
 CH2
CH2
nHC
 CH
CH
【注意】:聚乙炔在掺杂状态下具有较高的电导率。
(2)氧化反应
①可燃性:
②与酸性KMnO4的反应。现象:
您最近一年使用:0次
7 . 实验室可使用如图所示的装置探究Cu与浓硫酸的反应。
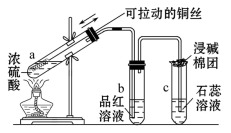
(1)通过什么现象证明H2SO4的还原产物是SO2_____ ?哪些措施可以减少(或消除)SO2对环境的污染____ ?
(2)过量的铜与一定量的浓硫酸反应时,硫酸能否全部参加反应____ ?

(1)通过什么现象证明H2SO4的还原产物是SO2
(2)过量的铜与一定量的浓硫酸反应时,硫酸能否全部参加反应
您最近一年使用:0次
8 . 乙酸的化学性质
【实验探究一】乙酸的酸性乙酸在溶于水时能够电离出CH3COO-和H+,因而乙酸具有一定的酸性。请小组内合作利用所给的试剂设计几个实验证明乙酸具有酸性。完成下面表格:
总结:乙酸的酸性
①_______ ;
②_______ ;
③_______ ;
④_______ ;
⑤_______ ;
【实验探究二】在试管中加入无水乙醇、浓硫酸、冰醋酸的混合物,再加入2~3块碎瓷片。按下图所示连接装置,用酒精灯小心均匀地加热试管,将产生的气体经导管通到饱和Na2CO3溶液的液面上。观察发生的现象,闻一闻生成物的气味。
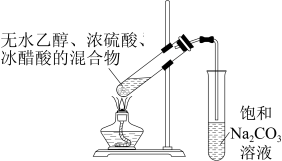
现象:_______ 。
结论:_______ 。
反应方程式:_______ 。
酯化反应:_______ 。
酯化反应原理:酸脱去_______ ,醇脱去_______ 。
【交流研讨】
a.反应中浓硫酸的作用是什么?碎瓷片的作用是什么?_______ 。
b.为什么反应物都必须是无水液体?_______ 。
c.为什么要用饱和Na2CO3溶液吸收产物?_______ 。
d.为什么导气管不能伸入饱和Na2CO3溶液中?_______ 。
【实验探究一】乙酸的酸性乙酸在溶于水时能够电离出CH3COO-和H+,因而乙酸具有一定的酸性。请小组内合作利用所给的试剂设计几个实验证明乙酸具有酸性。完成下面表格:
| 实验内容 | 实验现象 | 反应的化学方程式 |
| 向试管中加入约2mL乙酸溶液,然后滴入数滴紫色石蕊试液,观察颜色变化 | 溶液变红 | |
| 向试管中加入适量锌粒,然后加入约2mL冰醋酸溶液 | 溶液中有气泡生成 | |
| 向试管中加入适量碳酸钙,然后加入约2mL冰醋酸溶液 | 碳酸钙溶解,有大量气泡生成 | |
| 向试管中加入约2mLNaOH溶液,滴入数滴酚酞溶液,然后逐滴滴加乙酸溶液,观察颜色变化 | 溶液由红色逐渐变为无色 |
总结:乙酸的酸性
①
②
③
④
⑤
【实验探究二】在试管中加入无水乙醇、浓硫酸、冰醋酸的混合物,再加入2~3块碎瓷片。按下图所示连接装置,用酒精灯小心均匀地加热试管,将产生的气体经导管通到饱和Na2CO3溶液的液面上。观察发生的现象,闻一闻生成物的气味。

现象:
结论:
反应方程式:
酯化反应:
酯化反应原理:酸脱去
【交流研讨】
a.反应中浓硫酸的作用是什么?碎瓷片的作用是什么?
b.为什么反应物都必须是无水液体?
c.为什么要用饱和Na2CO3溶液吸收产物?
d.为什么导气管不能伸入饱和Na2CO3溶液中?
您最近一年使用:0次
解题方法
9 . 某研究小组用如图所示装置制取乙酸乙酯,请回答下列问题:
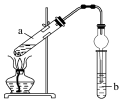
(1)为防止试管a中液体实验时发生暴沸,加热前应采取的措施为___________ 。
(2)装置中的球形漏斗除起冷凝作用外,它的另一重要作用是___________ 。
(3)试管b中饱和碳酸钠溶液的作用除了溶解乙醇,还有___________ ,___________ 。
(4)待试管b收集到一定量产物后停止加热,撤去试管b并用力振荡试管b,静置后试管b中所观察到的实验现象:___________ ,要分离试管中的液体混合物,采用的方法为___________ 。
(5)如果用含示踪原子18O的乙醇参与反应,生成的产物中,只有乙酸乙酯中含有18O,则酯化反应中,乙酸和乙醇分子中断裂的各是什么键,在方程式中表示出其断键部位:____________ 。

(1)为防止试管a中液体实验时发生暴沸,加热前应采取的措施为
(2)装置中的球形漏斗除起冷凝作用外,它的另一重要作用是
(3)试管b中饱和碳酸钠溶液的作用除了溶解乙醇,还有
(4)待试管b收集到一定量产物后停止加热,撤去试管b并用力振荡试管b,静置后试管b中所观察到的实验现象:
(5)如果用含示踪原子18O的乙醇参与反应,生成的产物中,只有乙酸乙酯中含有18O,则酯化反应中,乙酸和乙醇分子中断裂的各是什么键,在方程式中表示出其断键部位:
您最近一年使用:0次
10 . 酸性
羧酸是一类弱酸,具有酸类的共同性质。
(1)实验探究羧酸的酸性
(2)实验探究酸性的强弱
比较乙酸、碳酸和苯酚的酸性强弱
羧酸是一类弱酸,具有酸类的共同性质。
(1)实验探究羧酸的酸性
| 实验操作 | 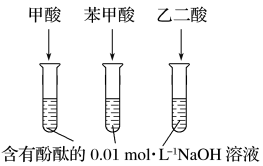 |
| 实验现象 | |
| 实验结论 |
(2)实验探究酸性的强弱
比较乙酸、碳酸和苯酚的酸性强弱
| 实验装置 |  |
| B装置的现象及解释 | 有 化学方程式:2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O |
| D装置的现象及解释 | 溶液 化学方程式: 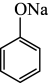 +CO2+H2O→ +CO2+H2O→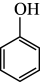 +NaHCO3 +NaHCO3 |
| C装置的作用 | 除去B中挥发的 |
| 实验结论 | 酸性:乙酸 |
您最近一年使用:0次



